Introduction
질소는 생물학적 고정, 무기화, 부동화, 휘산 등의 다양한 순환경로를 통해 복잡한 형태로 토양내 존재한다 (Scolow, 1999). 식물의 뿌리가 흡수할 수 있는 질소의 형태는 주로 용해된 질산태 질소 (NO3--N)와 암모늄태 질소 (NH4+-N)이다 (Li et al., 2013). 따라서 무기태 질소는 작물의 생장과 수량에 가장 큰 제한 요인 중 하나이다 (Fageria and Baligar, 2005).질소가 과다하게 사용되면 수계에 유출되어 부영양화, 지하수 오염 등 환경과 건강문제를 일으킨다 (Rabalais et al., 2002). 또한 토양에서 80% 이상의 질소가 유기물 형태로 존재하며 (Schulten and Schnitzer, 1998), 주로 미생물의 무기화 작용을 통해 생물에 유효한 형태로 전환된다 (Schimel and Bennett, 2004).
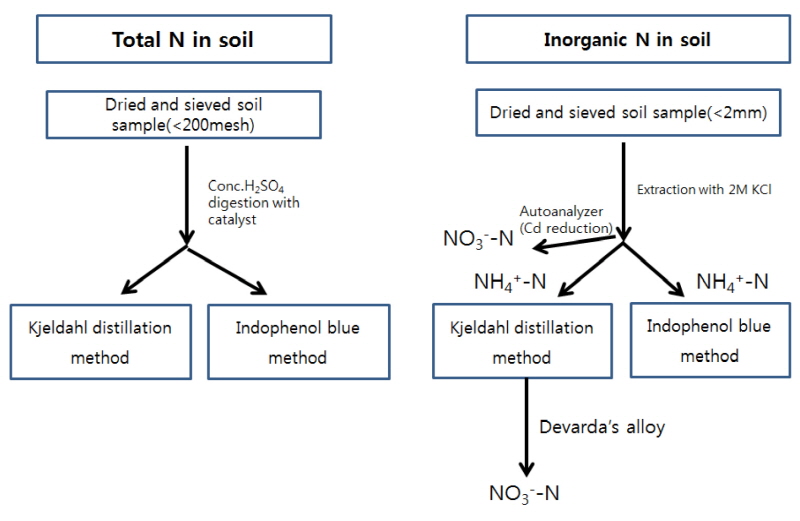
토양과 같이 불균질한 물질 내에 존재하는 질소의 분석은 까다롭다. 따라서 신속‧정확하게 토양 중 질소를 분석하는 것은 토양 내 질소의 동태를 이해하거나 적정 질소 비료 사용량 결정 등 지속가능한 농업을 위해 반드시 필요하다. 이를 위해 토양 내 전질소 (total N)와 토양 침출액 중의 무기태 질소를 분석하기 위한 많은 분석 방법이 개발되었다(Pansu and Gautheyrou, 2007). 이에 본문에서는 국내에서 농경지 토양 전질소와 무기태 질소 분석에 일반적으로 사용되고 있는 분석방법을 제시하고자 한다 (Fig. 1).
토양 시료 채취 및 시료 전처리 한 개의 시험구 내에서 20~30개 지점의 토양을 채취한다 (단, 비옥도가 균일한 토양의 경우는 5~10개 지점도 가능하다). 표토는 식물의 뿌리가 분포하는 약 15 cm깊이에서 심토는 작토층 아래에서 30 cm 깊이까지 균일한 토양부피가 되도록 채취한다. 채취한 토양시료는 20~25°C 온도와 20~60% 습도가 유지되는 실내에서 건조한다. 풍건된 시료는 전량을 모래나 자갈이 깨어지지 않도록 고무롤러나 나무방망이 또는 토양분쇄기를 사용하여 분쇄한다. 분쇄된 시료는 2 mm 체를 통과시키고 전질소분석에 사용되는 시료의 경우 2 mm 체를 통과한 토양을 유발로 갈아서 0.5 mm 체를 전량 통과시켜 사용한다. 체질한 시료는 균일하지 않으므로 잘 혼합한다 (RDA, 2012).
전질소 토양 중 전질소함량은 심토에서 0.02% 이하, 이탄토에서 2.5% 이상으로 보고되고 있다. 대부분 경작지표층 토양의 전질소함량은 0.06~0.5%이다. 전질소 함량의 정량법은 건식산화방법에 의한 Dumas법과 습식산화방법을 이용한Kjeldahl법이 있다 (Sparks, 1996).
Dumas법은 질소화합물을 질소가스로 변환시킨 후 표준조건 하에서 단위중량으로부터 질소량을 산출하는 원소분석법으로써 정제된 CO2가스 속에서 시료에 산화구리 (CuO)를 혼합하여600°C이상의 고온에서 가열하면 Cu에 결합된 N2O는 N2로 환원되고 CO가스는 CuO와 산화반응에 의하여 다시 CO2로 변환된다. N2-CO2혼합물은 농축된 알칼리물질을 함유하고 있는 질소계 (nitrometer)에 포집되어 CO2는 흡수되고 N2가스의 부피만 측정된다. Stewart et al. (1963)는 유기물함량이 높은 토양을 Dumas법으로 분석했을 때 불완전연소에 의해 CO2대신 생성된 CH4으로 인해 분석값이 높게 나온다고 하였다. 이후 이러한 단점을 보완하기 위해 정제된 O2가스를 이용하는 장비들이 개발되었다. 그러나 고가의 장비, 시료를 마쇄하는 전처리, 분석시간이 길다는 단점으로Dumas법은 제한적으로 사용되고 있다 (Keeney and Bremner, 1967).
Kjeldahl법은 시료 중 유기태질소를 농황산으로 분해하여 NH4+-N으로 환원시키고NaOH와 같은 강염기하에 분해액을 증류하면서 NH3 가스를 포집하여 분석하는 원리이다 (Sparks, 1996). Kjeldahl 법으로 전질소를 분석할 경우풍건하여 0.5 mm체를 통과한 토양 시료 5 g을 켈달플라스크에 넣고 농황산 25 mL을 넣은 후 분해 촉진제로 황산염혼합분말 (K2SO4:CuSO4=9:1) 5 g을 넣는다. 분해용 전기로에서 처음에는 낮은 온도로 10~30분 가열하고 산화가 완료된 후 400 ± 20°C에서 4 시간 고열로 분해한다 (이때 분해온도가 360°C 이하가 되면 불완전하여 분해시간이 지연되고, 410°C이상에서는 휘산에 의한 손실이 있다). 시료가 무색이 된 후 (촉매제로 인해 토양의 색은 무색으로 되나 시료는 엷은 청색을 띤다) 30분 내지 1시간 분해를 계속한다. 켈달플라스크가 냉각되면 증류수 350 ml를 넣고 잘 섞어준다. Block digester를 이용하여 분해할 경우 토양시료의 양은 0.5~1.0 g, 황산염혼합분말은 1.5 g, 농황산은 3~5 ml 가한 후 시료가 무색이 되면 냉각 후 분해관의 표선까지 증류수로 눈금을 맞춘다 (RDA, 2012; NIAST, 2000).
분해된 시료의 질소는 크게 증류법과 비색법으로 정량한다. Kjeldahl증류법으로 측정할 경우 Heating mentle을 장치한 후 그 위에 증류수를 2/3정도채운 3~5 L용 둥근플라스크를 설치한 다음 가열된 뜨거운 증기를 이용하여 시료를 가열한다. 켈달증류장치에 있는 냉각관에 수돗물을 틀어 흐르게 하고 2% 붕산용액 (Bromo cresol green과methyl red 시약함유, pH 4.5) 10 ml를 준비해 놓는다. 분해된 시료에 45% NaOH용액 50 mL을 가하여 산성을 alkali화 한다. 신속하게 켈달플라스크를 연결하고 수기에 약 75 ml쯤 증류되면 수기를 뗀다. 붕산용액에 포집된NH4-N을 0.005 M (0.01 N) H2SO4용액을 이용해 옅은 분홍색 (종말점)이 나타날 때까지 적정한다 (NIAST, 2000). 토양 시료 내 전질소 함량은 다음 식으로 계산한다.
T-N (%) = (T-B) × N × f × 14 × 1/1000 (ml) × 1/W × 100
T: 시료 적정에 소요된 황산표준용액의 ml
B: Blank의 적정에 소요된 황산표준용액의 ml
f: 황산표준용액의 보정치(factor)
N: 황산표준용액의 Normality
W: 토양시료의무게 (g)
Indophenol blue 비색법은 용액 중에 있는 암모늄태 질소가 phenol과 과염소산소다가 있을 때 sodium nitroprusside를 촉매로 하여 Indophenol (blue)을 만드는 원리이다. Indophenol blue 비색법으로 전질소를 분석할 경우 분해된 시료를 증류수로 녹여 100 mL로 맞춘다. 이때 pH 11 이하에서는 발색에 영향을 받기 때문에 분해액을 다시 2배 이상 희석한다. 분해액 1 mL를 시험관에 취하고 phenol-sodium nitroprusside-EDTA 혼합용액 3 mL를 넣고 37°C에서 5분간 둔 뒤 phosphate-sodium hypochlorite 혼합액 5 mL를 넣고 잘 흔들어준다. 20분간 30°C에서 항온시켜 665 nm에서 비색 정량한다 (RDA, 2012).
무기태 질소 최근 극지방이나 툰드라 고산지대와 같이 질소가 심하게 제한될 경우 식물체가 아미노산 형태의 용해된 유기태질소 (dissolved organic N, DON)를 토양으로부터 미생물의 무기화 과정 없이 바로 흡수할 수 있다는 주장들이 제기되고 있다 (Henry and Jefferies, 2003; Nordin et al.,2004). 그러나 대부분의 식물은 토양으로부터 NH4+와 NO3-형태의 무기태 질소를 흡수한다 (Liu et al., 2008). NO2- (nitrite)는 중성 또는 염기성 토양에 NH4+를 비료를 시용할 때를 제외하고는 검출한계 이하로 극히 소량 존재한다. NH2OH (hydroxylamine), H2N2O2 (hyponitrous acid), NH2NO2 (nitamide)의 형태가 이론적으로 토양 내 존재하지만 이러한 형태들은 미생물에 의한 질소전환 (transformation)에서의 중간물질로써 열역학적으로 불안정한 화합물이기 때문에 토양에서 검출되지 않는다 (Sparks, 1996). 1950년대까지 중성염용액으로 토양을 침출하면 대부분의 NH4+-N와 NO3--N가 회수되며 이때 무기태 질소는 토양질소의 약 2% 미만을 차지한다고 보고되었다. 물론 일부 토양에서는 다른 양이온으로 교환할 수 없는 고정된 (fixed) NH4+ 또는 비치환성 (nonexchangeable) NH4+가 보고되었다 (Young, 1962). 고정된 NH4+는 토양을 알칼리성KOBr용액으로 처리하여 치환성 NH4+와 labile organic N화합물을 제거한 후 HF-HCl로 분해하여 분석한다. 공간적인 변이가 심해 치환성 NH4+, NO3-를 결정하는 것은 복잡하다 (Biggar, 1978). 이 형태들의 무기태 질소는 미생물에 의해 형태가 빠르게 변할 수 있다. 이러한 변화를 최소화하려면 토양 시료 채취 후 즉시 무기태 질소 분석을 해야한다 (Sparks, 1996). 그러나 대부분의 경우 토양을 운반하고 전처리하는 과정 등의 지연이 생기므로 미생물 성장을 최소화하는 냉동법 등 다양한 방법들이 고안되었다 (Breimer and Slangen, 1981). 하지만 냉동시료를 녹이는 과정에서 무기태 질소의 변화가 일어날 수 있어 실온에서 풍건하는 방법 (암모니아가스의 오염 우려가 없는 곳에서) (Bremner and Keeney, 1965)과 습토의 분석 (Keeney and Nelson, 1982)이 추천되고 있다.
암모늄태 질소 습토 10 g에 2 M KCl 50 mL을 넣어 30분간 진탕한 뒤 Whatman No. 2 여과지에 여과한다. Indophenol blue 비색법은 전 질소와 동일하다. Kjeldahl증류법으로 측정할 경우 여과액을 MgO로 알칼리화 시키고증류한 후 2% 붕산용액 50 mL에 포집된 NH4+-N을 0.01N H2SO4용액으로 적정한다. 암모늄태 질소의 계산은 다음과 같다.
NH4+-N (mg/kg) = (T-B) × N × f × 14 × 1/1000 (ml) × 침출액량*/취한 시료 액량 × 1/W × 1,000,000
T:시료 적정에 소요된 황산 표준용액의 ml
B:Blank의 적정에 소요된 황산 표준용액의 ml
f:황산 표준용액의 보정치 (factor)
N:황산 표준용액의 Normality
W:풍건 토양시료의 무게 (g)
*침출액량: 습토 분석의 경우는 침출액 + (습토무게-건토무게)로 한다 (NIAST, 2000).
질산태 질소질산태 질소의 침출 과정은 암모늄태 질소와 동일하다. Kjeldahl 증류법으로 측정할 경우 NH4+-N의 증류가 끝난 켈달플라스크에 de varda’s alloy를 넣어 NO3--N를 NH4+-N로 전환시킨 다음 다시 증류하면서 2% 붕산용액 50 mL에 포집된 NH4+-N을 0.005 M (0.01 N)H2SO4용액으로 적정한다. 자동원소분석기를 이용하여 NO3--N를 분석할 경우, 여과액의 질산성질소를 Cd을 이용하여 아질산성질소로 환원한 뒤 sulfanil amide에 의한 diaxotization 반응과 N-(1-naphthyl)-ethyl inediamine에 의한 coupling 반응을 이용하여 비색 정량한다 (RDA, 2012).
Conclusion
토양 내 전질소와 무기태 질소를 분석하는 방법에 대해 기술하였다. 토양의 전질소는 주로 분석값이 안정적이며 비교적 많은 시료를 분석할 수 있는Kjeldahl분해증류법으로 측정하는 것이 일반적이다. 토양 내 무기태 질소는 주로 질산태 질소와 암모늄태 질소로서 2 M KCl로 침출하여Kjeldahl분해증류법이나 Indophenol blue법으로 분석한다. 특히 비색법을 이용하여 무기태 질소를 분석할 경우 다가양이온 (예: Ca2+, Mg2+, Fe3+)의 간섭을 최소화하기 위해EDTA와 같은 킬레이트제를 처리하여 침출하는 것이 필요하다. 최근 습식분석 외에도 간이 진단장비를 이용하여 농업현장에서 질소 측정 분석법 개발에 대한 수요가 커지고 있다. 이러한 분석 방법의 활용성을 높이기 위해서는 분석결과의 신뢰성을 확보하기 위한 다양한 연구가 필요할 것이다.