Introduction
Materials and Methods
토양시료, 안정화제 및 시험식물
토양 내 pH 변화 및 중금속 유효태함량 분석
벼 생장반응 및 식물체 내 중금속 전함량 분석
데이터 분석과 통계처리
Results and Discussion
안정화제 처리에 따른 토양 내 pH 및 중금속 유효태함량 변화
안정화제 처리별 벼 중금속 함량 및 생육 변화
토양 pH, 유효태 침출법 및 벼 중금속함량 간의 상관관계
Conclusions
Introduction
비소는 다른 중금속과 달리 금속적 및 비금속적 성질을 동시에 지니고 있어 준금속으로 분류되고, 일반토양의 무기비소는 환원조건에서 As3+ (arsenic, As (III))형태로 존재하며 산화조건에서는 대부분 As5+ (arsenate, As (V))형태로 존재한다 (Jiang et al., 2014). 무기태인 3가 비소는 5가 비소보다 독성이 10배 정도 높다고 알려져 있으며 (Cao et al., 2003; Coelho et al., 2020; Jung et al., 2021), 폐암, 피부암, 간암 등을 일으키는 발암물질로 IARC (international agency for research on cancer)에서는 ‘1A’ 등급으로 분류하고 있다 (IARC, 2004). 토양 중금속오염은 식량안보 및 생태계의 위협요인일 뿐만 아니라, 국민건강에도 직 ‧ 간접적으로 영향을 미칠 수 있다. 2022년도 통계청 「농업면적조사」 자료에 의하면, 우리나라 경지면적 중 논 비율이 50.8% (775,640 ha)로 가장 넓은 면적을 차지하고 있을뿐더러 쌀을 주식으로 이용하기 때문에 국민건강증진을 위해선, 논토양 중금속오염으로부터 안전한 쌀 생산이 필수적으로 요구되며, 이에 따른 안전관리가 수반되어야 한다 (Statistics Korea, 2022). 그러므로, 우리나라는 비소오염으로부터 안전한 쌀 생산을 위하여, 토양은 토양환경보전법에 의거하여 25 mg kg-1, 그리고 백미의 무기비소는 식품공전에 의거하여 0.20 mg kg-1으로 우려기준을 설정하여 관리하고 있다 (Antoniadis et al., 2019; Jung et al., 2021). 농경지 토양 중 납 (Pb)오염은 농작물의 생육과 생산성 및 안전성에 직결된다. 또한 납은 작물에서 인체로 흡수되기 때문에 오염토양에서의 작물재배는 주의를 필요로 한다. 2019년도 전국 일반농경지 논토양 2,110지점에 대한 중금속 평균함량은 토양환경보전법의 토양오염 우려기준에 비하여 매우 낮은 수준 (0.01 - 0.19배)이었지만, 2021년 환경부의 토양오염실태조사에서 공업단지 인근 토양 중 납함량이 최대 485.9 mg kg-1으로 보고되었으며, 이는 우려기준 (200 mg kg-1)을 초과한 수치이다 (ME, 2021). 따라서 토양의 납 오염을 관리하기 위한 적절한 방법을 모색하는 것이 매우 중요하다.
현재 농경지 토양의 중금속 오염관리는 토양환경보전법에 따라 관리되고 있다. 그러나 중금속 우려기준 초과 농도로 광범위하게 오염된 농경지를 토양환경보전법 시행규칙에 맞는 복원을 추진한다면 고액의 예산이 투입되어야 하며, 예산이 확보되지 않으면 수년 동안 방치되는 것이 현실이다. 작물의 안전성을 강조하는 사회적 요구와 더불어 효과적인 농경지 토양의 중금속 오염복원 기술개발 또한 요구되었다. 이러한 시대적 패러다임에 부응하기 위하여, 영농학적 (경종적)으로 개량제 (amendment)를 이용한 토양 내 중금속 안정화 공법 (stabilization)에 관하여 다양한 연구가 진행되고 있다 (Hamid et al., 2018; Choi et al., 2020; Jung et al., 2021).
안정화 공법은 중금속 오염토양에 개량제 화합물을 투입함으로써, 토양 내 중금속의 존재 형태를 난용성 또는 저독성으로 변환시켜 잠재적인 위해성을 감소시키는 방법이다 (Kim et al., 2019). 산화환원 (redox), 산도 (pH) 등 토양환경변화는 중금속의 용해도에 크게 영향을 주고 있으며, 논토양과 같은 담수상태의 환원조건에서 비소 (As), 철 (Fe) 등의 금속이온이 쉽게 용출되는 반면, 밭토양의 산화조건은 중금속인 카드뮴 (Cd), 납 (Pb) 등을 포함한 2가 금속이온의 용해도가 높아진다 (Jung et al., 2017). 이러한 중금속의 토양화학적 특성을 고려한 최적 개량제를 탐색 ‧ 발굴하기 위해 여러 토양 중금속 안정화제 적용 연구가 수행되었다. 특히, 논토양의 비소를 비롯한 납 등의 중금속을 동시에 안정화할 수 있는 효과적인 무기개량제로 석회와 철 산화물 등이 보고되었다 (Hartley et al., 2004; Oh et al., 2012; Kim et al., 2019; Li et al., 2022). 철 산화물은 토양 내 비소와 반응하여 FeAsO4 ‧ H2O, FeAsO4 ‧ 2H2O, Fe3(AsO4)2 등의 불용화물을 생성하고, 칼슘은 Ca-As-O 형태의 침전물을 형성함으로써, 토양 내 비소의 이동성을 둔화시킨다. 또한, 논토양의 담수는 토양미생물의 매개에 의해 납 (Pb)과 황산염 (SO42-)을 황화납 (PbS)화합물로 환원시킴으로써 불용화되고, 납을 비롯한 중금속은 탄산염 (CO32-)과 결합하여 중금속-탄산염 화합물을 형성하여 침전됨으로써 토양 내 이동이 제한된다 (Yokoyama et al., 2012; Koh et al., 2015; Xu et al., 2019).
본 연구는 비소-납 복합오염 논토양에 대한 Fe 또는 Ca 화합물 적용에 따른 중금속의 용해도 및 벼의 중금속 축적에 미치는 영향을 평가하고, 중금속-토양입자 간의 결합력 및 작물생육 특성을 고려한 최적 침출법 선발을 위해 수행되었다.
Materials and Methods
토양시료, 안정화제 및 시험식물
본 연구는 광산 주변에 위치한 비소와 납으로 오염된 논토양을 사용하였다. 토양오염공정시험기준법 (NIER, 2022)에 준하여 풍건한 토양의 중금속 오염도를 분석한 결과, 비소 (As)와 납 (Pb)의 토양 내 함량은 각각 31.5 mg kg-1, 362 mg kg-1으로 우려기준을 초과하였다 (Table 1). 토양의 토성과 화학성은 농업과학기술 연구조사분석기준 (RDA, 2012)에 준하여 분석되었다. 본 토양은 미사질양토 (silt loam)로 점토함량이 19.8%를 차지하였고, 유효인산을 제외한 pH, 유기물 등 나머지 항목은 논토양 적정기준에 적합하였다 (Table 2). 시험토양을 직경 2 mm 체로 거른 후 건토 3 kg과 안정화제 30 또는 60 g (토양 무게의 1 또는 2%)을 혼합처리하였다. FeSO4, CaSO4, CaCO3을 안정화제로 사용하였으며 (Kim et al., 2019; Moore et al., 2000), 안정화제 전체 무게가 시험토양 무게의 3%를 초과하지 않도록 혼합하였다. 대조구는 시험토양이며, 처리구는 단일 (FeSO4, CaSO4) 또는 2개의 안정화제 (CaCO3 + CaSO4 (1:1), FeSO4 + CaCO3 (1:1), FeSO4 + CaCO3 (2:1), FeSO4 + CaSO4 (1:1))를 시험토양과 혼합하여 사용하였다. 각 처리는 1/5,000 a 와그너 포트 (0.02 m2 표면적)를 이용하여 온실조건에서 수행되었으며, 처리 후 60일 안정화 후, 국립농업과학원 작물별 비료사용처방기준에 의거하여 질소, 인산 및 칼리질 비료를 각각 110, 45, 그리고 57 kg ha-1으로 토양에 혼화처리하였다. 본 연구의 재배실험은 완전임의배치 3반복으로 수행되었다. 시험식물인 신동진벼 종자를 2 mL L-1 농업용 살균제 (8% ipconazole) 용액에서 48시간 동안 표면 살균한 후, 수돗물을 이용하여 종자를 세척하였다. 소독된 종자를 30°C에서 48시간 동안 침종 및 발아시킨 다음, 수도용 상토로 충진된 규격육묘상 (60 cm × 30 cm × 3 cm tray)에 파종하였다. 균일하게 생장시킨 30일된 유묘를 각 처리구별 와그너 포트에 1주씩 이앙하였고, 온실조건에서 자연광과 상시 담수상태 (3 - 4 cm 담수심)로 출수기 전까지 재배실험을 수행하였다.
Table 1.
Concentration of heavy metals of the paddy soil used in this study.
|
As (mg kg-1) |
Cd (mg kg-1) |
Pb (mg kg-1) |
Cu (mg kg-1) |
Zn (mg kg-1) |
Ni (mg kg-1) | |
| Heavy metal concentration | 31.5 | 1.04 | 362 | 35 | 176 | 15 |
| Warning criteria† | 25 | 4 | 200 | 150 | 300 | 100 |
Table 2.
Physicochemical properties of the paddy soil used in this study.
|
pH
(1:5) |
OM† (g kg-1) |
Av. P2O5 (mg kg-1) |
Av. SiO2 (mg kg-1) | Exch. cations (cmolc kg-1) | Size distribution of soil particles (%) | ||||
| K | Ca | Mg | Sand | Silt | Clay | ||||
| 5.9 | 23 | 57 | 183 | 0.8 | 6.1 | 1.6 | 28.2 | 52.0 | 19.8 |
토양 내 pH 변화 및 중금속 유효태함량 분석
벼 재배기간 중 토양 pH는 담수상태에서 전극을 꽂아 이앙 후 6주 및 12주에 측정하였다.
토양 내 중금속 (비소 및 납)의 안정화 효율성과 식물로의 중금속 흡수 ‧ 이행성을 평가하기 위하여, 단일추출법으로 Mehlich3 (Mehlich, 1984) 및 1.0 M NH4NO3 침출법 (DIN, 1995)을 사용하였다. 벼 이앙 후 6주, 12주에 각 처리별로 원통형 오거를 이용하여 수직으로 15 cm 깊이 전체 토양을 약 200 g 채취하여 풍건한 후, 2 mm 표준체로 거른 토양시료를 분석에 이용하였다. 토양 중 비소 및 납의 침출 방법별 유효태함량 비교 ‧ 분석을 위하여, Mehlich3 침출법은 토양시료를 침출용액 (0.2 M CH3COOH, 0.25 M NH4NO3, 0.015 M NH4F, 0.013 M HNO3, 0.001 M EDTA)으로 추출하여 0.45 µm syringe filter로 여과하였다. 여과액을 유도결합프라즈마 원자방출분광기 (ICP-AES, AU/CINTRA 6, GBC Scientific, Australia)로 비소와 납을 측정하였다. 1.0 M NH4NO3 침출법은 토양시료를 1.0 M NH4NO3 침출용액으로 추출하여 0.45 µm syringe filter로 여과한 다음, 유도결합플라즈마 질량분석기 (ICP-MS, Agilent 7900, Agilent Technologies Inc., Santa Clara, CA, USA)로 비소 및 납을 분석하였다.
벼 생장반응 및 식물체 내 중금속 전함량 분석
비소 및 납으로 오염된 논토양에 대한 안정화제 처리에 따른 벼 생장반응을 분석하기 위해, 이앙 후 60일에 지상부 건물중을 조사하였다.
식물체의 비소 및 납 함량 분석을 위하여, 이앙 후 12주 (출수기 전)에 지상부만을 채취하여 잎집 (leaf sheath)과 잎몸 (leaf blade)으로 분리한 후, 세척, 건조 및 분쇄하여 분석시료로 사용하였다. 잎집 및 잎몸 시료의 분해는 Graphite Block Acid Digestion System (ODLAB Co., Ltd., Seoul, Korea)을 이용하였고, 각 분석시료 500 mg에 10 mL 질산 (conc. HNO3)을 넣고 산분해하였다. 여과지 (No. 40, Whatman, Buckinghamshire, UK)를 이용하여 분해액의 불순물을 제거한 후, 유도결합플라즈마 질량분석기 (ICP-MS, Agilent 7900, Agilent Technologies Inc., Santa Clara, CA, USA)에서 비소 및 납 함량을 측정하였다.
데이터 분석과 통계처리
모든 데이터 통계 처리는 Statistical Analysis Software (SASS ver. 9.2; SAS Institute Inc., Cary, NC, USA) 프로그램을 이용하여 처리 간 분산분석 (ANOVA)과 상관분석을 실시하였고, 통계적 유의성은 Fisher 최소유의차 검정 (p < 0.05)을 통하여 판단하였다.
Results and Discussion
안정화제 처리에 따른 토양 내 pH 및 중금속 유효태함량 변화
토양 내 pH 변화에 있어, 이앙 후 6주에는 단독 및 복합 안정화제 처리구 모두에서 무처리에 비해 유의적으로 감소하였다 (Fig. 1A). 그러나, 이앙 후 12주에는 단독처리구 및 FeSO4 + CaSO4 (1:1) 처리구만 감소하였고, 나머지 복합처리구들은 유의적으로 증가함을 확인할 수 있었다 (Fig. 1B). FeSO4 + CaSO4 (1:1) 처리는 토양에서 황산염의 생성으로 인한 pH의 감소라고 판단한다 (Fernandes et al., 2011). 또한, 본 연구결과와 유사하게 Simón et al. (2005)과 Moreno-Jiménez et al. (2012)은 토양에 CaCO3를 적용하면 토양의 pH가 증가한다는 결과를 보고하였다.
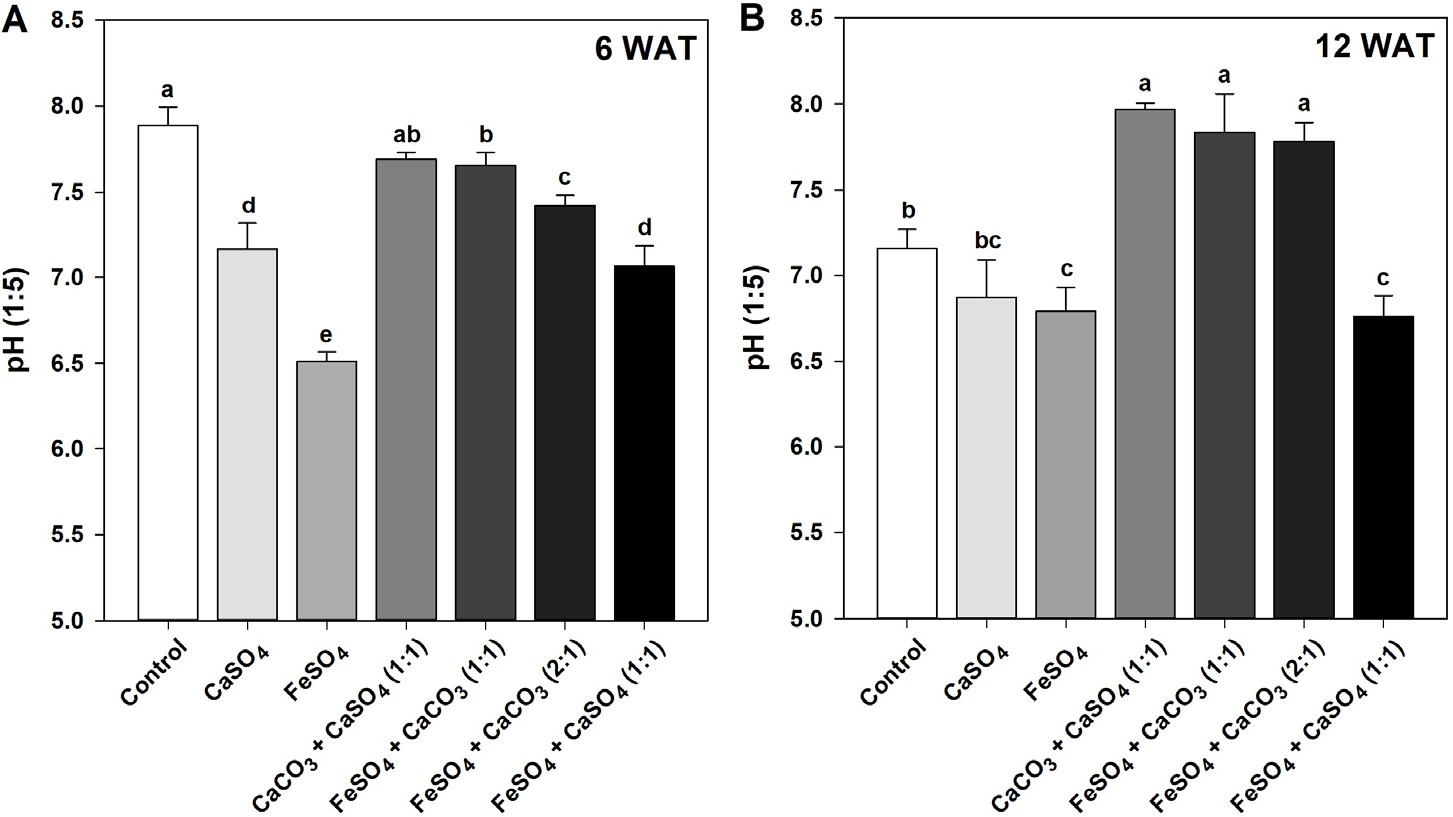
Fig. 1.
Changes in pH of the soil as affected by CaSO4, FeSO4, CaCO3 + CaSO4 (1:1), FeSO4 + CaCO3 (1:1), FeSO4 + CaCO3 (2:1), and FeSO4 + CaSO4 (1:1), treated before transplanting rice seedlings. The pH changes in soil solution were recorded at 6 and 12 weeks after transplant (WAT) of rice seedlings, respectively. Vertical bars represent standard deviations of the mean. Means denoted by the same letter are not significantly different at the p < 0.05 level according to Fisher’s least significant difference (LSD) test.
비소-납 복합오염 논토양에 안정화제를 적용하고, 벼 이앙한 후 6주 및 12주 모두에서 2가지 침출법 (1.0 M NH4NO3 및 Mehlich3)을 이용한 비소와 납의 유효태함량은 안정화제 무처리구와 처리구 간에 유의적인 차이를 나타냈다 (Figs. 2 and 3). 단독 안정화제 처리구 중 FeSO4 적용한 토양의 비소 유효태함량이 가장 낮게 검출되었을 뿐만 아니라, 무처리에 비해 복합 안정화제 처리구에서도 FeSO4를 포함한 처리에서 유의적으로 감소하는 경향을 나타냈다 (Figs. 2A, B and 3A, B). CaSO4 단독처리구 또한 토양의 비소 유효태함량이 무처리에 비해 유의적으로 줄어듦을 확인할 수 있었다 (Figs. 2A, B and 3A, B). 이는 FeSO4 및 CaSO4에 공통으로 존재하는 SO42-가 논토양의 환원상태에서 비소와 결합하여 As-S 결합형태 (AsS, As2S3)의 불용성 화합물 생성을 증가시킴으로써, 유효태 비소함량이 낮게 침출되는 것으로 판단된다 (Burton et al., 2014; Hashimoto and Kanke, 2018). 또한, 두 화합물 모두에 SO42-를 가지고 있음에도 불구하고 FeSO4의 안정화 효과가 CaSO4 보다 높게 나타난 이유는 논토양의 환경특성인 환원조건으로 인한 5가 비소 (As5+)에 비해 3가 비소 (As3+)가 월등히 많이 존재함으로써, Fe를 교환하여 불용화하는 것이 Ca 교환 불용화보다 반응성이 더 강하기 때문으로 판단된다 (Eary, 1992; O’Day et al., 2004; Rickard and Luther III, 2006; Burton et al., 2013, 2014; Xu et al., 2019).
비소의 경우, 안정화제 처리 후 6주에서 12주로 갈수록 토양 내에서 비소-안정화제 결합에 의한 안정화가 증진되었던 반면 (Figs. 2A, B and 3A, B), 납의 경우 모든 안정화제 처리구에서 유효태함량이 6주보다 12주에서 유의적으로 높게 검출되었다 (Figs. 2C, D and 3C, D). 이러한 결과는 토양 내에서 납-안정화제 간의 안정화가 서서히 진행되기 때문으로 판단된다. Kim et al. (2018)은 토양 내에서 비소는 120주 그리고 납은 64주에 안정화되는 것으로 보고하였고, 이는 중금속 간에 상이한 안정화 지속성을 나타내는 것이다. 또한, 단독 FeSO4 처리구만이 대조구 또는 다른 안정화제 처리구에 비해 유의적으로 높은 유효태 납함량을 나타냈고, 나머지 단독 및 복합 안정화제처리구에서는 통계적인 차이가 없었다 (Figs. 2C, D and 3C, D). FeSO4 처리구의 황산염은 Pb이온과 반응하여 황산-납 화합물 (PbSO4)을 형성할 수 있다. 황산-납 화합물은 용해도가 낮고 식물체로의 이동이 쉽지 않지만 (Tandy et al., 2017), 토양의 pH가 낮을 경우에는 황산-납 화합물의 용해도를 증가시킴으로써, 토양용액에서의 납 이온 함량을 높일 수 있을 것이다 (Kicińska et al., 2022). 따라서, 철 성분을 함유한 FeSO4는 비소오염지 개량에는 효과적이지만 (Hartley et al., 2004), 납오염지 또는 납을 포함한 복합 중금속오염지에는 오히려 토양 내의 납 가용화를 촉진하기 때문에 적용을 지양해야 할 것으로 판단된다.
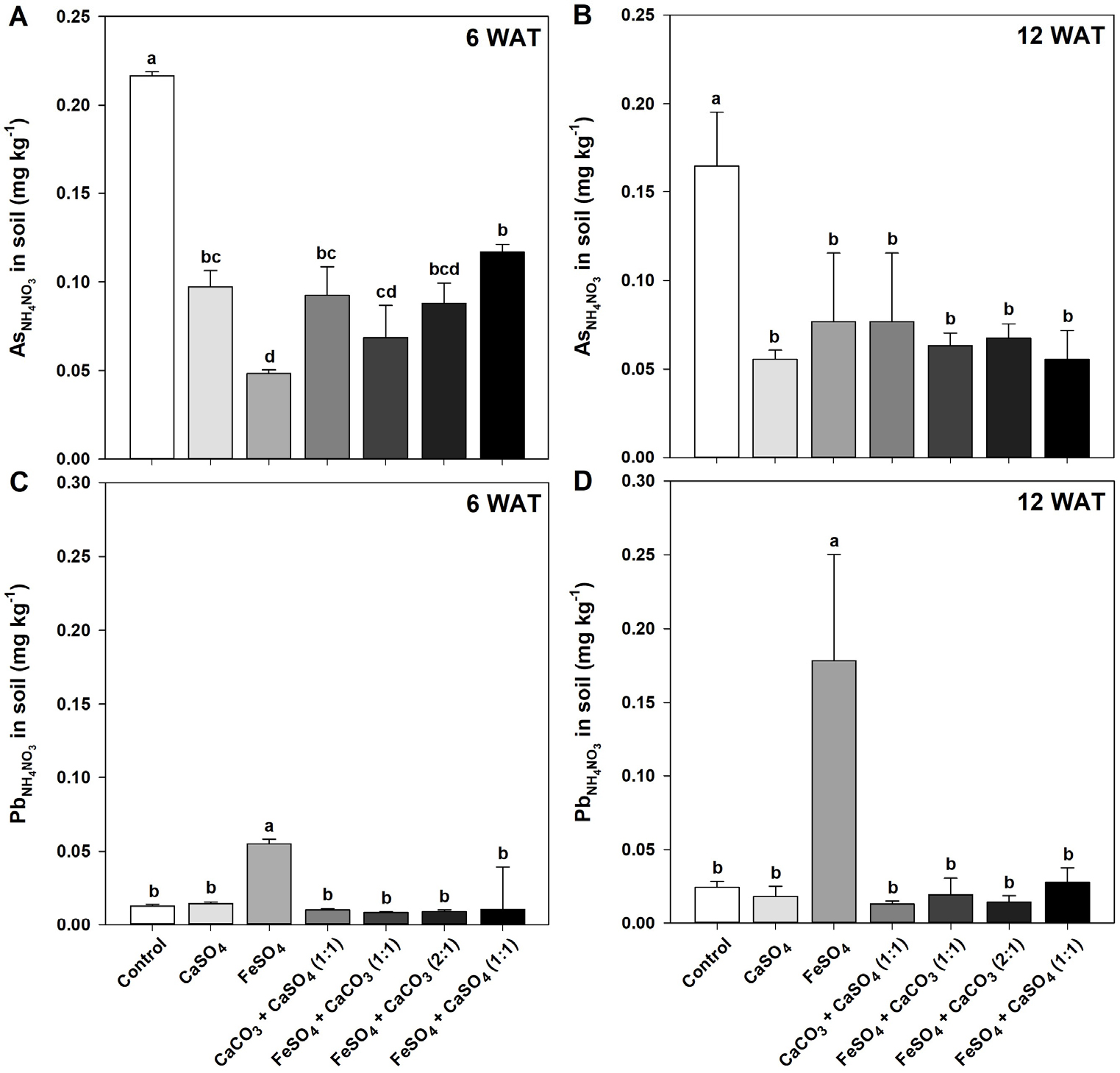
Fig. 2.
As (A and B) and Pb (C and D) concentration in the soils with the extracting solution of 1 M ammonium nitrate (NH4NO3) as affected by CaSO4, FeSO4, CaCO3 + CaSO4 (1:1), FeSO4 + CaCO3 (1:1), FeSO4 + CaCO3 (2:1), and FeSO4 + CaSO4 (1:1), treated before transplanting rice seedlings. The NH4NO3-extractable As and Pb concentration in soil were measured at 6 and 12 weeks after transplant (WAT) of rice seedlings, respectively. Vertical bars represent standard deviations of the mean. Means denoted by the same letter are not significantly different at the p < 0.05 level according to Fisher’s least significant difference (LSD) test.
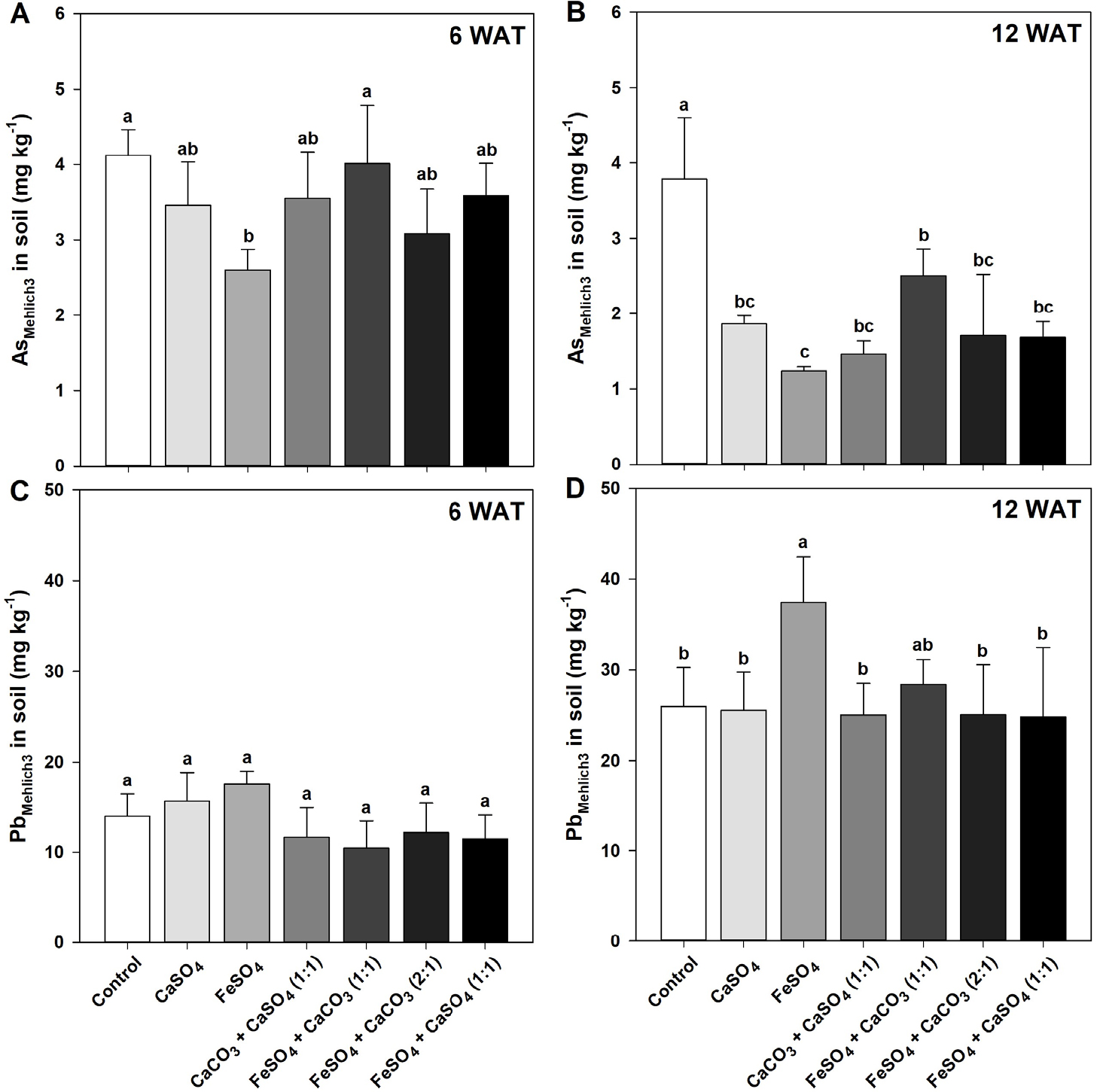
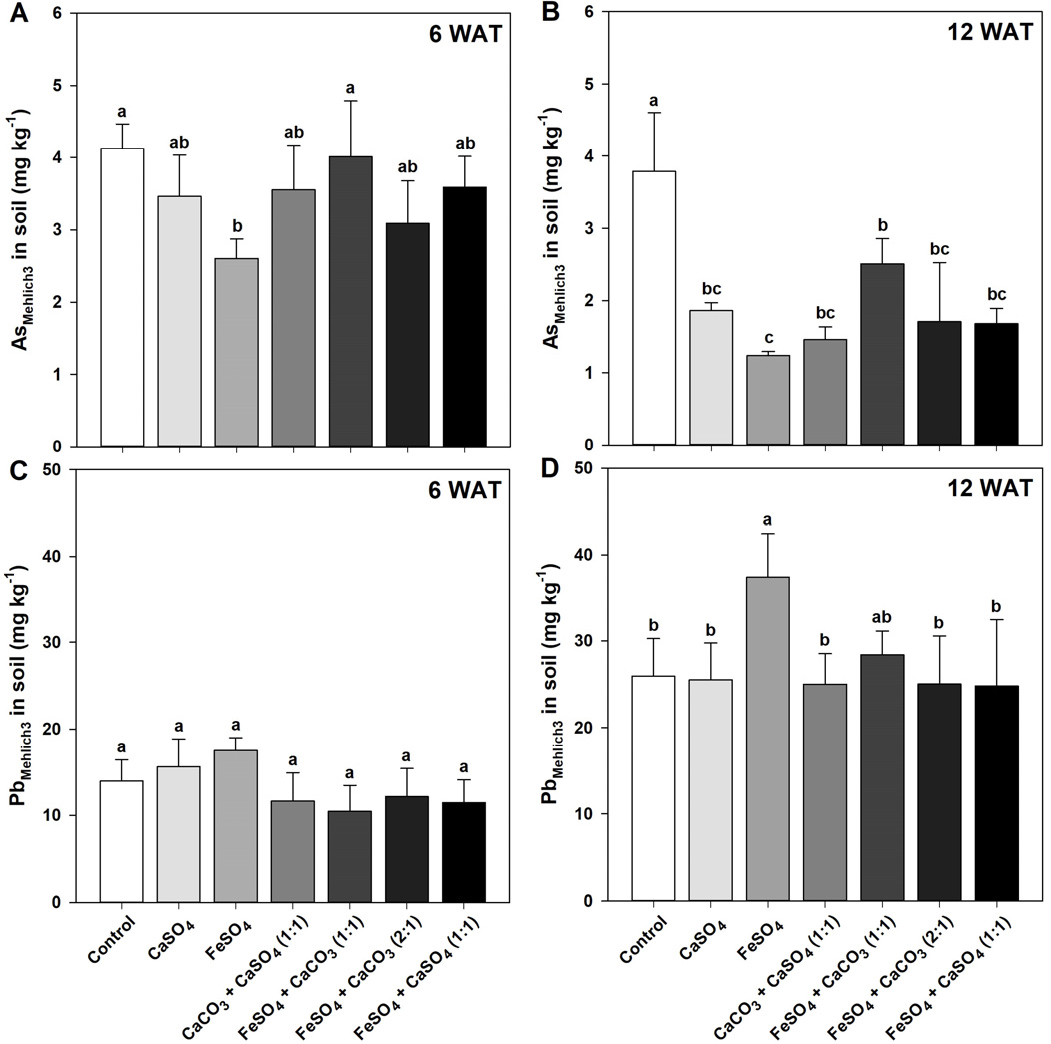
Fig. 3.
As (A and B) and Pb (C and D) concentration in the soils with the extracting solution of Mehlich3 as affected by CaSO4, FeSO4, CaCO3 + CaSO4 (1:1), FeSO4 + CaCO3 (1:1), FeSO4 + CaCO3 (2:1), and FeSO4 + CaSO4 (1:1), treated before transplanting rice seedlings. The Mehlich3-extractable As and Pb concentration in soil were measured at 6 and 12 weeks after transplant (WAT) of rice seedlings, respectively. Vertical bars represent standard deviations of the mean. Means denoted by the same letter are not significantly different at the p < 0.05 level according to Fisher’s least significant difference (LSD) test.
안정화제 처리별 벼 중금속 함량 및 생육 변화
벼 잎몸의 비소함량은 대조구 대비 단독 및 복합 안정화제 처리구 간에 유의적인 차이는 없었다 (Fig. 4B). 그렇지만 토양으로부터 잎집으로의 비소전이는 모든 안정화제 처리구에서 감소하는 경향을 보였고, FeSO4 + CaSO4 (1:1) 복합처리구가 가장 낮은 비소함량을 나타냈다 (Fig. 4A). 토양 내 낮은 비소함량에도 불구하고, 벼 지상부의 비소함량이 높게 나타낸 이유는 벼 생육 차이에 기인한 것으로 판단된다 (Ray et al., 2022).
잎몸의 납함량은 무처리에 비해 모든 안정화제 처리구에서 오히려 증가하는 경향을 보였을 뿐만 아니라 CaSO4 단독 및 FeSO4 + CaSO4 (1:1) 복합처리구는 매우 높은 함량을 나타냈다 (Fig. 4D). 잎집의 납함량은 대조구에 비교하여 FeSO4 + CaSO4 (1:1) 복합처리구만이 유의적으로 증대됨을 확인할 수 있었다 (Fig. 4C). 이는 SO42-을 지닌 안정화제는 Pb-S 복합체를 형성하여 납의 불용화도를 증대시킬 것으로 기대하였지만, 동시에 토양 중 pH가 감소하는 영향이 더 크게 작용하였기 때문에 토양 내 납 용해도가 증가하였던 것으로 판단된다 (Fig. 1).
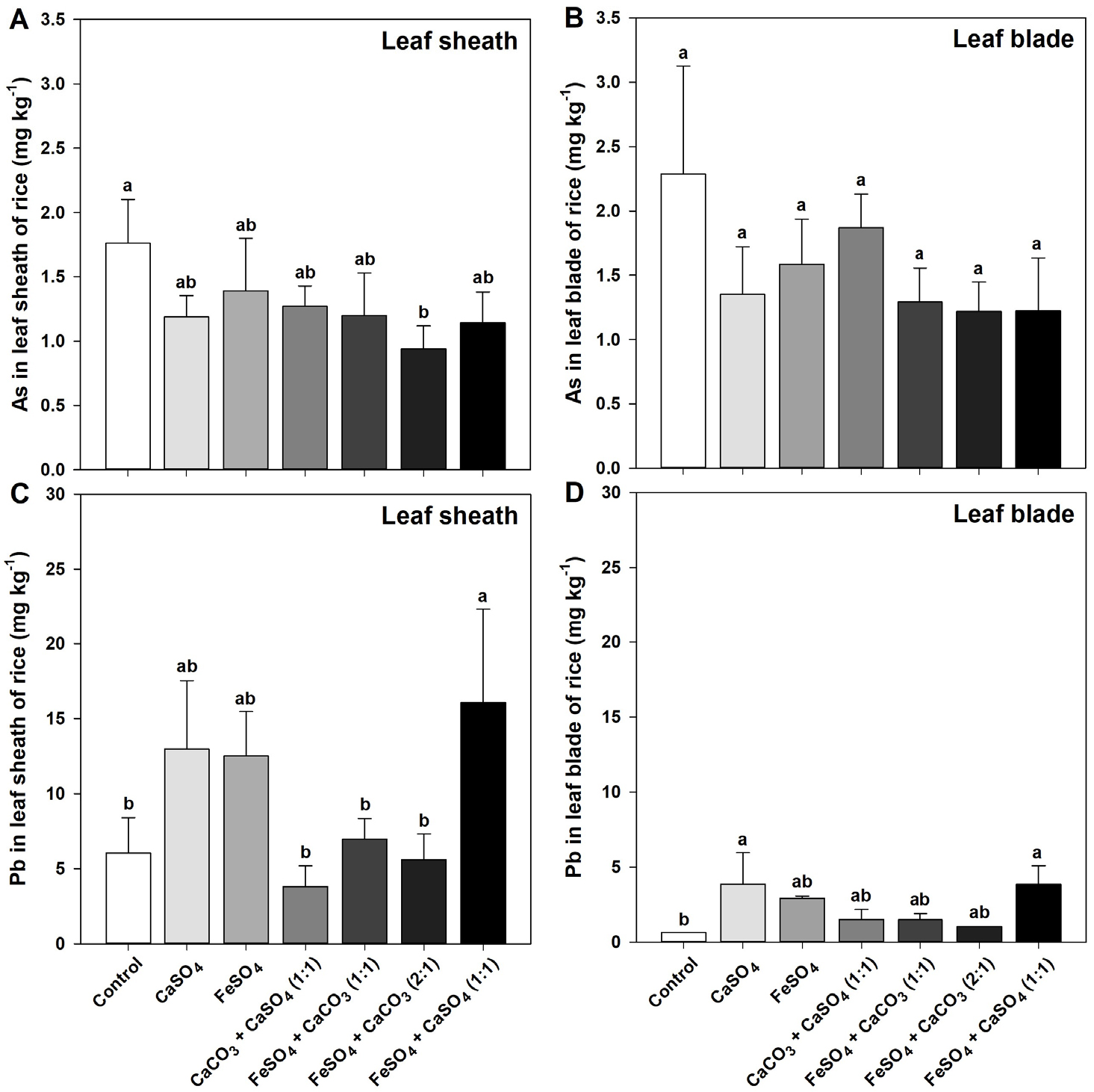
Fig. 4.
As (A and B) and Pb (C and D) concentration in the leaf sheath (A and C) and leaf blade (B and D) of rice plants at 12 weeks after transplant (before heading stage) as affected by CaSO4, FeSO4, CaCO3 + CaSO4 (1:1), FeSO4 + CaCO3 (1:1), FeSO4 + CaCO3 (2:1), and FeSO4 + CaSO4 (1:1), treated before transplanting rice seedlings. The As and Pb concentration in leaf sheath and leaf blade were measured at 12 weeks after transplant (WAT) of rice seedlings, respectively. Vertical bars represent standard deviations of the mean. Means denoted by the same letter are not significantly different at the p < 0.05 level according to Fisher’s least significant difference (LSD) test.
단독 및 복합 안정화제 처리에 따른 벼 지상부 건물중은 FeSO4 + CaCO3 (2:1) 복합처리구에서 무처리구에 비해 50% 이상 생육 감소를 나타냈지만, 다른 안정화제 처리구들은 유의적인 차이가 없었다 (Fig. 5). 비소와 납을 동시에 개량할 수 있는 안정화제 조합은 CaCO3 + CaSO4 (1:1), FeSO4 + CaCO3 (1:1), FeSO4 + CaCO3 (2:1)로 확인되었음에도 불구하고, 작물생육을 반영한 조합으로는 CaSO4 + CaCO3 (1:1), FeSO4 + CaCO3 (1:1) 복합처리 조합만이 비소 및 납 복합오염지 개량에 효과적일 것으로 판단된다. 따라서, 안정화제가 중금속뿐만 아니라 작물이 필요하는 양분들의 유효도에도 영향을 미칠 것임으로 (Kim et al., 2020), 이를 고려한 중금속오염지 개량을 위한 안정화제 선택이 필요할 것으로 판단된다.
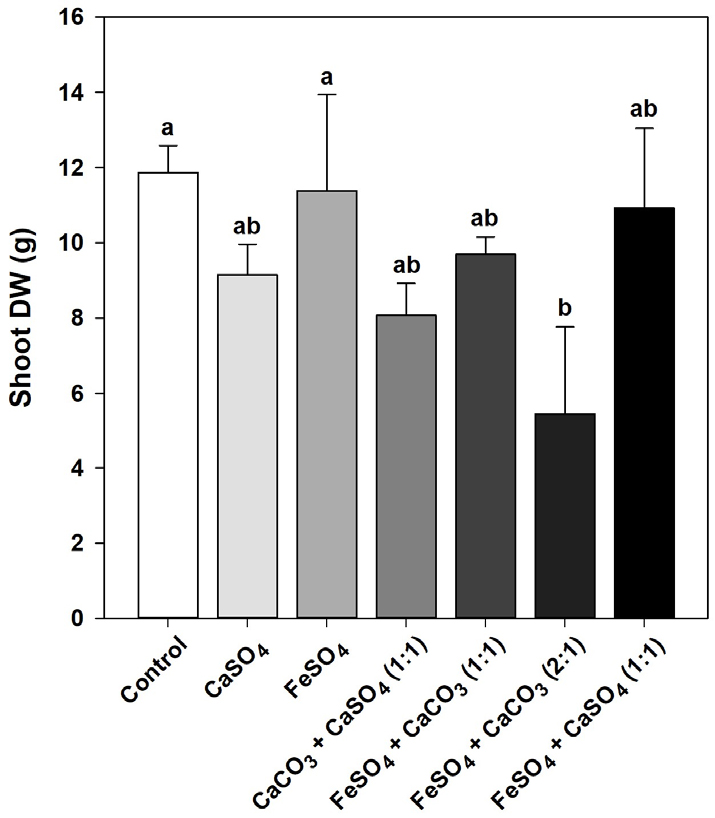
Fig. 5.
Shoot dry weight (DW) in rice plants as affected by CaSO4, FeSO4, CaCO3 + CaSO4 (1:1), FeSO4 + CaCO3 (1:1), FeSO4 + CaCO3 (2:1), and FeSO4 + CaSO4 (1:1), treated before transplanting rice seedlings. The shoot DW was measured at 60 days after transplant of rice seedlings. Vertical bars represent standard deviations of the mean. Means denoted by the same letter are not significantly different at the p < 0.05 level according to Fisher’s least significant difference (LSD) test.
토양 pH, 유효태 침출법 및 벼 중금속함량 간의 상관관계
토양 pH, 유효태 중금속 침출법 및 벼 비소 또는 납함량 간의 상관성을 비교 ‧ 분석하였다 (Tables 3 and 4). 비소는 토양 pH와 유효태 침출법 (1 M NH4NO3, Mehlich3) 간에 정 (+)의 상관성 (0.623, 0.439)을 보였던 반면 (Table 3), 납은 부 (-)의 상관성 (-0.668, -0.428)을 나타냈다 (Table 4). 또한, 토양 pH와 벼 비소함량 간에는 연관성이 없었지만, 납은 부 (-)의 상관성 (-0.590, -0.598)을 보였다 (Tables 3 and 4). 토양 유효태 중금속 침출법 (1 M NH4NO3, Mehlich3)과 벼 중금속함량 간의 상관성에 있어, 비소는 1 M NH4NO3, Mehlich3의 두 침출법 모두에서 상관관계 (0.541 - 0.620)가 존재하였지만 (Table 3), 납은 Mehlich3 침출법만이 상관성 (0.469 - 0.615)을 나타냈다 (Table 4). 중금속 측정 방법에 있어, 침출법에 따른 상관관계는 중요하다. Yoon et al. (2017)은 Mehlich3 침출법은 측정 분포 범위가 넓고, 다양한 성분을 한꺼번에 침출하여 분석하기 위해 개발된 복합 침출액이기 때문에 다른 침출액에 비해 식물과 유효태 중금속과의 관계를 설명하기 적합하다고 판단하였다. 따라서 토양 내 양분 및 중금속과의 높은 상관성을 나타내기 때문에 비소 및 납 복합오염지의 유효태 중금속 분석은 Mehlich3 침출법이 가장 적합할 것으로 판단된다 (Han et al., 2020).
Table 3.
Pearson’s correlation coefficient (r) among pH, Mehlich3 and ammonium nitrate extractable As concentration in soils and As concentration in the leaf sheath and leaf blade of rice plants.
| pH | AsMehlich3† | AsAmmonium nitrate‡ | AsLeaf sheath§ | AsLeaf blade¶ | |
| pH | 1 | ||||
| AsMehlich3 | 0.623** | 1 | |||
| AsAmmonium nitrate | 0.439* | 0.615** | 1 | ||
| AsLeaf sheath | 0.166 | 0.583** | 0.588** | 1 | |
| AsLeaf blade | 0.317 | 0.541** | 0.620** | 0.820** | 1 |
Table 4.
Pearson’s correlation coefficient (r) among pH, Mehlich3 and ammonium nitrate extractable Pb concentration in soils and Pb concentration in the leaf sheath and leaf blade of rice plants.
| pH | PbMehlich3† | PbAmmonium nitrate‡ | PbLeaf sheath§ | PbLeaf blade¶ | |
| pH | 1 | ||||
| PbMehlich3 | -0.668** | 1 | |||
| PbAmmonium nitrate | -0.428* | 0.137 | 1 | ||
| PbLeaf sheath | -0.590** | 0.469* | 0.288 | 1 | |
| PbLeaf blade | -0.598** | 0.615** | 0.199 | 0.914** | 1 |
Conclusions
본 연구는 비소 및 납 복합오염토양에서 안정화제 처리에 따른 토양 내 비소와 납의 유효태함량, 벼 중금속함량 및 생물체량을 비교함으로써, 토양 중 중금속 안정화와 벼의 생육에 미치는 영향을 평가하였다. 비소 및 납 복합오염지 개량을 위한 토양 안정화제로 FeSO4 단독처리와 FeSO4에 CaCO3를 혼용하여 사용 시, 토양 내 비소 유효태함량은 감소하였다. 이상의 의미있는 결과에도 불구하고 토양 안정화제 처리로 인한 벼 생육저해를 초래하였음으로 토양 안정화제 처리가 작물생육에 필수적으로 요구되는 양분의 유효도에 미치는 영향에 대한 후속연구가 필요할 것으로 판단된다.