Introduction
Materials and Methods
현장 재배시험
토양 특성 분석
토양 특성 분석
통계 분석
Results and Discussion
부산석고 시용에 따른 토양 이화학적 특성 변화
토양 pH 및 EC의 경시적 변화
수용성 칼슘과 황의 하층 이동
부산석고 처리가 작물 수량에 미치는 영향
부산석고 처리가 작물 품질에 미치는 영향
Conclusions
Introduction
석고 (gypsum)는 황산칼슘의 이수화물 (CaSO4 ‧ 2H2O)로 이루어진 석회질 광물로 비료생산 등 다양한 산업의 원료로 활용되고 있다. 석고는 생성원인에 따라 천연석고와 부산물 석고로 분류된다. 천연석고는 국내에서 전혀 생산이 되지 않아 대부분 수입되고 있다. 반면에 인산 제조와 황산화물 포집 등의 공정과정에서 발생되는 부산물 석고 (by-product)는 국내에서 매년 400만 톤 이상 생산되고 있으며 이 중 일부만 재활용되고 있다 (ME, 2010). 인산비료 제조시 발생되는 부산석고는 인광석 (Ca3(PO4)2)에 물 (H2O)과 황산 (H2SO4)을 첨가하여 반응시키는 습식공정 (wet process)을 통해 생성되는 부산물로서 인산석고 (phosphogypsum, PG)라 부른다: Ca5F(PO4)3 + 5H2SO4 + 10H2O → 3H3PO4 + 5CaSO4 ‧ 2H2O + HF. 지금까지 부산석고의 대부분은 슬러리 상태로 야적 (stacks; stockpiles)에 방치되고 있으며, 전 세계적으로 약 50여개의 대규모 야적장 (e.g., 미국 Florida, 스페인 Huelva)이 존재한다 (IAEA, 2008). 우리나라의 경우 남해화학 부지에 약 2천만 톤 (2009년 기준)이 적치되어 있으며, 매년 200 - 450만 톤의 부산석고가 지속적으로 발생 중이다.
부산석고는 농업, 건축, 도로건설 및 매립지 관리 등 다양한 산업분야에 재활용되고 있다. 특히, 부산석고에는 식물 영양 공급원인 칼슘, 인, 황 등이 포함되어 있어 비료로서의 농업적 활용가치가 있다 (Hentati et al., 2015; Saadaoui et al., 2017). 지난 수십 년간 해외에서는 다양한 연구를 통해 부산석고 시용에 따른 작물 생산량 증진 (Liu et al., 2010; Blum et al., 2013; Li et al., 2015), 산성토양 개선 및 알루미늄 독성 완화 (Carvalho and van Raij, 1997; Garrido et al., 2003) 및 염 토양 정화 (Tang et al., 2006; Nayak et al., 2013; Gharaibeh et al., 2014) 등의 긍정적 효과가 많이 보고 있다. 반면 국내에서는 주로 간척지 및 산성심토 개량을 위해 부산석고 활용 가능성에 대한 연구만 진행되어 왔지만, 2003년 이후부터 부산석고가 비료로서 인정을 받음으로써 현재까지 농가에 판매되고 있다 (Park, 2004). 하지만 부산석고 중 자연 방사성 물질 (e.g. 238U, 226Ra, 232Th) 및 중금속 (e.g. As, Ba, Cd, Cr, Cu, Ni, Pb, Se, Sr, Zn, V, Y, Zr)과 같은 유해성분이 검출되어, 농업적 재활용에 있어 안정성에 대한 우려가 있었다 (Tayibi et al., 2009; Saadaoui et al., 2017). 이러한 우려와는 달리 국내에서 발생한 부산석고에서는 아주 소량의 자연 방사성 물질과 중금속이 검출되어 (RDA, 2018), 비료 및 토양 개량제로서의 부산석고 활용에 문제가 없는 것으로 판단된다.
하지만, 국내에서는 부산석고 시비에 의한 농업토양의 질 및 작물 생산성 변화에 대한 과학적 연구결과 또는 근거 자료가 매우 부족한 실정이다. 만약 야적장에 방치되어 있는 수많은 양의 부산석고가 재활용된다면, 기업의 경제적 손실뿐만 아니라 주변 환경문제를 해결하고 더 나아가 우리나라 비료산업의 경쟁력을 향상시킬 것으로 판단된다. 따라서 다양한 연구를 통해 부산석고를 범용적 토양개량제로서 활용하기 위한 과학적인 근거를 마련하는 것이 시급하다고 사료된다. 본 연구에서는 부산석고 처리가 밭 토양 이화학성과 양파 생산성 및 품질에 미치는 영향을 알아보고, 부산석고의 적정 시비수준을 찾기 위해 수행하였다.
Materials and Methods
현장 재배시험
본 연구에서는 양파를 대상작물로 선정하였으며 이치방 품종을 재배하였다. 시험 포장지는 경남 산청군 도평면에 위치한 약 1,900 m2의 밭을 선정하였다. 정식 2주 전, 무기질 비료, 부산석고 및 패화석 (oyster shell, OS)을 토양에 처리한 후 로타리 작업을 수행하였다. 양파 묘는 20 cm × 12 cm 간격으로 2019년 11월 7일에 정식하였다. 이 후 7개월 동안 재배한 후, 2020년 6월 1일에 작물을 수확하였다.
부산석고 처리수준은 다음과 같이 총 네 가지로 구성하였다: PG0 (대조구), PG50, PG100 및 PG150. 부산석고 처리는 대상 농경지 토양의 칼슘 포화도 65%를 기준으로 하여, 이의 50% (PG50; 104 kg 10a-1), 100% (PG100; 208 kg 10a-1), 150% (PG150; 312 kg 10a-1)에 해당되는 양을 산출하여 수행하였다. 또 다른 석회질 비료로서 이용되고 있는 패화석 (OS) 처리구를 본 연구에 포함시켰으며, 200 kg 10a-1 수준으로 토양에 처리하였다. 모든 처리구 토양에 비료 3요소 (N-P-K = 8.4-37.9-8.0 kg 10a-1)를 균일하게 시비하였다. 무기질 비료 처리량은 시험포장 농경지 토양 특성 분석결과 값 (Table 1)을 흙토람의 비료사용처방 프로그램에 적용하여 산출하였다.
Table 1.
Physicochemical properties of soil in a field used in this study.
토양 특성 분석
토양 분석을 위해 각 처리구의 표토 (10 cm)를 부산석고 및 패화석 시용 전과 작물 수확 후 채취하여, 토양 중 pH, EC, 유기물 (OM), 유효인산 (Av. P2O5), 교환성 K, Ca, Mg 농도를 분석하였다. 경시적 토양 pH와 EC 농도의 변화를 조사하기 위해 인산석고 처리 후 8, 12, 16, 20, 24, 28주 차의 토양을 채취하여 분석하였다. 또한, 부산석고 시용에 의한 Ca 및 SO4의 깊이별 분포를 조사하기 위해 토양 단면 (soil profile)을 따라 10 cm 간격으로 70 cm 깊이까지 토양을 채취하여 두 이온의 농도를 분석하였다.
토양 이화학적 특성 분석은 풍건한 토양 시료를 이용하였다. 토양 pH와 EC (electrical conductivity)는 토양과 증류수를 1:5 비율로 진탕하여 각각 pH meter (Orion Star 2-Star, Thermo Scientific, USA)와 EC meter (Orion 3-Star, Thermo Scientific, USA)로 측정하였다. 토양 유기물은 Tyurin법 (Nelson and Sommers, 1996)으로 정량하였고, 유효인산은 Lancaster법 (NIAST, 2000)으로 침출하여 720 nm에서 UV/Vis 분광광도계 (Varian CARY 50 CONC, USA)이용하여 측정하였다. 양이온 교환용량 (cation exchange capacity, CEC) 및 교환성 양이온 (K, Ca, Mg)은 1N NH4OAc (pH 7.0) 용액으로 침출하여 (NIAST, 2000), 각각 Kjedahl (K-355, BÜCHI, Switzerland)과 ICP-OES (OPTIMA 5300DV, PerkinElmer, USA)으로 분석하였다. 수용성 Ca과 SO4은 증류수 (1:5 = w/v)로 침출하여 각각 ICP-OES (OPTIMA 5300DV, PerkinElmer, USA)와 IC (DIONEX AQUION, Thermo Scientific, USA) 으로 분석하였다.
토양 특성 분석
수확한 양파의 수량은 농촌진흥청 표준분석법에 준하여 구중을 생체중으로 측정하였다. 양파 중 영양분 함량을 분석하기 위해, 먼저 식물체 가식부를 분리하여 60°C에서 건조한 후, 분쇄하여 HNO3 습식분해 (wet digestion)를 하였다. 습식분해 된 용액을 이용하여 식물체 중 질소와 인산함량을 각각 Kjedahl법과 Vanadate법으로 분석하였다. 식물체 중 S, K, Ca, Mg 함량은 ICP-OES (OPTIMA 5300DV, PerkinElmer, USA)으로 분석하였다.
양파 가식부의 유리 아미노산 (free amino acids) 농도는 Yoon et al. (2017)의 방법에 따라 분석하였다. 시료 (0.1 g)를 100 mL의 3% sulfosalicylic acid에 넣고 1시간 동안 진탕한 후, 4°C 조건에서 3,500 rpm 속도로 1시간 동안 원심분리를 하였다. 이와 같은 추출과정을 세 번 반복한 후, 모든 추출액을 모아 0.45 µm syringe filter로 필터링하였다. 추출시료 10 µL를 inhydrin method에 따라 Ionex Ostion LCP5020 cation exchange column (22 × 0.37 cm)이 장착된 L-8900 high-speed amino acid analyzer (Hitachi High-Tech. Corp., Japan)에 주입하여 유기 아미노산을 정성 및 정량 분석하였다. 본 연구에서는 식물체내 아미노산 중 황 흡수와 밀접하게 관련된 cysteine과 methionine 농도를 분석하였고, 총 아미노산 함량은 34가지 아미노산 (phosphoserine, taurine, phosphoethanolamine, urea, proline, aspartic acid, serine, glutamic acid, sarcosine, α-aminoadipic acid, glycine, alanine, citrulline, α-aminobutyric acid, cystathionine, tyrosine, β-alanine, β-aminoisobutyric acid, γ-aminobutyric acid, 2-aminoethanol, hydroxyproline, ornithine, 1-methylhistidine, anserine, carnosine, arginine, threonine, valine, methionine, isoleucine, leucine, phenylalanine, lysine, histidine)을 합산하여 구하였다. Proline은 570 nm, 나머지 아미노산은 440 nm 파장에서는 측정하여 정량을 하였다.
통계 분석
본 연구의 분석자료는 Minitab16 (Minitab Inc., USA)을 이용하여 통계 분석하였다. 재배 전후 토양 이화학적 특성과 부산석고 시용에 따른 토양 및 식물체 특성의 유의적 차이를 평가하기 위해서 일원분산분석 (One-way ANOVA) 및 사후분석 (Fisher’s LSD)을 실시하였다.
Results and Discussion
부산석고 시용에 따른 토양 이화학적 특성 변화
재배 시험 전후 토양 이화학적 특성을 비교 분석해 본 결과에 따르면 (Table 2 cf. Table 1), 다양한 토양 인자에서 큰 차이를 보였다. 가장 큰 변화를 보인 토양 인자는 pH로 수확 전 7.0에서 6.2로 감소하였다. 또한 부산석고 처리 유무에 따른 처리구간 토양 pH의 차이가 보였지만 통계적인 유의성은 없었다 (p < 0.05). 모든 처리구에서 심토의 pH는 표토에 비해 높았으며, 대조구보다 부산석고 처리구의 pH가 더 낮았다. 부산석고 처리에 의한 토양 산성도 증가는 여러 연구에서 보고된 바 있다 (e.g. Lee et al., 2009; Al-Enazy et al., 2018). 그 원인은 부산석고에서 용해된 SO42-의 직접적인 영향뿐만 아니라 토양 입자에 흡착된 H+과 용해된 Ca2+간의 치환작용으로 의한 토양 용액 중 수소이온 활성 증가에 따른 것으로 사료된다 (Smaoui-Jardak et al., 2017). 양파의 재배 적정 토양 산도가 pH 6.3 - 7.3인 것을 감안할 때, 본 연구에서는 재배기간 동안 부산석고 공급에 의한 토양 산성화 피해는 없었던 것으로 판단된다.
토양 전기전도도 (EC)의 경우, 재배 전 0.14 dS m-1에서 재배 후 1.0 dS m-1 이상으로 모든 처리구에서 상당히 증가하였다 (p < 0.05). 특히, 표토 및 심토 모두 부산석고 처리 수준이 증가함에 따라 EC 값이 증가하였으며 (Table 2), PG150 처리구에서 EC의 최대값 (1.93 dS m-1)이 측정되었다. 이와 같은 부산석고 시용에 따른 토양 EC 증가는 강우-석고 반응 작용에 의해 토양 용액 중으로 유입된 부산석고의 구성성분 (Ca, SO4, F, Na, Cl etc.)과 연관된 것으로 사료된다 (Amor and Gueddari, 2016; Saadaoui et al., 2017). 본 연구와 유사하게도, Elloumi et al. (2015)의 연구결과에 따르면, 부산석고 2.5%와 5%를 처리한 해바라기 재배 토양의 EC 값은 재배 전 0.15 dS m-1에서 수확 후 각각 2.39 dS m-1와 2.53 dS m-1로 증가하였다.
전반적으로 재배 후 토양 중 유기물 함량과 유효인산 농도는 증가하였으며, 두 토양인자 모두 대조구 (PG0)와 OS 처리구에서 가장 높은 농도를 보였다 (Table 2). 이와 반대로, 교환성 Mg 농도는 재배 후 상당히 감소하였다 (p < 0.05).
교환성 Ca 농도의 경우, 재배 후 PG0, PG50 및 OS 처리구에서 농도가 감소한 반면, PG100과 PG150 처리구에서는 각각 5%와 10%씩 증가하였다. 이처럼 본 연구에서는 부산석고 처리 수준이 PG100 이상일 때 토양 중 칼슘 농도 증가 효과를 보여주었다. 양파 생장 단계에서 칼슘은 아주 중요한 영양소로서 칼슘 시비는 초기 생육 증진뿐만 아니라 구근 수량, 질 및 저장성 향상을 위해 매우 중요하다 (Batal et al., 1994; Ghoname et al., 2007). 게다가, 표토보다 심토에서의 더 높은 Ca 농도가 발견되었으며, 이것은 부산석고에서 유출된 Ca 이온이 토양 단면을 따라 수직적 이동에 의한 것으로 판단된다. 이러한 부산석고 시용 효과는 특히 산성토양 중 심토의 산성도를 개선하기 위해 널리 적용되고 있다 (Toma and Saigusa, 1997). Carvalho and van Raij (1997)과 Saadaoui et al. (2017)의 연구에 따르면, 부산석고 공급에 의해 산성토양의 Al 독성을 완화시킬 뿐만 아니라 뿌리성장 촉진 및 식물의 수분과 Ca 흡수를 향상시켰다.
Table 2.
Properties of top- and sub-soil in a field following onion cultivation.
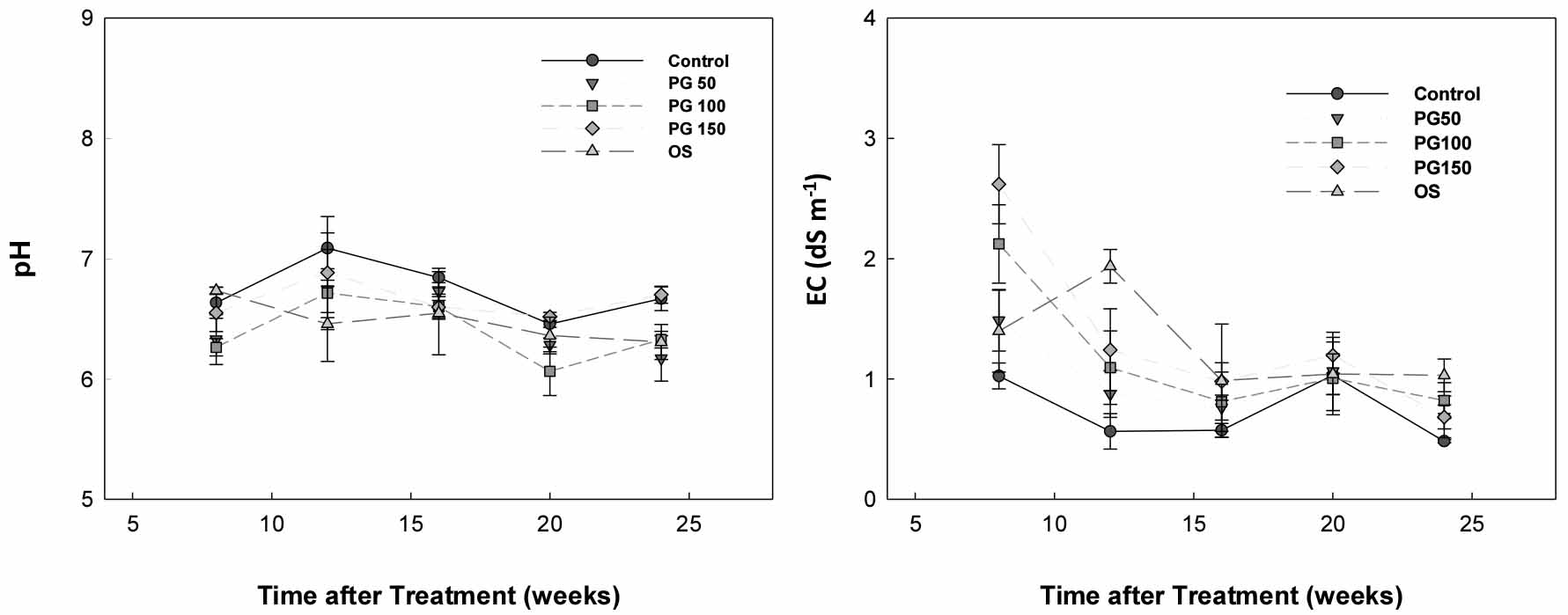
토양 pH 및 EC의 경시적 변화
부산석고 시용에 따른 양파 재배 기간 중 토양 pH의 변화는 패화석 처리구 (OS)를 제외한 모든 처리구에서 유사한 경향을 보였다 (Fig. 1). 패화석을 처리한 토양의 pH는 시간이 지남에 따라 점차 감소한 반면 부산석고를 처리한 토양 pH는 처리 후 감소하였다가 16주차 때 급격히 증가한 후 다시 점차 감소하였다. 이 시기에 인산석고 처리구에서의 pH 값 상승은 인산석고 시용 후 1, 2월에 증가된 강우에 의해 용해되어진 Ca 이온의 영향으로 사료된다. 토양 EC의 경우, 인산석고 시용 후 8주차 때 최대값을 보였으며 점차 감소하였다. 특히, PG150 처리구의 EC가 2.0 dS m-1 이상으로 밭토양 적정 값 이상이었다. 그러나 수확기 토양 EC 값은 1.0 dS m-1 이하로 감소하였다. 따라서 농경지에서의 부산석고 활용은 토양 염 조건에 따라 안정화 기간을 가지는 등 공급 시기 및 방법에 있어 조절이 필요할 것으로 판단된다.
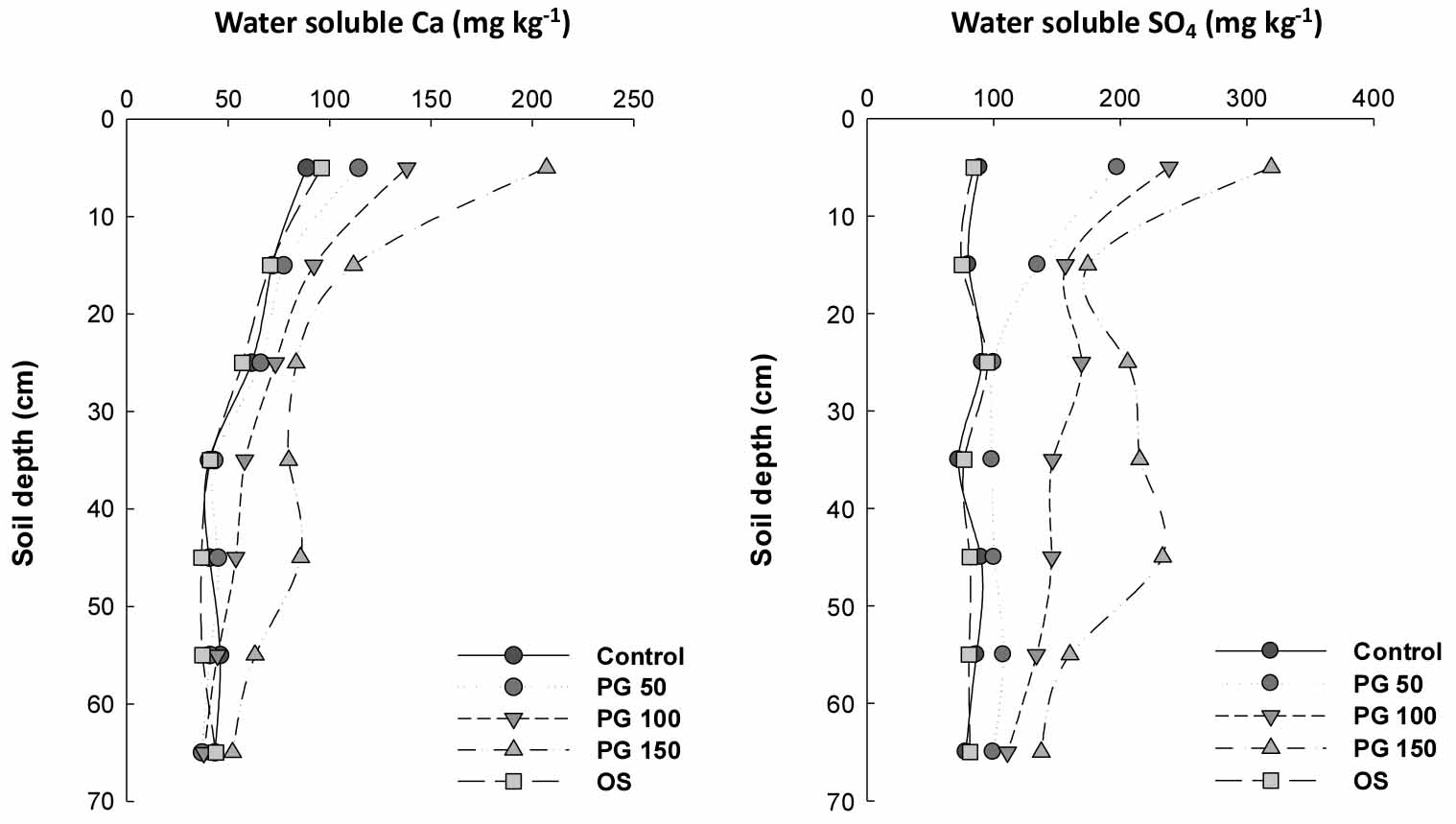
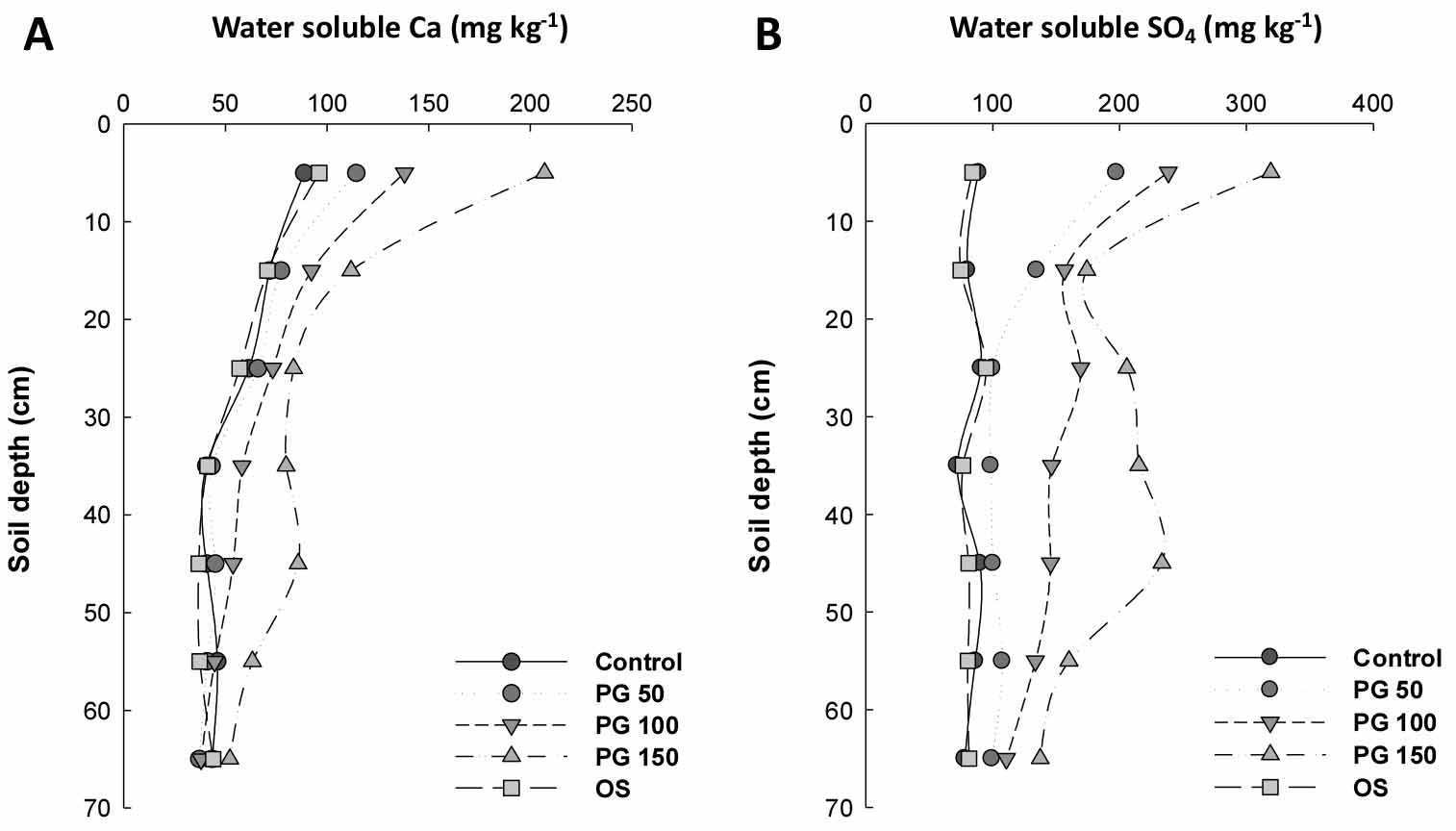
수용성 칼슘과 황의 하층 이동
전반적으로 토양 단면을 따라 깊이별 수용성 칼슘 농도는 차이가 있었다 (Fig. 2). 또한 부산석고 시용에 의해 수용성 칼슘 농도는 증가하였으며, 처리수준이 높을수록 그 증가율은 높았다. 반면 수용성 황 농도의 경우, 대조구와 OS처리구에서는 토양 단면에 따라 차이가 없었지만 수용성 칼슘농도와 동일하게 부산석고 처리 수준에 따라 차이를 보였다 (Fig. 2). 일반적으로 수용성 이온의 수직 이동은 이온의 용해도, 토성과 관련된 배수등급, 그리고 강우량에 큰 영향을 받는다. 본 연구결과에 따르면, 부산석고 시용에 의해 칼슘과 황이 약 70 cm 깊이까지 수직이동을 하였으며, 재배기간 동안 비닐 멀칭을 하였음에도 불구하고 상당히 높은 수직 이동율을 보여준다. 이와 같이 수용성 Ca과 SO4의 빠른 수직 이동율은 부산석고가 심토 개량에 한계가 있는 석회보다 심토를 개량할 목적으로 적극 활용될 수 있음을 시사한다 (Blum et al., 2013). 그러나 본 연구에서 이용된 또 다른 토양 개량제인 패화석 (OS)의 경우, 이러한 심토 개량 효과를 보이지 않았다.
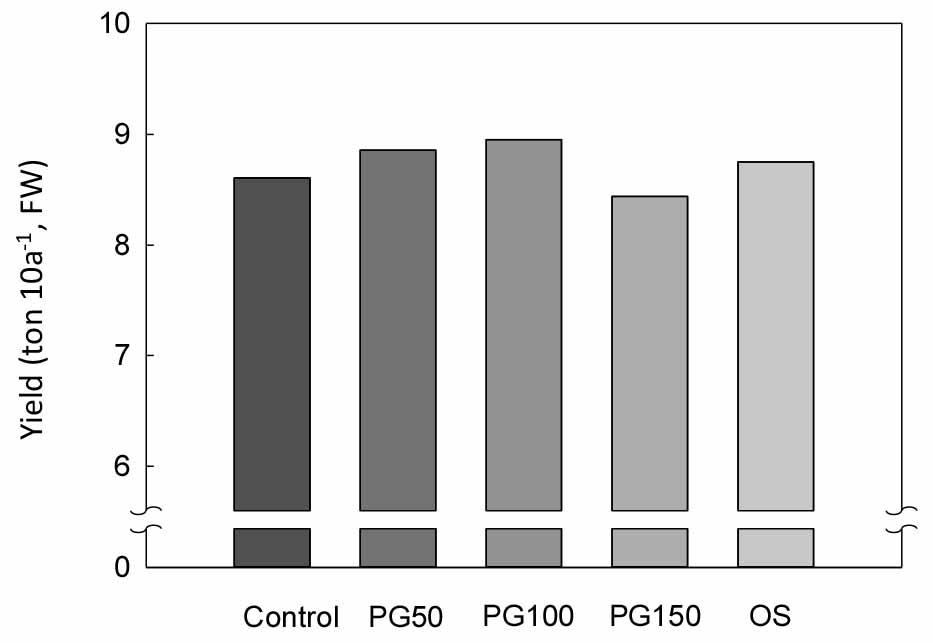
부산석고 처리가 작물 수량에 미치는 영향
부산석고 시용에 따른 양파 생산량은 Fig. 3과 같다. 본 시험지 토양의 석회 포화도는 약 61%로 석회가 크게 부족한 토양이 아니었다. 그리고 패화석 처리에 의한 양파의 수량 증수 효과는 없었다. 부산석고 처리구 (PG0, PG50, PG100)에서는 처리수준이 높을수록 양파수량이 증가되었지만, 최대 처리수준인 PG150에서는 오히려 수량이 감소하였다 (Fig. 3). 본 연구에서는 처리구간 통계적으로 유의적 차이는 없었다 (p < 0.05). Smaoui-Jardak et al. (2017)의 연구결과에 따르면, PG 처리농도가 0 - 10% 수준에서는 처리농도가 높을수록 토마토의 성장 및 생산량이 비례적으로 증가하였지만, 20% 이상의 PG 처리농도에서는 생육이 억제되고 생산량이 크게 감소되었다. 이는 고농도의 PG 처리가 토양 염 농도를 증가시키고 부산석고에 포함되어 있는 유해물질 (e.g. 중금속 등)의 토양 용액 중 용해도를 높임으로써 작물의 생육과 수량에 악영향을 미친 것으로 보인다 (Smaoui-Jardak et al., 2017). 본 연구에서도 특히 고농도의 부산석고 시용 후, 급격히 증가한 EC농도 (>2.5 dS m-1; Fig. 1B)로 인해 양파 초기생육 단계에서 염 피해가 발생하여 이후 수확 시 양파의 생산량에 악영향을 미친 것으로 판단된다.
2020년 기준으로 국내 양파 생산 단수는 7.9 ton 10a-1이며, 경남지역의 단수는 8.7 ton 10a-1 (KOSTAT, 2020)이다. 본 연구에서 석회 포화도 65%를 충족시킨 PG50과 PG100 처리구의 생산 수량은 8.8 ton 10a-1 이상으로 국내 및 경남지역 평균 단수 값보다 더 높았다. 따라서 양파 생산성 증진 측면에서 볼 때, 본 경작지 토양에서 가장 적절한 부산석고 시용량은 석회포화도 100%로 조절한 208 kg 10a-1 (PG100)인 것으로 사료된다.
부산석고 처리가 작물 품질에 미치는 영향
부산석고 시용에 따른 양파 가식부위의 양분함량은 Table 3에서 보는 바와 같다. 대조구와 비교하였을 때, PG50과 PG100 처리구에서는 양파의 질소 및 인 이용률이 증가한 반면, PG150 처리구에서는 감소하였다. 양파 중 칼륨과 황 함량은 부산석고 처리 수준이 증가함에 따라 증가하였다 (Table 3). 칼륨은 광합성 등 식물의 대사 작용과 병해충에 대한 저항성 발현에 있어서 중요한 역할을 한다 (El-Morsy et al., 2016). 양파의 경우, 칼륨 시비는 수량 증가와 결구의 색상 및 광택 등 품질 향상에 도움이 된다 (Shafeek et al., 2013; Behairy et al., 2015). 본 연구에서 부산석고에 의한 양파의 칼륨 이용률 증가는 보였지만, 토양 중 교환성 칼륨 농도에는 영향이 없었다. 또한 Smaoui-Jardak et al. (2017)은 고농도 부산석고 처리가 식물의 칼륨흡수를 억제한다고 보고하였지만, 본 연구의 PG150 처리구의 양파에서는 오히려 가장 높은 칼륨 함량이 나타났다.
Table 3.
Nutrient content in eatable part of onion treated with different amendments. Data indicate mean of three replicates. Same letters in each column represent no significant difference among treatments (LSD, p < 0.05).
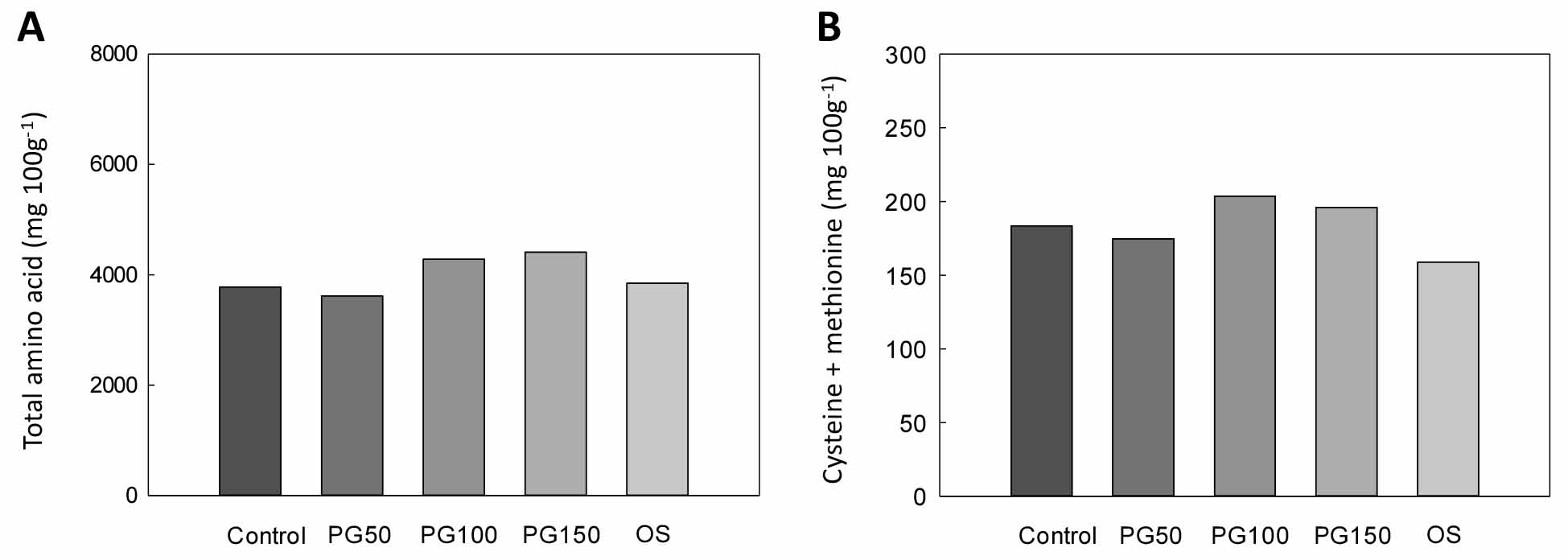
칼륨시비의 효과와 유사하게, 황 시비는 결구의 수량 및 병해충 저항성을 증가시킬 뿐만 아니라 양파의 맛을 향상시킨다 (Mishu et al., 2013; de Souza et al., 2015). 특히, 황은 식물체 내에서 시스테인과 메치오닌 아미노산의 구성 성분으로 이들 아미노산은 식물체 내의 필수 단백질 형성에 있어 중요한 역할을 한다 (Nayak et al., 2016). 최근 세계적으로 황 결핍에 대한 보고가 점점 증가하고 있으며, 농경지 토양 중 황 부족에 대한 황 시비의 중요성이 증가하고 있는 실정이다. 본 연구 결과에서는 부산석고 시용에 의한 식물체 내 황 함량 증가로 아미노산 합성이 증가되어 전 아미노산 함량이 높아진 것으로 나타났으며, 부산석고 처리수준이 높을수록 증가하는 경향을 보였다 (Fig. 4). 특히 황을 함유하고 있는 시스테인과 메치오닌 함량은 부산석고 처리수준이 208 kg 10a-1인 PG100처리구에서 가장 높았다 (Fig. 4). 따라서 부산석고는 작물생육에 있어서 중요한 황 공급원이 될 것이라 판단된다.
Conclusions
본 재배시험 연구결과를 통해 부산석고가 양파 재배에 있어서 토양 개량제 또는 비료로서 높은 잠재력이 있음을 확일 할 수 있었다. 특히, 부산석고 시용에 의해 증가된 토양 중 칼슘과 황 농도 그리고 양파의 양분 (N, P, S, K, Ca) 흡수율 및 식물 대사물질 (amino acids) 함량은 부산석고가 농업 토양의 질과 작물 품질 및 수량 향상에 큰 장점이 있음을 시사하였다. 하지만, 본 연구의 PG150 처리구처럼 높은 수준의 부산석고 공급은 오히려 토양 염류농도를 증가시키고, 작물의 수량 및 양분 이용율을 저하시켰다. 따라서 농업분야에서 부산석고를 효율적으로 재활용하기 위해서는 경작지 토양 및 대상 작물의 특성 등을 종합적으로 고려하여 최적의 부산석고 활용방안을 모색할 필요가 있다. 이를 위해, 앞으로 부산석고에 대한 장기적인 연구를 통해 통합적인 토양 개량효과를 지속적으로 평가함으로써 현장에서의 부산석고 활용가치를 극대화할 필요가 있다.