Introduction
농업유래 대기오염 연구의 주목적은 기후변화 대응과 축산업 유래 악취저감 등 오염적 측면에 있었으나, 최근 급격한 미세먼지 발생의 증가는 국민 건강을 위협하고 있는 수준에 이르렀으므로, 농업분야에서의 미세먼지 발생원인과 배경농도 파악이 국가적 관리차원에서 필요하다. 석탄・석유 등 화석연료가 연소되는 과정에서 배출되는 황산화물 (SOx)은 대기 중의 수증기 (H2O) 및 암모니아 (NH3)와 반응하고, 자동차 배기가스의 질소산화물 (NOx)과 휘발성 유기화합물 (VOCs)은 대기 중의 H2O, 오존 (O3), NH3 등과 반응하여 황산암모늄 [(NH4)2SO4]과 질산암모늄 (NH4NO3) 등 2차 생성 초미세먼지 (PM2.5)를 만든다. 이렇게 농업에서 발생한 2차 생성 초미세먼지 원인물질인 NH3는 전체 NH3 배출량의 79.3%를 차지할 만큼 매우 높다고 보고된다 (National Air Pollutants Emission Service, 2020). 국내 대기정책지원시스템 (Clean Air Policy Support System, CAPSS)의 보고에 의하면, 2차 생성 PM2.5에 중요한 역할을 하는 NH3 배출정보는 아직까지 명확하게 알려지지 않은 상태이나, 총 PM2.5 농도변화에 직・간접적으로 많은 영향을 미치는 NH3의 주요 배출원은 경종 및 축산 등 농업부문이며, 국내 총 배출량의 약 78% (비료사용농경지 6.7%와 분뇨관리 71.1%)를 차지하고 있다고 하였다.
국내 경종분야 2차 생성 초미세먼지 원인물질은 NH3 기체이며, 부산물비료 및 무기질 비료 시비로 인해 증가한다고 보고된 바 있다 (Freney et al., 1983; Kirk and Nye, 1991; Nieder et al., 1996; David et al., 2009). 농산물 생산성 증진에 크게 기여하는 대표적 무기질 질소비료인 요소 [CO(NH2)2]가 농경지에 시비되면 다양한 화학적 반응을 거쳐 NH3가 휘산되는데, 그 반응 순서는 요소 가수분해 → 암모늄이온 (NH4+) 흡착과 NH4+의 NH3와 H+으로 해리 → 토양 액상의 NH3가 토양 기상으로 이동 → 토양 표면과 주변 대기에서 NH3 분압 차이에 따른 NH3 휘산 순이다. 즉, 토양 표면 (경계층)에서 토양 표면에 가까운 주변 대기로의 NH3 기체가 발생된다 (Rachhpal-Singh and Nye, 1986). 하지만, 농경지에서 발생하는 NH3 배출량은 식물캐노피를 통과하여 대기로 배출되는 NH3로 평가하는 것을 검토할 필요성이 있다 (Schjoerring, 1995; Pacholski, 2003). 따라서 첫 번째 접근법은 토양 표면에서 배출되는 NH3 휘산 (ammonia volatilization)을 평가하기 위해 사용되며, 후자의 접근법은 순 NH3 플럭스 (net ammonia fluxes)에 해당되며 대기로 배출되는 2차 생성 미세먼지 원인물질을 평가하기 위해 사용될 수 있다.
본 연구의 목적은 농경지에서 발생하는 2차 생성 미세먼지 원인물질 (NH3)과 배출량 산정을 2가지 접근법으로 도출하는 것이며, 1) 토양에서 발생하는 NH3 배출량은 토양 챔버법으로; 2) 토양에서 발생하는 NH3 기체가 식물캐노피를 통화하여 배출되는 NH3는 식물챔버법으로 산정하는데 있다. 이를 위하여 토양표면으로부터 배출되는 NH3 배출량과 식물 캐노피에서 배출되는 NH3 배출량과의 차이를 비교하고자 한다.
Materials and Methods
노지 고추 재배
고추 재배 실험은 경기도 안성시 미양면 내 일반 고추농가 포장에서 2019년에 수행하였다. 시험포장 토양의 토성은 사양토이며, 토양산도 (pH)는 중성 (pH 7.3)이고 치환성 양이온 (Exchangeable cations)은 9.5 cmolc kg-1으로 적정범위 수준이었으나, 유기물함량과 총 질소 함량은 0.83%와 0.08%으로 낮은 편이었다. 고추 품종은 ‘청양’이었으며, 재배기간은 5월 20일부터 9월 30일까지 133일이었다. 고추의 시험구 총 면적은 96 m2 (각 처리구 면적: 16 m2)이었으며, 고추의 재식거리는 100 cm × 35 cm (조간 × 주간)이었다. 각 시험구의 처리는 무비구 (None)와 시비구 (퇴비+NPK)였으며, 시비구의 질소원은 일반 농협에서 시판되고 있는 1등급 가축분퇴비 (N 0.85%)와 요소 (N 46%)였다. 시비구의 시비량은 퇴비 20톤 ha-1 (170 kg N ha-1)과 요소 190 kg N ha-1였다. 시험은 완전임의 3반복으로 수행하였다.
비료의 시비 방법은 퇴비+NPK 시비구에서 퇴비 (170 kg N ha-1)와 인산 (110 kg P2O5 ha-1)은 토양 표면에 전량 기비로 시비하였으며, 질소 (190 kg N ha-1)와 및 가리 (150 kg K2O ha-1)는 농촌진흥청 고추 표준재배법에 따라 분시하여 시비하였다. 1차, 2차 및 3차 추비 시 요소와 가리는 물에 용해하여 토양 5 cm 깊이에 주입하여 처리하였다.
암모니아 플럭스 측정
고추 재배기간 NH3 플럭스는 동적 챔버 (Dynamic Flow-through Chamber method) 방법을 사용하여 측정하였다 (Fig. 1). 챔버의 재질은 PVC 소재로 토양 챔버의 부피가 9.8L (∅ 25 cm × H 20 cm)이며, 식물 캐노피 챔버의 부피는 396 L (W 60 cm × L 60 cm × H 110 cm)였다. NH3 가스 포집을 위한 토양챔버는 조간 사이에 설치하였으며 식물챔버는 고추를 포함하여 설치하였다 (Fig. 1a). NH3 포집에 사용한 용액은 0.05N-H2SO4 (50 mL)였으며, 포집 시간은 토양 챔버의 경우 1시간 (09:30AM - 10:30AM)이였으며, 식물캐노피 챔버는 2시간 (09:00AM - 11:00AM)이었다. 유량은 각 챔버의 부피를 고려하여 챔버 내 기체를 완전히 포집 할 수 있도록 설정하였으며, 토양챔버가 1 L min-1이었고, 식물캐노피챔버가 4 L min-1였다 (Fig. 1b and 1c). 토양챔버와 식물캐노피챔버에서 NH3 기체 포집 시 외부 NH3 기체 유입을 방지하기 위하여 공기가 유입되는 곳에 여과장치 (syringe filter, 0.45 µm)를 부착하였다. NH3 기체는 질소질 비료 (퇴비와 요소) 시비 후 1 - 5일까지 매일 포집하고, 이후부터 7일 간격으로 고추 수확기까지 수행하였다. 0.05N-H2SO4 용액에 포집한 NH3는 비색법 (Nesslerization method)으로 측정하여 농도를 결정하였다. 일 배출된 NH3는 Eq. (1)과 같이 산정하였다 (Andreas et al., 2006).
여기서, 는 NH3 플럭스 (mg N m-2 h-1), V는 챔버 부피 (L), conc.는 NH3 농도 (volume-ppm), 는 온도에 따른 대기 중 NH3 밀도, 은 NH3에서 NH3-N 변환 계수, 는 면적 (m-2) 및 는 시간 변환 계수 (h-1)이다.
고추 재배기간 NH3 휘산이 측정되지 않은 값 (측정 지점과 지점 사이의 NH3 휘산량)은 직선보간법 (linear interpolation)으로 계산하였고, 누적 NH3 배출량은 일 계산된 값을 합하여 산정하였다. 질소 시비에 대한 NH3 휘산량 (%)은 시비구의 누적 NH3 휘산량에서 무비구의 NH3 휘산량의 차이를 질소 시비량으로 나누고 100을 곱하여 산정하였다.
통계 분석
처리 간 누적 NH3 배출량의 차이는 STAR V. 2.0.1프로그램을 사용하여 분산분석 후 95% 유의 수준에서 최소유의차검정 (LDS)으로 평가하였다.
Results and Discussion
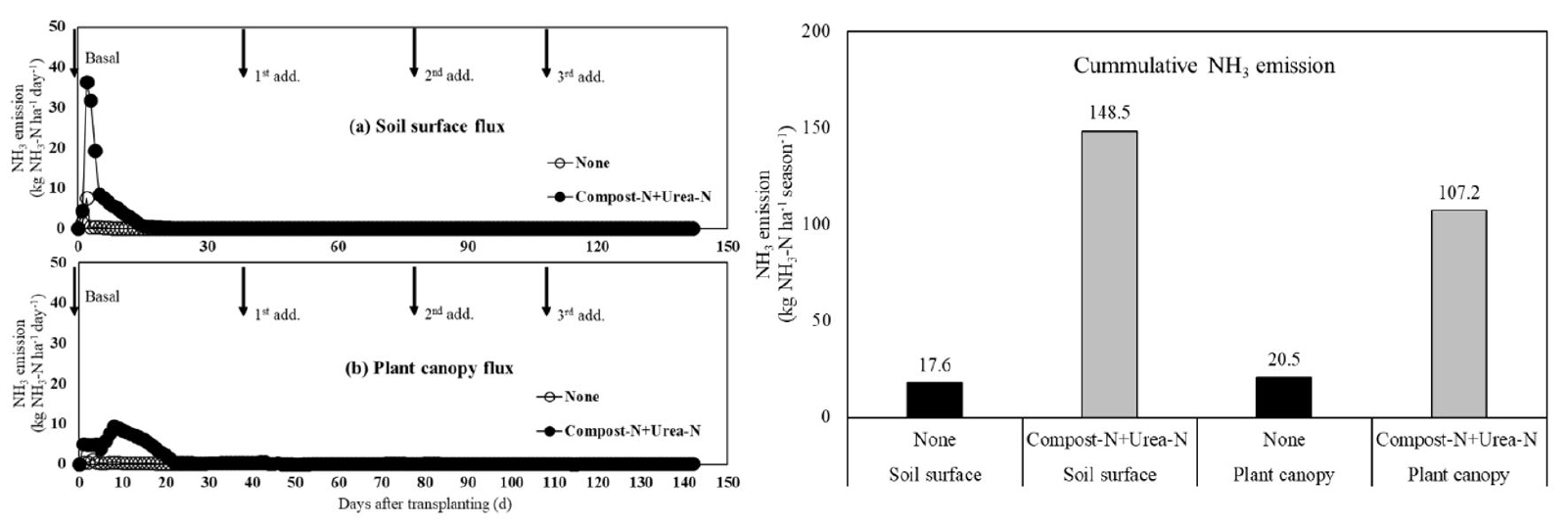
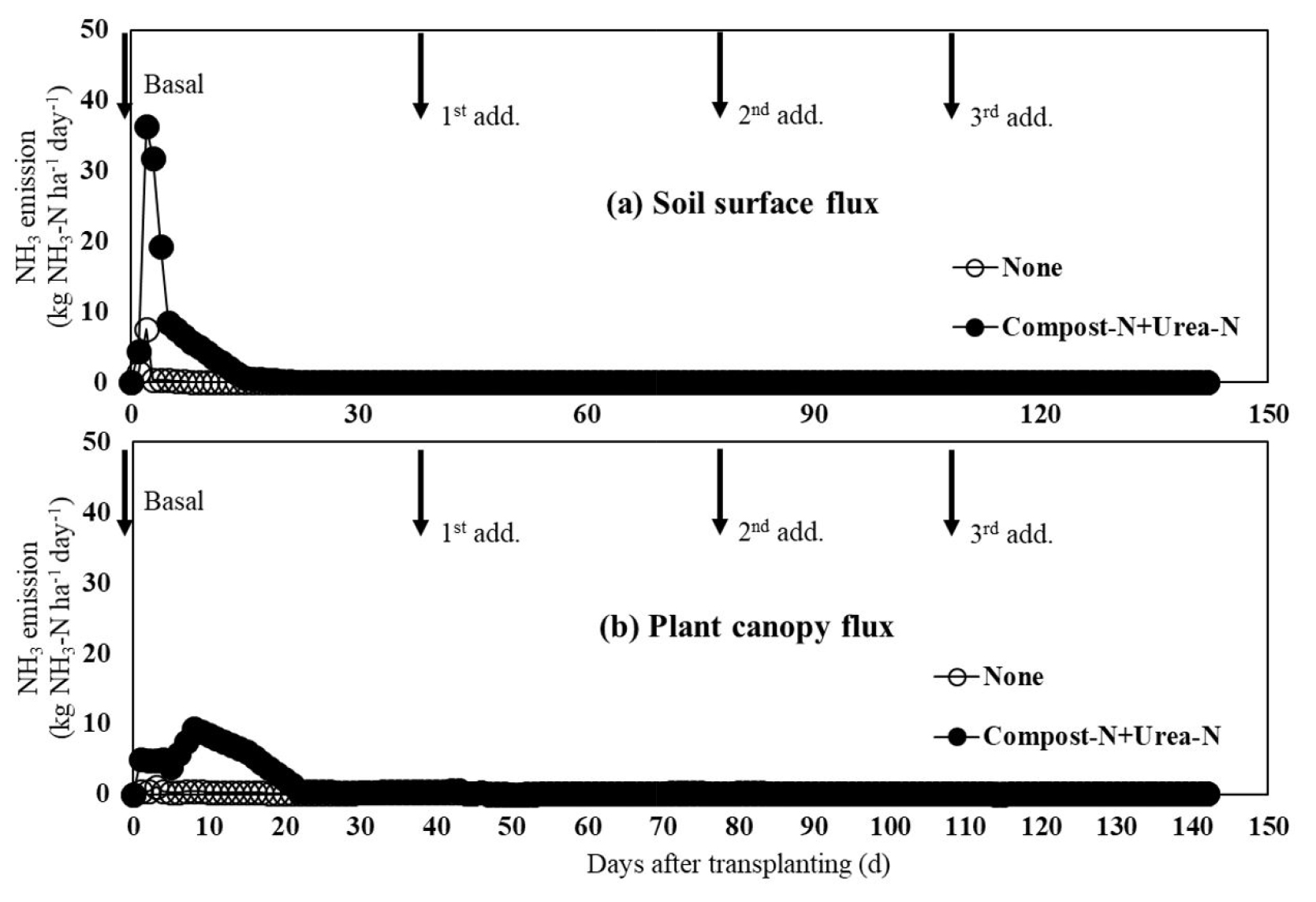
무비구 (None)와 퇴비+요소 시비구 (compost-N 170+urea-N 190)의 암모니아 (NH3) 휘산량은 기비 후 대부분 발생하였다 (Fig. 2). 토양 챔버에서 무비구와 시비구 (360 kg N ha-1)의 NH3 플럭스의 차이는 확연하게 나타났다. 무비구는 고추묘 이식 후 2일에서 NH3 기체가 최고점 (7.6 kg NH3-N ha-1 day-1)에 도달하였고, 시비구에서도 마찬가지로 이식 후 2일에서 NH3 기체가 최고점 (36.3 kg NH3-N ha-1 day-1)에 도달하였다. 무비구와 시비구의 NH3 휘산량은 이후부터 급격히 감소하다가 이식 후 4일과 16일부터 고추 수확기까지 미미하였다 (Fig. 2a). 식물캐노피챔버는 고추 재배기간 NH3 플럭스가 토양챔버와 다른 양상을 보였다 (Fig. 2b). 무비구에서 NH3 휘산이 이식 후 5일에 최고점 (0.6 kg NH3-N ha-1 day-1)을 보였으나, 이후부터 수확까지 미미하였다. 시비구에서는 이식 후 1일에 최고점 (8.4 kg NH3-N ha-1 day-1)을 보였고 이후 급격히 감소하다가 이식 후 5일부터 8일까지 다시 NH3 휘산이 증가하였다. 이후부터 점차 감소하다가 20일부터는 NH3 휘산이 미미하였다. 총 NH3 휘산량은 95%이상이 기비 후 20일까지 발생하였으나, 1차, 2차 및 3차 요소 추비 후 NH3 휘산량은 거의 없었다. 본 연구에서 요소의 분시비율은 기비 54% (103 kg N ha-1), 1차 추비 15% (28 kg N ha-1), 2차 추비 18% (32 kg N ha-1) 및 3차 추비 15% (28 kg N ha-1)이었다. 1차, 2차 및 3차 추비로 요소를 시비함에도 불구하고 NH3 휘산량은 전체의 5%미만이였다. 이러한 결과는 요소의 시비방법에 차이가 있는 것으로 판단된다. 본 시험에서 기비로 시비한 요소는 토양 표면에 직접 시비 후 고추묘를 이식하여 NH3 휘산량을 측정하였다. 반면에 1차, 2차 및 3차에 걸친 요소 추비는 분시비율에 따라 시비량을 주당 (per plant) 계산하여 물에 용해 후 토양 5cm 깊이에 주입하여 처리하였다. 이럴 경우, 요소의 가수분해 속도는 빨라지고 가수분해된 암모늄 이온 (NH3+)은 식물에 의해 바로 흡수될 수 있다. 한편, 고추의 생육 초기에는 무기태 질소 성분 (NH3+와 NO3-)이 토양에 상당히 많이 존재하여도 뿌리의 양분 흡수 능력이 높지 않아 다량 흡수하지 못한다. 식물이 흡수하지 못하는 토양 잔존 질소는 다양한 생지화학적 반응과정에서 NH3 휘산, NO3- 용탈 및 유거에 의해 대기 또는 수계로 유출된다. 그러나, 생육 중・후기 토양에 시비된 무기질 질소 비료는 고추의 양분 (NH4+와 NO3-) 요구량에 부합되어 NH3 형태로 휘산되는 양보다 식물에 의해 흡수되는 양이 상당히 높았을 것으로 판단되었다.
고추 재배기간 누적 NH3 휘산량은 무비구보다 시비구에서 높았고, 식물캐노피챔버보다 토양챔버에서 높았다(Table 1). 토양챔버에서 시비구의 NH3 휘산량은 148.5 kg NH3-N ha-1season-1였으며 총 시비량의 36.4%였다. 식물캐노피챔버에서 NH3 휘산량은 107.2 kg NH3-N ha-1 season-1으로 총 시비량의 24.1%였으며 토양챔버법보다 유의적으로 낮았다.
NH3 휘산은 작물 경작지에 질소 손실의 중요한 경로이다 (Yang et al., 2015; Yao et al., 2018). 본 연구는 토양챔버와 식물캐노피챔버법을 사용하여 토양표면 NH3 배출량과 식물캐노피 NH3 배출량을 평가하는 것이다. 토양 표면에서 발생하는 NH3 배출량은 식물캐노피에서 배출되는 양보다 현저하게 높게 나타났다 (Table 1). 이는 두 가지로 설명할 수 있다. 첫째, 작물을 포함하지 않고 측정한 토양챔버에서의 NH3 배출량은 작물을 포함하여 측정한 NH3 배출량보다 높은데, 이것은 고추의 뿌리가 충분히 옆으로 퍼지지 못하여 작물이 흡수한 무기태 질소보다 NH3 기체로 휘산되는 량이 상대적으로 높았을 것으로 생각된다. 관행 농법의 양분관리는 작물을 토양에 이식하기 전에 경작지 전 면적에 골고루 질소 비료를 시비한다. 즉, 고랑과 이랑 전 면적에 같은 양의 질소비료가 시비되면 고추가 심어져 있는 곳과 없는 곳에서 질소의 행방이 달라진다. 따라서 고추 사이에 시비된 질소비료가 NH3 배출량을 더 증가시켰던 것으로 판단된다. 반면에 식물캐노피 챔버에서 누적 NH3 배출량은 고추가 생장하는 동안 뿌리로부터 무기태 질소 (NH4+와 NO3-)를 흡수하여 바이오매스 및 수량을 상대적으로 증대시켜 NH3 배출량이 낮아진 것으로 판단된다. 둘째, 식물은 토양표면에서 배출된 NH3를 기공 또는 잎 표면을 통해 아포플라스트 (apoplast)로 확산된 다음 동화 작용을 거칠 수 있다. Hayashi et al. (2008)의 보고에 따르면, 작물 생육기간 동안 대기 중 NH3는 잎의 친수성 부분을 통하여 흡수하는 경향이 있다고 하였다. 이는 잎의 NH3 농도가 대기보다 낮으면 잎을 통해서 직접 NH3를 흡수하여 질소 동화가 가능하다는 것을 설명해준다. 공기 오염원 제거 측면에서 식물캐노피는 연간 20톤의 NH3를 흡수할 수 있다고 예측되었다 (Hutchinson et al., 1972). 그러나 오래된 잎은 NH3 농도가 높아서 NH3를 대기로 배출하는 경향도 있는 것으로 밝혀졌다 (David et al., 2009). 또한, 식물캐노피의 NH3 플럭스는 엽면적 지수 (LAI)와 밀접한 관련이 있으며, LAI가 클수록 토양에서 휘산된 NH3 기체를 더 많이 흡수한다는 결과도 보고되었다 (Katata et al., 2013).
Table 1.
Cummulative amounts of NH3 emission during red pepper cultivation in the treatments of no fertilization (none) and compost with urea fertilized field (compost-N+urea-N).
Conclusions
농경지에서 발생하는 2차 생성 초미세먼지 원인물질은 암모니아 (NH3) 기체이며, 부산물비료 및 무기질 비료 시비로 인해 증가한다. 본 연구의 목적은 고추 재배지에서 배출되는 NH3 기체를 토양표면과 식물캐노피에서 측정하여 보다 정확한 NH3 배출량 산정법을 제시하는데 있다. 실험 결과, 토양표면에서 직접 배출되는 NH3 기체는 총 질소 시비량의 36.4%였으며, 식물캐노피에서 배출되는 양은 24.1%로 토양표면 배출량보다 12.3% 낮게 산정되었다. 이러한 측정방법 간 차이는 작물이 뿌리로부터 또는 잎으로부터 흡수하는 암모늄 이온 (NH3+)과 NH3 기체를 간과했기 때문으로 판단된다. 기존 농경지에서 NH3 휘산량은 토양표면 배출량을 기준으로 산정되었다. 본 연구 결과에서 제언하는 것은 토양과 작물 및 미기상을 고려한 NH3 휘산량 측정법이 가능하다는 것이며, 보다 더 정밀하고 정확한 NH3 휘산량 산정을 위해서 다양한 측정 방법이 개발되어 배출량 산정방법이 개선되길 기대한다.