Ⓒ The Korean Society of Soil Science and Fertilizer.
ABSTRACT
Introduction
Materials and Methods
Results and Discussion
Conclusion
Introduction
질소는 작물 재배에 필수적인 요소로서 무기질 비료, 가축분뇨, 풋거름 작물 등 다양한 형태로 농경지에 시용되고 있다. 그중 요소(urea)는 전 세계적으로 가장 많이 시용되는 무기질 질소 비료이다(Heffer and Prud’homme, 2011). 토양에 시용된 요소는 요소 가수분해 효소(urease)에 의해 빠르게 무기화되며(Chien et al., 2009; Ernst and Massey, 1960), 무기화된 질소는 식물에 이용되어진다. 요소는 urease에 의해 가수분해 되는 과정에서 암모늄(NH4+), OH-, CO2가 생성되기 때문에 요소 입자 주위의 토양은 높은 pH와 NH4+ 농도 조건이 형성된다. 이와 같은 조건은 암모니아 (NH3) 휘산을 촉진하여 상당량의 질소가 농경지로부터 손실된다(Sommer et al., 2004; Hayashi et al., 2008). 전 세계적으로 농경지에 시용된 질소의 평균 14%(10-19%)가 암모니아 형태로 휘산되는 것으로 알려져 있으며(Ferm, 1998; Kim et al., 2007), 농경지에서 휘산된 암모니아는 산성비의 원인 물질이 되며, 침적에 의해 수계 부영양화를 일으키는 등 생태계에 악영향을 미치는 것으로 알려져 있다(Janzen et al., 1999; Howarth and Marino, 2006).
현재 요소가 포함된 무기질 질소비료의 이용율 향상을 위해서 urease inhibitor(Di et al., 2007; Lee et al., 2005a; Lee et al., 2005b), lime 및 zeolite(Zaman et al., 2007) 등 다양한 방법이 활용되고 있다. 이 중에서 N-(n-butyl) thi-ophosphoric triamide(NBPT, 상품명“Agrotain”)이 가장 효과적이고 높은 경제성을 가지고 있다(Watson, 2000). 토양에 Agrotain을 요소와 함께 시용하면, Agrotain이 urease의 Ni과 강하게 결합하여 요소의 무기화를 지연 시키는 것으로 알려져 있다(Manunza et al., 1999). 목초 재배지에서의 urease inhibitor가 포함된 요소의 시용은 일반 요소 시용에 비해 29-93%의 암모니아 휘산을 감소시켰고, 목초의 수량을 증가 시켰다(Zaman et al., 2009). 그러나 농경지에 시용된 요소의 암모니아 휘산량은 재배환경에 큰 영향을 받는 것으로 알려져 있다(Hargrove, 1988; Terman, 1979). 따라서 본 연구는 우리나라의 대표 밭 작물인 배추를 대상으로 urease inhibitor (Agrotain) 피복 요소의 현장 적용성 평가를 실시하였다.
Materials and Methods
배추 재배시험본 시험은 경상남도 진주시 소재 경상대학교 실습포장에서 배추를 대상으로 agrotain 피복 요소 시용에 의한 질소 이용율 평가를 실시하였다. 그리고 포장시험 토양을 대상으로 암모니아 휘산량 평가를 실내 시험으로 평가하였다. 배추재배와 암모니아 휘산량 평가에 사용한 토양의 이화학적 특성은 Table 1과 같다. Agrotain이 피복된 요소의 배추에 대한 질소 이용율 평가를 위해서 표준시비량 대비 80%와 100% 두 수준을 설정하였으며 이를 표준시비량과 상호비교하였다. 배추 포장시험 시험처리는 질소를 처리하지 않은 대조구(Control), 표준시비량 질소의 80%를 요소 처리(GSP 80%), 표준시비량 질소의 100%를 요소처리(GSP 100%), 표준시비량 질소의 80%를 Agrotain 피복 요소 처리(GSP 80% + Agro), 표준시비량 질소의 100%를 Agrotain 피복 요소를 처리(GSP 100% + Agro) 하였고, 이때 Agrotain은 요소 중량에 0.15%를 피복하였다. 그리고 인산과 칼륨은 모든 처리구에 표준시비량을 시비하였으며 배추 재배시 표준시비량은 32.0 (N) - 7.8 (P2O5) - 19.8 (K2O) kg 10a-1이었다(Table 2).
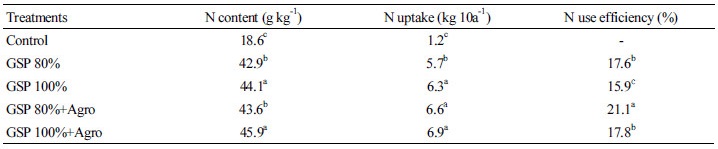
배추 재배 시험에 사용된 품종은 불암 3호로 2015년 8월 31일 기비 시용 후 경운하여 동년 동월 31일 80 × 45 cm 간격으로 모종을 이식 하였다. 이때 처리구당 면적은 30m2이었고 3반복으로 수행하였다. 배추 재배기간 1차 웃거름은 2015년 9월 22일 그리고 2차 웃거름은 동년 10월 12일 시비하였으며, 동년 11월 27일 수확하였다. 모든 시험은 완전임의 배치법 3반복으로 수행하였다. 수확한 배추 수량은 처리구당 10포기를 수확하여 측정하였으며, 배추 중 질소 함량은 식물체를 72°C에서 2일 건조 후 농촌진흥청 농사시험연구 기준에 따라 분석하였다(RDA, 2003). 그리고 질소이용율 (NUE)은 다음 식(1)에 근거하여 계산하였다.
Table 1. Selected properties of upland soil used in the experiment.
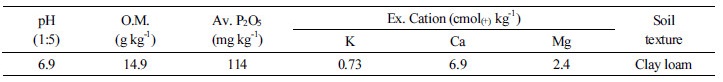
Table 2. The amount of fertilizer applied for the chinese cabbage cultivation.
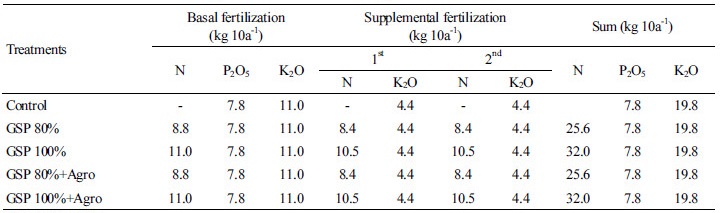
*Agro: Agrotain
Table 3. The amount of fertilizer applied for the experiment under upland condition.
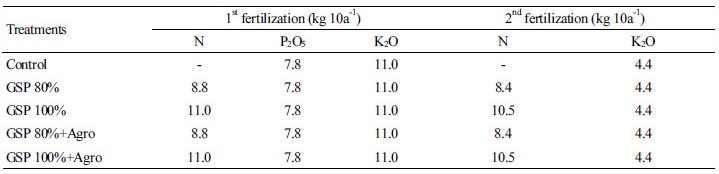
*Agro: Agrotain
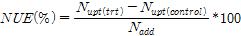 (1)
(1)
여기서 Nupt(trt)는 질소 처리구의 배추를 통한 질소 흡수량, Nupt(control)는 질소 무처리구(control)의 배추를 통한 질소 흡수량 그리고 Nadd는 질소 처리량을 의미한다.
Agrotain 피복요소의 암모니아 휘산량 평가는 포장시험지 토양을 이용하여 실내에서 Dynamics chamber 방법을 이용하여 연속적으로 측정하였다. 챔버 내에서 발생하는 암모니아 가스는 Fig. 1와 같이 포집용기내의 0.1N-H2SO4 용액에 포집하였다. 챔버 내에서 휘산되는 암모니아는 풍속에 영향을 받지 않게 air pump의 공기 흡입량을 flow meter (2 m sec-1)로 조절하였다(Kissel et al., 1977). 황산용액 내 포집된 암모니아 농도는 Indophenol-Blue 비색법(NIAST, 2000)을 이용하여 분석하였다. 각 처리별 시비량(Table 3) 중 1차 시비는 토양과 교반 하였으며, 2차 시비는 표층 시비 하였다. 시험 기간 중 암모니아 휘산량은 전량 포집하였으며 매일 황산용액에 포집된 암모니아 휘산량을 측정하여 전체 휘산량으로 계산하였다. 이때 토양의 수분함량은 포장용수량의 65%로 조절하여 일주일 간격으로 증발되는 수분을 보충하였다.
Fig. 1.
Experiment design for the measurement of ammonia volatilization.
Results and Discussion
배추 재배시험Agrotain 피복 요소 처리에 의한 배추 생체 수량은 무피복 요소 처리에 비해 증가하는 경향을 나타내었다(Fig. 2). 본 시험포장의 토양의 비옥도가 매우 낮은 이유로 무질소 처리구의 배추 수량은 질소 처리구보다 현저히 낮았다. Agrotain 피복 요소를 표준시비량 질소의 80% 처리한 GSP 80%+Agro 처리구의 배추 수량은 2.7 Mg ha-1로 무피복 동일량 요소 처리구에 비해서 17.2%의 증수 효과가 있었다. 그리고 Agrotain 피복 요소를 표준시비량 질소의 100% 처리한 GSP 100%+Agro 처리구의 배추 수량은 2.9 Mg ha-1로 무피복 동일량 요소처리구에 비해서 7.3%의 증수 효과가 나타났다. 이는 Agrotain 처리에 의한 건초의 증량인 9.5%와 유사한 결과를 보였다(Zaman et al., 2009).
Fig. 2.
Harvested weight of chinese cabbage applied fertilizer.
Agrotain 피복 요소 처리구의 배추 중 질소 함량은 동일량의 질소를 무피복 요소를 처리한 것에 비해서 증가 하는 경향을 보였다(Table 4). 그리고 Agrotain 피복요소를 표준시비량 질소 80%를 시용한 처리구의 질소 이용율은 21.1%로 무피복 요소 처리구에 비해서 3.5% 증가하였다. 표준시비량 질소의 100%를 Agrotain 피복 요소로 시용한 처리구의 질소 이용율은 무피복 요소 처리구에 비해서 1.9% 증가하는 경향을 보였다. 본 시험에서 배추에 대한 질소 이용율은 대부분 낮게 평가 되었으며 Agrotain 무피복 요소 처리에 의한 질소 이용율은 기존 연구결과인 47%보다 낮게 평가되었다(Yun et al, 2009). 이와 같은 결과는 본 시험에 이용된 포장의 양분 비옥도가 대단히 낮아서 평균 수량이 적었기 때문으로 생각된다.
Table 4. The nitrogen (N) content and N use efficiency in chinese cabbage.
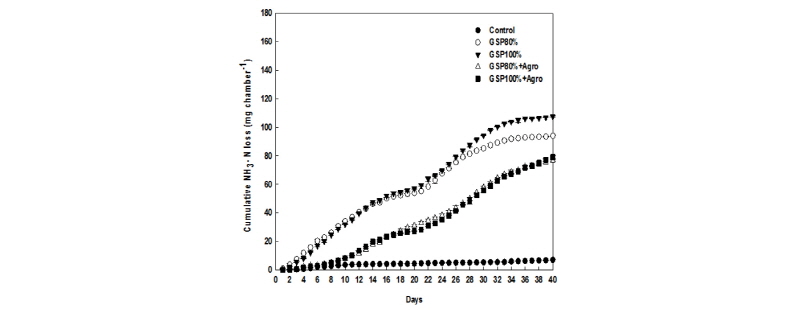
밭 조건에서 암모니아 휘산량 평가밭 토양 조건에서 Agrotain 피복 요소 처리에 의한 암모니아 휘산량은 Fig. 3과 같다. 처리한 요소비료에 대한 암모니아 휘산율은 GSP 80% 처리구에서 9.6%로 가장 높게 나타났으며, GSP 100%, GSP 80%+Agro, GSP 100%+Agro 순으로 높게 나타났다. 이는 중국(Cai et al., 1986)과 필리핀(Fillery et al., 1986)의 논에서의 요소 처리에 의한 암모니아 휘산량 8.8%와 13.0%와 비슷한 결과를 보였다. Agrotain 피복 요소 처리에 의한 암모니아 휘산량 저감율은 GSP 100% 대비 GSP 100%+Agro 처리구에서 28.3%, GSP 80% 대비 GSP 80%+Agro 처리구에서 20.2% 크게 감소하였다. 뉴질랜드 초지에서 Agrotain에 의한 소의 분뇨 처리로부터 발생되는 암모니아 휘산량 저감율인 42-81% 보다 낮게 측정 되었다(Surinder Saggar et al,. 2013; Yun et al., 2010). 그리고 Zaman et al., (2009)의 연구에서는 계절 별 Agrotain 처리에 따른 암모니아 휘산 저감량은 70.5%로 본 시험결과와 큰 차이를 보였다. 이와 같은 차이는 온도와 토양특성에서 기인된 것으로 판단된다. GSP 100% 처리구와 GSP 80% 처리구의 암모니아 휘산량은 큰 차이를 보였지만 GSP 100%+Agro 처리구의 암모니아 휘산량은 GSP 80% 처리구와 비슷한 값을 보였다. 따라서 Agrotain은 토양중에서 요소 가수분해 효소의 활성을 억제하여 암모니아 휘산량을 감소시키는 것으로 나타났다. Agrotain 피복 요소와 무피복 요소 시용 후 암모니아 휘산량은 1차와 2차 시용후 큰 차이를 나타낸 것은 1차 시비는 토양과 교반하였고, 2차 시비는 표층 시비로 인한 토양 교질과의 접촉 면적 차이 때문인 것으로 판단된다.
Fig. 3.
Cumulative ammonia losses from N fertilizer applied soil under upland condition.
Conclusion
Agrotain 피복 요소의 배추에 대한 질소 이용율은 GSP 80%+Agro, GSP 100%+Agro에서 각각 21.1, 17.8% 이었으며 동일량의 요소 처리에 따른 질소 이용율 보다 3.5, 1.9% 씩 증가하였다. 그리고 배추 수량은 GSP 80%+Agro, GSP 100%+Agro 처리구에서 동일 양의 요소를 처리하였을 때 비하여 각각 17.2, 7.3% 증수효과가 나타났다. Agrotain이 피복된 요소 비료 시용후 암모니아 휘산량은 GSP 100%+Agro에서는 동일 양의 요소 처리구인 GSP 100% 보다 28.3% 감소 하였으며, 또한 GSP 80%+Agro에서 GSP 80%에 비하여 20.2% 감소하였다. 따라서 Agrotain은 암모니아 휘산량을 감소 시켜 작물의 질소 이용율을 증가 시키는 것으로 나타났다.
Acknowledgements
This work was supported by a project of the Namhae Chemical Corp (Project No. 2016-0506).
References
Cai, G., Z. Zhu, A.C.F. Trevitt, J.R. Freney, and J.R. Simpson. 1986. Nitrogen loss from ammonium bicarbonate and urea fertilizers applied to flooded rice. Fertil. Res. 10:203-215.
Chien, S.H., L.I. Prochnow, and H. Cantarella. 2009. Recent developments of fertilizer production and use to improve nutrient efficiency and minimize environmental impacts. Adv. Agron. 102:267-322.
Di, H.J., K.C. Cameron, and R.R. Sherlock. 2007. Comparison of the effectiveness of a nitrification inhibitor, dicyandiamide, in reducing nitrous oxide emissions in four different soils under different climatic and management conditions. Soil Use & Manage. 23:1-9.
Ernst, J.W. and H.F. Massey. 1960. The effects of several factors on volatilization of ammonia formed from urea in the soil. Soil Sci. Soc. Am. Proc. 24(2):87-90.
Ferm, M. 1998. Atmospheric ammonia and ammonium transport in Europe and critical loads: a review. Nutr. Cycl. Agroecosys. 51:5-17.
Fillery, I.R.P., J.R. Simpson, and S.K. De Datta. 1986. Contribution of ammonia volatilization to total nitrogen loss after applications of urea to wetland rice fields. Fertil. Res. 8:193-202.
Hargrove, W.L., 1988. Soil, environmental, and management factors influencing ammonia volatilization under field conditions. In: Bock, B.R., Kissel, D.E. (Eds.), Ammonia volatilization from Urea Fertilizer. Natl. Fert. Dev. Center. Tenessee Valley Authority, Muscle Shoals, pp. 17-36 (Bull. Y-2006).
Hayashi, K., S. Nishimura, and K. Yagi. 2008. Ammonia volatilization from a paddy field following applications of urea: rice plants are both an absorber and an emitter for atmospheric ammonia. Sci. Total Environ. 390:485-494.
Heffer, P. and M. Prud'homme. 2011. Fertilizer Outlook 2011-2015. International Fertilizer Industry Association - IFA, Paris. Available at: http://www.fertilizer.org/ifa/HomePage/LIBRARY/Conference-papers/Annual-Conferences/2011-IFAAnnual-Conference (accessed on 11.03.12).
Howarth, R. and R. Marino. 2006. Nitrogen as the limiting nutrient for eutrophication in coastal marine ecosystems: evolving views over three decades. Limnol. Oceanogr. 51:364-376.
Janzen, H.H., R.L. Desjardins, J.M.R. Asselin, and B. Grace. 1999. The Health of Our Air: Toward Sustainable Agriculture in Canada. Agriculture and Agei-Food, Research Branch, Ottawa, p. 98.
Kim, S.J., J.E. Yang, B.O. Cho, J.J. Kim, and Y.O. Shin. 2007. Factors Controlling the Losses of Urea through Ammonia Volatilization. Korean J. Soil Sci. Fert. 40(1):77-82.
Kissel, D.E., H.L. Brewer, and Arkin. 1977. Design and test of a field sampler for ammonia volatilization, Soil Sci. Soc. Am. J. 41:1133-1138.
Lee, D.W., K.D. Park, C.Y. Park, U.G. Kang, I.S. Son, E.S. Yun, S.T. Park, and S.S. Lee. 2005a. Ammonia Volatilization from Coated Urea in Paddy Soil of Transplanting Rice Culture. Korean J. Soil Sci. Fert. 38(6):321-327.
Lee, D.W., K.D. Park, C.Y. Park, W.T. Jeon, I.S. Son, S.T. Park, S.S. Lee, and U.G. Kang. 2005b. Ammonia Volatilization from Coated Urea in Paddy Soil of Direct Seeding Rice Culture. Korean J. Soil Sci. Fert. 38(6):328-333.
Manunza, B., S. Deiana, M. Pintore, and C. Gessa. 1999. The binding mechanism of urea, hydroxamic acid and N-(N-butyl)-phosphoric triamide to the urease active site. A comparative molecular dynamics study. Soil Biol. Biochem. 31:789-796.
NIAST. 2000. Method of soil and plant analysis, National Institute of Agriculture Science and Technology. RDA, Suwon, Korea.
RDA. 2003. Standard methods for agricultural experiments, Rural Development Administration, Korea.
Sommer, S.G., J.K. Schjoerring, and O.T. Denmead, 2004, Ammonia emission from mineral fertilizers and fertilizes crop. Adv. Agron. 82:557-622.
Surinder, S., J. Singh, D.L. Giltrap, M. Zaman, J. Luo, M. Rollo, D.G. Kim, G. Rys, and T.J. van der Weerden. 2013. Quantification of reductions in ammonia emissions from fertiliser urea and animal urine in grazed pastures with urease inhibitors for agriculture inventory: New Zealand as a case study. Sci. of the Tot. Enviro. 465:136-146.
Terman, G.L. 1979. Volatilization losses of nitrogen as ammonia from surface applied fertilizers, organic amendments, and crop residues. Adv. Agron. 31:189-223.
Watson, C.J. 2000. Urease activity and inhibition: principles and practice. Proceeding No. 454, publication. The International Fertilizer Society, York, UK.
Yun, H.B., W.K. Park, S.M. Lee, S.C. Kim, and Y.B. Lee. 2009. Nitrogen Uptake by Chinese Cabbage and Soil Chemical Properties as Affected by Successive Application of Chicken Manure Compost. Korea J. Environ. Agri. 28:9-14.
Yun, H.B., Y. Lee, C.Y. Tu, J.E. Tang, S.M. Lee, J.H. Shin, S.C. Kim, and Y.B. Lee. 2010. Soil Nitrogen Mineralization Influenced by Continuous Application of Livestock Manure Composts. Korean J. Soil Sci. Fert. 43:329-334.
Zaman, M., M.L. Nguyen, F. Matheson, J.D. Blennerhassett, and B.F. Quin. 2007. Can soil amendments (zeolite or lime) shift the balance between nitrous oxide and dinitrogen emissions from pasture and wetland soils receiving urine or urea-N. Aust. J. Soil Res. 45:543-553.
Zaman, M., S. Saggar, D.J. Blennerhassett, and J. Singh. 2009. Effect of urease and nitrification inhibitors on N transformation, gaseous emissions of ammonia and nitrous oxide, pasture yield and N uptake in grazed pasture system. Soil Biol. Biochem. 41:1270-1280.

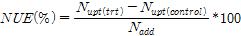 (1)
(1)