Introduction
식중독 발생은 후진국은 물론 생활수준이 높은 선진국에서도 계속해서 증가하는 추세에 있고 인간의 건강을 해칠 뿐만 아니라, 막대한 경제적인 손실을 야기하고 있다. 우리의 음식문화인 쌈과 서구화된 식탁에 등장한 샐러드 등 여러 종류의 채소를 가열, 조리하지 않은 채로 생식하는 일이 많아지고 있다 (Jung et al., 2006). 우리나라 국민 1인당 연간 식품 소비량의 경우 채소류는 연간 137.5 kg 수준으로 어패류 (41.3 kg), 육류 (52.9 kg)에 비해 많은 편이며, 주식인 곡류 (133.1 kg)에 비해서도 조금 높은 수준을 나타냈다 (Choi and Heo, 2016). 하지만 신선한 과일과 채소 등 신선 농식품의 소비가 증가되면서 최근 신선 과일 및 채소로 인한 식중독 발생이 증가하고 있다 (Sivapalasingam et al., 2004). 채소류는 토양에서 생산되기 때문에 자연적으로 토양에 존재하는 다양한 미생물에 노출되어 있다 (Beuchat et al., 2001). 외국의 농산물 식중독 사고에서 알 수 있듯이 과일 및 채소와 같은 신선 농산물은 수확 후 소비되는 과정의 여러 단계에서 병원성 미생물을 포함한 다양한 미생물에 오염될 수 있다 (Kang et al., 2011). 가공처리를 통해 초기 병원성 미생물을 일부 제거하더라도 저장·유통 중 적당한 온도와 습도 조건에서 병원성 미생물이 증식하여 식중독을 유발할 수 있다 (NACMCF, 1999).
실제로 상추, 깻잎 등의 채소류에서 식중독균인 B. cereus가 검출되었고 (Ueda, 1998) 채소류, 구근류 등에서도 대장균군, 대장균, B. cereus 등이 조사되었다 (Kim et al., 2006). Jung et al. (2006)은 비가열 채소류의 미생물 오염도를 조사한 결과 치커리에서 S. aureus와 B. cereus가 22%로 가장 많이 검출되었으며, B. cereus는 쑥갓에서도 많이 검출되었다고 하였다. Kim et al. (2004)은 즉석 섭취용 샐러드 제품의 미생물 오염조사에서 대장균군, 대장균, S. aureus, Salmonella spp. 등이 검출되었다고 보고하였다. 그리고 Kim and Shin (2008)은 비 전처리 채소 및 전처리 채소에서 B. cereus, Campylobacter jejuni, Vibrio parahaemolyticus, S. aureus 등이 검출되었다고 하였다. Burnett and Buechat (2001)은 채소나 과일은 병원성 미생물에 의해 오염될 수 있는데 그 오염 원인으로는 토양, 가축분뇨, 관개수, 먼지, 미숙퇴비 등을 들 수 있으며 다양한 종류의 병원성 미생물이 식중독을 야기할 수 있지만 이중 Shigella spp., Salmonella, E. coli O157:H7, Campylobacter spp., L. monocytogenes, S. aureus, Yersinia enterocolitica, B. cereus, Clostridium botulinum, viruses 등이 과일과 채소와 같은 신선 농산물과 관련하여 식중독 사고 및 국민의 건강상의 문제에 크게 상관성이 있는 것으로 보고하였다. 병원성 미생물에 오염된 토양이나 퇴비가 농산물에 접촉되어 사람이 오염 농산물을 섭취하면 식중독이 발생할 수 있다 (Morgan et al., 1988). Maule (2000)은 병원성 미생물이 토양이나 퇴비에 장시간 생존할 수 있고 인간에게 전이되어 감염시킬 수 있다고 하였다. Morgan et al. (1988)은 영국에서 E. coli O157에 의한 최초의 식중독 사고는 토양에 존재하던 병원균과 관여되어 있다고 하였는데 당시 24명의 환자 중 1명이 사망하였다. 관개용수, 퇴비 등의 농자재 등을 통해 식중독세균이 토양으로 유입될 수 있으며, 토양 내에서 오랫동안 생존하여 오염이 발생할 수 있다 (Ibenyassine et al., 2006). 그러므로 우리나라에서 농산물 생산단계의 토양 내에 존재하는 병원성 미생물의 분포를 알아보는 것은 재배단계 농작물의 안전성을 확인하는데 있어 매우 중요하다고 할 것이다. 본 연구는 국내에서 많이 소비되고 있는 배추 재배 토양을 대상으로 일반 세균수, 대장균, 대장균군, Salmonella spp., E. coli O157:H7, L. monocytogenes, S. aureus 등의 병원성 미생물의 분포 및 오염도를 조사하여 토양의 미생물학적 안전성 확보를 위한 기초자료를 제공하고자 수행하였다.
Materials and Methods
검체 채취 대상 및 방법 전국 주요 배추 재배지 중에서 4개 지역을 선정하였으며 2017년 2월부터 8월까지 배추 재배 토양을 대상으로 Ⅰ지역 (7월, 3농가 19점), Ⅱ지역 (8월, 3농가 17점), Ⅲ지역 (5월, 3농가 11점), Ⅳ지역 (2월, 3농가 10점)에서 총 57점의 시료를 채취하였다. 토양시료는 재배지의 표토를 0~15 cm 깊이로 채취하였다. 채취된 시료는 냉장상태로 보관하여 실험실로 운반한 후 냉장보관하면서 24시간 이내에 실험을 실시하였고 일반세균수, 대장균군, E. coli은 정량적 분석을 수행하였고, Salmonella spp., E. coli O157:H7, L. monocytogenes, S. aureus는 정성적 분석을 수행하였다.
일반세균수, 대장균군, 대장균의 정량적 분석 일반세균수, 대장균군, 대장균의 정량적 분석은 식품공전 방법 (KFDA, 2008)에 의해 실시되었다. 일반세균수 (total aerobic bacteria)의 정량적 분석을 위해서 검체 25 g을 취하여 0.85% 생리식염수 225 mL와 혼합하고 균질기 (BagMixerⓇ 400, Interscience, Saint-Nom la Breteche Arpents, France)에서 2분간 균질화하였다. 그 중 시료 1 mL을 Petrifilm Aerobic Count Plate (3M)위에 분주하여 37°C에서 24~48시간 배양하였다. 희석액으로 단계 희석한 후 Petrifilm 위에 형성된 colony를 계수하여 colony-forming unit (CFU) g-1으로 나타내었다. 또한 대장균군 (coliform) 및 대장균 (E. coli)의 정량적 분석을 위해서는 Petrifilm E. coli/Coliform Count Plate (3M)에 분주하여 37°C에서 24~48시간 배양하였다. 배양 후 기포를 가진 blue colony를 E. coli 양성으로, 기포를 가진 red colony와 기포를 가진 blue colony를 coliform 양성으로 간주하여 계수하였다.
Salmonella spp.의 정성적 분석 Salmonella spp.의 정성적 분석은 식품공전 방법 (KFDA, 2008)에 의해 실시되었다. 검체 25 g을 취하여 buffered pepton water (BPW, Difco, USA) 225 mL이 담겨진 멸균된 stomacher bag에 넣어 균질기 (BagMixerⓇ 400, Interscience)를 이용하여 2분간 균질화 한 다음 37°C에서 24시간 동안 배양하였다. 증균된 액 1mL을 Rappaport-Vassiliadis broth (Difco, USA) 9 mL에 넣어 42°C에서 24시간 동안 배양하였다. 2차 증균 배양된 액은 Xylose lysine desoxycholate agar (XLD, Difco, USA)에 획선 도말하였고, 37°C에서 24시간 동안 배양하였다. 배양 후 의심되는 colony는 latex agglutination test (Microgen Bioproducts, UK)로 확인하였고, 확정을 위해 colony를 TSA에 계대한 후, API kit (API 20E)와 PowerCheckTM Salmonella spp. Detection Kit (Power check PCR kit, Kogen, Korea)를 이용하여 PCR (Biorad, USA)로 확인하였다. PCR 반응에서 DNA 5 µL primer는 10 pM 농도로 2쌍 첨가하고 3차 멸균 증류수로 최종 반응용액을 20 µL로 조절하였다. 또한 PCR thermal cycler의 반응 조건은 95°C에서 10분간 predenaturation을 실시한 후, 95°C에서 30초간 denaturation, 60°C에서 30초간 primer annealing, 72°C에서 30초간 extension의 조건으로 35 cycle을 수행하고, final extension을 72°C에서 10분간 실시하였다. PCR에 의한 증폭생성물은 2.0% agarose gel 전기영동에 의해 확인하였다.
E. coli O157:H7의 정성적 분석 E. coli O157:H7의 정성적 분석은 식품공전 방법 (KFDA, 2008)에 의해 실시되었다. 검체 25 g을 취하여 novobiocin antimicrobic supplement (BactoTM Oxford antimicrobic supplement, Difco)를 첨가한 EC Medium, Modified (mEC, Difco, USA) 225 mL가 들어있는 멸균된 stomacher bag에 넣어 균질기 (BagMixerⓇ 400, Interscience)를 이용하여 2분간 균질한 후 42°C에서 24시간 동안 배양하였다. 증균된 액은 Sorbitol MacConkey agar (SMAC, Difco)에 획선 도말하였고, 37°C에서 24시간 동안 배양하였다. 배양 후 의심되는 colony는 latex agglutination test (Microgen Bioproducts, UK)로 확인하였고, 확정을 위해 colony를 TSA에 계대한 후, API kit (API 20E)와 PowerCheckTM E. coli O157:H7 Detection Kit (Power check PCR kit, Kogen, Korea)를 이용하여 PCR (Biorad, USA)로 확인하였다. PCR 반응에서 DNA 5 µL primer는 10 pM 농도로 2쌍 첨가하고 3차 멸균 증류수로 최종 반응용액을 20 µL로 조절하였다. 또한 PCR thermal cycler의 반응 조건은 95°C에서 10분간 predenaturation을 실시한 후, 95°C에서 30초간 denaturation, 60°C에서 30초간 primer annealing, 72°C에서 30초간 extension의 조건으로 35 cycle을 수행하고, final extension을 72°C에서 10분간 실시하였다. PCR에 의한 증폭생성물은 2.0% agarose gel 전기영동에 의해 확인하였다.
L. monocytogenes의 정성적 분석 L. monocytogenes의 정성적 분석은 식품공전 방법 (KFDA, 2008)에 의해 실시되었다. 검체 25 g을 취하여 UVM (University of Vermont Medium)-Modified Listeria (Difco, USA) 225 mL이 들어있는 멸균된 stomacher bag에 넣어 균질기 (BagMixerⓇ 400, Interscience)를 이용하여 2분간 균질화 한 다음 37°C에서 24시간 동안 배양하였다. 증균된 액 1 mL을 Fraser Listeria broth (Difco, USA) 9 mL에 넣은 후 37°C에서 24시간 동안 배양하였다. 2차 증균된 액은 antimicrobic supplement (BactoTM Oxford antimicrobic supplement, Difco)를 첨가한 Oxford agar base (OAB, Difco)에 획선 도말하였고, 37°C에서 24시간 동안 배양하였다. 배양 후 의심되는 colony를 TSA에 계대한 후, API kit (API Listeria)와 PowerCheckTM Listeria monocytogenes Detection Kit (Power check PCR kit, Kogen, Korea)를 이용하여 PCR (Biorad, USA)로 확인하였다. PCR 반응에서 DNA 5 µL primer는 10 pM 농도로 2쌍 첨가하고 3차 멸균 증류수로 최종 반응용액을 20 µL로 조절하였다. 또한 PCR thermal cycler의 반응 조건은 95°C에서 10분간 predenaturation을 실시한 후, 95°C에서 30초간 denaturation, 60°C에서 30초간 primer annealing, 72°C에서 30초간 extension의 조건으로 35 cycle을 수행하고, final extension을 72°C에서 10분간 실시하였다. PCR에 의한 증폭생성물은 2.0% agarose gel 전기영동에 의해 확인하였다.
S. aureus의 정성적 분석 S. aureus의 정성적 분석은 식품공전 방법 (KFDA, 2008)에 의해 실시되었다. 검체 25 g을 취하여 10% NaCl이 첨가된 tryptic soy broth (TSB, Difco, USA) 225 mL이 담겨진 멸균된 stomacher bag에 넣어 균질기 (BagMixerⓇ 400, Interscience)를 이용하여 2분간 균질화한 다음 37°C에서 24시간 동안 배양하여 내염성을 가지는 S. aureus를 증균하였다. 증균 배양된 액은 egg yolk가 첨가된 Baird Paker agar (BPA, Difco, USA)에 획선 도말하였고, 37°C에서 24시간 동안 배양되었다. 배양 후 검정색 colony를 계수하였으며, tryptic soy agar (TSA, Difco)에 계대하였다. 개별 colony를 API kit (API Staph, Bio-merieux, France)와 PowerCheckTM Staphylococcus aureus Detection Kit (Power check PCR kit, Kogen, Korea)를 이용하여 PCR (Biorad, USA)로 확인하였다. PCR 반응에서 DNA 5 µL primer는 10 pM 농도로 2쌍 첨가하고 3차 멸균 증류수로 최종 반응용액을 20 µL로 조절하였다. 또한 PCR thermal cycler의 반응 조건은 95°C에서 10분간 predenaturation을 실시한 후, 95°C에서 30초간 denaturation, 60°C에서 30초간 primer annealing, 72°C에서 30초간 extension의 조건으로 35 cycle을 수행하고, final extension을 72°C에서 10분간 실시하였다. PCR에 의한 증폭생성물은 2.0% agarose gel 전기영동에 의해 확인하였다.
통계 처리 분석된 모든 결과들에 대해서는 SPSS 통계처리 프로그램 version 11을 사용하여 통계분석하였다. 통계분석은 ANOVA 프로그램의 Tukey's test으로 p < 0.05의 수준에서 통계학적 유의성을 검증하였다.
Results and Discussion
배추 재배 토양 중의 일반 세균수와 대장균군, 대장균의 분포 4개 지역의 배추재배 토양 각각에 대한 일반 세균수를 조사한 결과 (Table 1), Ⅰ지역 토양의 일반 세균수는 최소 5.7 log CFU g-1, 최대 8.7 log CFU g-1, 평균 6.9 log CFU g-1, Ⅱ지역 토양은 최소 6.3 log CFU g-1, 최대 7.7 log CFU g-1, 평균 6.8 log CFU g-1, Ⅲ지역 토양은 최소 6.0 log CFU g-1, 최대 8.2 log CFU g-1, 평균 7.1 log CFU g-1, Ⅳ지역 토양은 최소 5.8 log CFU g-1, 최대 7.1 log CFU g-1, 평균 6.3 log CFU g-1이었다. 토양의 일반세균수는 지역별로 유의한 차이가 없었다 (p > 0.05).
Table 1. Population of total aerobic bacteria in soil.
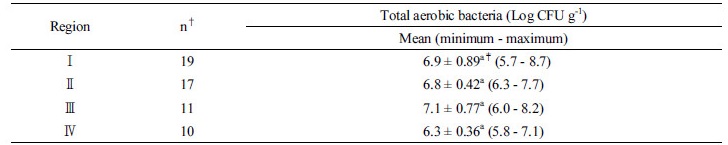
†Number of samples analyzed.
‡Means with the same letter within a column are not significantly different at P > 0.05.
4개 지역의 토양에서 대장균군은Ⅰ지역 토양 19시료 중 13시료 (68%)에서, Ⅱ지역 토양 17시료 중 15시료 (88%)에서, Ⅲ지역 토양 11시료 중 9시료 (82%)에서, Ⅳ지역 토양 10시료 중 2시료 (20%)에서 검출되었다 (Table 2). Ⅱ지역 토양의 대장균군 검출율이 가장 높았고, Ⅳ지역 토양의 대장균군 검출율이 가장 낮았다. Ⅳ지역의 시료채취 시기는 가장 온도가 낮은 겨울이었는데 온도의 영향으로 Ⅳ지역 토양의 대장균군 검출율이 가장 낮았다고 생각한다. 병원성 미생물의 생존에 영향을 미치는 요인으로 온도, 습도, pH, 미생물간 경쟁 등이 있다고 하였는데 (Hill and Sobsey, 2001) 이 중 병원성 미생물의 생존에 주된 영향을 미치는 요인은 온도라고 하였다 (Tiquia, 2005). Ishii et al. (2006)는 토양에서 대장균군이 여름, 가을 보다 온도가 낮은 겨울에 훨씬 낮은 밀도로 검출되거나 불검출되었다고 하였는데 본 결과와 흡사하였다. 대장균군수의 경우 Ⅰ지역 토양에서, 그 범위는 2.4~5.5 log CFU g-1, 평균 3.9 log CFU g-1 수준으로 나타났고, Ⅱ지역 토양에서, 범위는 2.8~6.3 log CFU g-1, 평균 4.6 log CFU g-1 수준으로 나타났다. 또한, Ⅲ지역 토양에서, 범위는 2.4~5.5 log CFU g-1, 평균 4.7 log CFU g-1 수준으로 나타났으며, Ⅳ지역 토양에서, 범위는 1.1~1.4 log CFU g-1, 평균 1.3 log CFU g-1 수준이었다. Ⅲ지역 토양의 대장균군수가 가장 높았고, Ⅳ지역 토양의 대장균군수가 가장 낮았다. Ⅳ지역의 대장균군수가 가장 낮은 결과도 겨울의 낮은 온도 영향으로 판단한다. 대장균군은 유당을 분해하여 가스나 산을 발생하는 그람 음성의 아포를 만들지 않는 간균을 지칭하는 것으로 대장균군이 검출되면 병원성이 있는 유해미생물과 대장균의 존재 가능성을 의미하고 있다.
Table 2. Incidence of coliforms in soil.
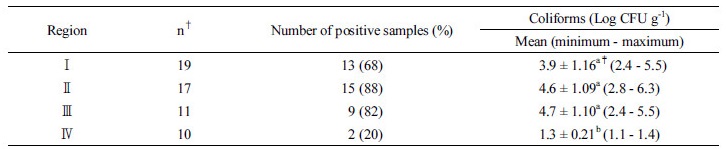
†Number of samples analyzed.
‡Means with the same letter within a column are not significantly different at P > 0.05.
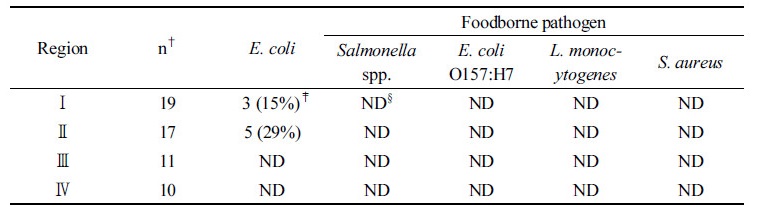
각 지역 토양에서 대장균은 Ⅰ지역 19시료 중 3시료 (15%)에서, Ⅱ지역 17시료 중 5시료 (29%)에서 검출되었고, Ⅲ, Ⅳ지역 토양에서는 전혀 검출되지 않았다 (Table 3). 대장균의 경우 Ⅰ지역 토양에서, 범위는 0.7~4.0 log CFU g-1, 평균 2.0 log CFU g-1 수준으로 나타났고, Ⅱ지역 토양에서, 범위는 2.1~3.0 log CFU g-1, 평균 2.4 log CFU g-1 수준으로 나타났다. Ishii et al. (2006)은 토양에서 대장균이 3.0 log CFU g-1 까지 검출되고, 25°C 이하 토양에서 30일 이상 생존할 수 있다고 하였다. 또한 E. coli O157:H7는 토양에서는 130일 동안 생존할 수 있다고 보고하였다 (Maule, 2000). 대장균은 토양에 오래 생존할 수 있고 또한 작물을 오염시킬 가능성이 있으므로 오염원을 차단하는 등의 철저한 위생관리가 필요하다.
Table 3. Incidence of E. coli in soil.

†Number of samples analyzed.
‡Means with the same letter within a column are not significantly different at P > 0.05.
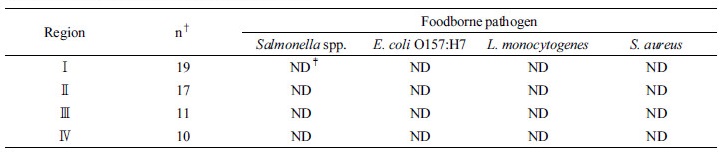
토양 중의 병원성 미생물의 분포 각각의 토양에 오염된 병원성 미생물을 검출하기 위하여 각 시료를 selective enrichment broth와 selective agar에서 배양하고, 배양 후 selective agar에서 의심되는 colony는 PCR로 확인한 결과 4개 지역 토양에서 Salmonella spp., E. coli O157:H7, S. aureus, L. monocytogenes 등은 검출되지 않았다 (Table 4).
식중독균은 본 실험에서는 검출되지 않았지만 Catherine et al. (2014)은 토양에서 Salmonella spp., Clostridium perfringens, B. cereus와 같은 병원성 미생물이 검출되었고 이 병원성 미생물은 토양, 관개수를 통하여 작물을 오염시킬 수 있다고 하였다. 식중독을 일으키는 병원성 미생물은 장내세균이지만 외부로 노출되었을 때 생존할 수 있다는 보고 (Unc and Goss, 2004)와 토양에서도 130일 동안 생존할 수 있다 (Maule, 2000). Welshimer (1960)은 L. monocytogenes가 토양에서 67일 동안 생존할 수 있다고 하였고, You et al. (2006)은 병원성 미생물이 가축분 퇴비가 포함된 토양에서 증식할 수 있다고 하였다. Islam et al. (2005)은 E. coli O157:H7로 오염된 퇴비를 토양에 주었을 때 E. coli O157:H7이 상추표면으로 옮겨질 수 있다고 하였고 E. coli O157:H7로 오염된 토양에서 이 균은 양상추 뿌리를 통하여 잎으로 이동될 수 있다 (Solomon et al., 2002). 따라서 토양에 존재하는 병원성 미생물은 장기간 생존할 수 있고 작물로 이동할 수 있으므로 농산물로 인한 식중독 사고를 예방하기 위해서는 병원성 미생물이 토양에 존재하지 않도록 관리하는 것이 중요하다. 미생물학적으로 안전한 토양 조건을 위해서는 안전한 가축분 퇴비와 액비를 사용하는 것이 가장 좋은 방법이다. 현재 우리나라 가축분 퇴비와 액비에서 Salmonella와 E. coli O157:H7 같은 병원성 미생물에 관한 기준이 있지만 농식품 안전에 관한 소비자의 관심이 커지고 있는 현실을 고려하면 Salmonella와 E. coli O157:H7 외의 병원성 미생물을 추가 지정하여 미생물학적으로 안전한 퇴비와 액비가 생산되도록 제도적으로 기준을 강화할 필요가 있다고 생각한다. 또한 농산물의 미생물 위해평가의 기초자료 확보를 위해서는 토양의 지속적인 병원성 미생물 실태조사가 필요하다고 생각한다.
Conclusions
본 연구는 국내에서 많이 소비되고 있는 배추 재배 토양을 대상으로 일반 세균수, 대장균, 대장균군, Salmonella spp., E. coli O157:H7, L. monocytogenes, S. aureus 등의 병원성 미생물의 분포 및 오염도를 조사하여 토양의 미생물학적 안전성 확보를 위한 기초자료를 제공하고자 수행하였다. 4개 지역의 배추재배 토양에 대한 일반 세균수를 조사한 결과, Ⅰ지역 토양의 일반 세균수는 5.7~8.7 log CFU g-1, Ⅱ지역 토양은 6.3~7.7 log CFU g-1, Ⅲ지역 토양은 6.0~8.2 log CFU g-1, Ⅳ지역 토양은 5.8~7.1 log CFU g-1이었다. 4개 지역의 토양에서 대장균군은 Ⅰ지역 토양 19시료 중 13시료 (68%)에서, Ⅱ지역 토양 17시료 중 15시료 (88%)에서, Ⅲ지역 토양 11시료 중 9시료 (82%)에서, Ⅳ지역 토양 10시료 중 2시료 (20%)에서 검출되었다. 대장균은 Ⅰ지역 19시료 중 3시료 (15%)에서, Ⅱ지역 17시료 중 5시료 (29%)에서 검출되었고, Ⅲ과 Ⅳ지역 토양에서는 전혀 검출되지 않았다. 4개 지역 토양에서 Salmonella spp., E. coli O157:H7, S. aureus, L. monocytogenes 등은 검출되지 않았다. 병원성 미생물은 토양이나 퇴비에서 장시간 생존할 수 있고 작물을 오염시킬 수 있으므로 농산물로 인한 식중독 사고를 예방하기 위하여 병원성 미생물이 토양에 존재하지 않도록 관리하는 것이 중요하다. 그러기 위해서는 충분히 부숙한 퇴비와 액비를 생산하는 것이 최선의 방법이라고 생각한다.