Introduction
오늘날 세계적으로 도시화 및 산업화로 인해 인간 삶의 질은 향상되었지만, 무차별적인 개발로 발생된 수많은 오염물질은 주변 자연환경을 오염시킬 뿐만 아니라 인간 건강에 대한 위해성을 증가시켰다. 특히, 광산개발사업 이후 휴 ․ 폐광산 주변지역은 독성물질인 중금속 유출로 인해 심각한 토양 및 수질 오염이 진행되고 있다. 우리나라 휴 ․ 폐광산 주변지역 토양오염 조사결과 대부분의 광산 주변지역이 카드뮴, 구리, 납 및 아연 등과 같은 중금속으로 오염되어 있는 것이 확인되었다 (MoE, 2015; Yang et al., 2006).
우리나라에서는 현재 다수의 폐광산 주변지역에 대한 토양 위해성 평가를 수행하여, 많은 지역이 농경지로 사용하기에 부적합하며, 인체에 위해성이 있음을 보고하고 있다 (Choi et al., 2010; Kim et al., 2009b; Lim et al., 2008; Park et al., 2011). 하지만, 폐광산 주변에서의 상당한 중금속 검출에도 불구하고 휴 ․ 폐광산 주변 지역 상당수가 여전히 농경지 및 주거지로 이용되고 있다. Jung and Thornton (1997)의 연구결과에 따르면 Pb-Zn 광산주변 농경지 벼에서 0.21 mg kg-1의 Cd이 검출되어, 벼의 식품공전 기준 (0.2 mg kg-1)을 초과하는 것으로 나타났다. Lim et al. (2008)가 송천 Au-Ag 광산주변 토양에서 재배된 작물 중 중금속함량을 조사한 결과에 따르면, 고추 (0.39~0.42 mg kg-1), 배추 (1.65~3.20 mg kg-1), 상추 (2.2 mg kg-1), 감자 (1.5~3.0 mg kg-1) 등 이 지역에서 재배된 대다수 작물에서 우리나라 식물체 중 평균 비소농도인 0.09 mg kg-1 (Jung, 1995)보다 높게 검출되었다. 따라서 중금속 위해성을 최소화하기 위한 오염지역 주변토양 관리방안을 마련하기 위한 연구의 필요성이 대두되고 있다 (Naidu et al., 2003a).
우리나라를 포함한 세계 여러 국가에서는 중금속 총 함량을 기준으로 오염 정도를 분류하여 토양 중 중금속에 대한 안전관리를 시행하고 있다. 하지만, 중금속 오염지에서 생산되는 농산물 안전관리 측면에서 볼 때, 중금속 총 함량 기준 적용은 부적합할 수도 있다. 왜냐하면 토양으로부터 식물로 이동하는 중금속은 뿌리의 흡수를 통해 식물체내로 전이 및 축적이 되는데, 이는 토양 특성 (pH, 유기물, 영양분, 점토함량 및 미생물 등)과 환경적 요소에 따라 중금속 이동성 및 식물 유효태 농도가 상이하기 때문이다 (Adriano, 1986; Kim et al., 2011; Lee et al., 2012; Nicholson et al., 1997). Rosas-Castor et al. (2014)은 옥수수 재배 토양 내 비소 식물유효도에 대한 연구를 통해, 토양 중 철 ․ 망간 산화물이 비소의 강한 흡착제 역할을 하고, 토양 pH에 따라 비소 화학종 분포도가 변화하여 유효도가 변이하며, 토양 중 인 (P) 함량이 식물의 비소 흡수량과 역 (negative)의 상관관계를 밝혀내었다. 또한 이 저자들은 토양 중 미생물과 유기물 함량이 비소의 식물 유효도에 영향을 미치는 것을 보고하였다.
효율적인 중금속 오염토양 관리를 통한 안전한 농산물 생산을 위해서는 중금속 총 함량 분석기준은 적절치 않은 것으로 생각된다 (Heemsbergen et al., 2009; Kim et al., 2009a; Naidu et al., 2003b; Salazar et al., 2012). 이에 효율적인 토양환경 관리를 위한 중금속 유효도 측정법을 연구하기 위해 다양한 화학적 침출법이 이용되고 있다. 토양 내 비소의 식물 유효태 함량을 측정하기 위한 방법에는 수용성 침출 (Száková et al., 2009), 킬레이트 (EDTA and DTPA) 침출 (Bermond et al., 1998; Hammer and Keller, 2002; Jackson and Alloway, 1991), 중성염 (0.05 M (NH4)2SO4, 1 M NH4NO3, 0.5 M NaHCO3, 0.01 M CaCl2) 침출 (DIN, 1995; McLaughlin et al., 1999; Nolan et al., 2005) 등 다양한 방법이 있다.
독일에서는 1 M NH4NO3-extractable 비소농도 0.1 mg kg-1을 토양관리 기준으로 적용하여 농경지에서 오염도를 규제하고 있다 (Prueb, 1997). 이밖에 많은 연구에서 토양 중 extractable 비소농도와 식물체 내 비소농도간의 높은 연관성을 보고하고 있다. Chojnacka et al. (2005)은 0.1 M NaNO3와 2% (NH4)2C6H5O7 침출용액을 이용하여 토양 중 비소농도가 밀에 농축된 비소함량과 높은 상관성이 있음을 보고하였다. Giri et al. (2012)은 0.5 M NaHCO3로 침출한 논 토양 중 비소농도와 쌀에 축적된 비소함량 사이에 상당한 상관관계가 있다고 설명하였다.
그동안 우리나라의 토양 중 비소의 식물유효태 농도와 식물체 비소농도간의 상관관계 연구는 주로 1 M HCl, 1 M NH4NO3, 또는 킬레이트제 (EDTA 등)로 추출된 토양 중 비소농도와 벼에서 검출된 비소농도의 상관관계에 대한 연구로 국한되어 왔다 (Kim et al., 2010; Oh et al., 2015). 이에 따라 벼 이외 다양한 작물 중 비소함량을 예측, 규제하기 위해서는 토양 중 비소 유효태 침출법에 대한 다양한 연구가 필요하다.
이에 본 연구에서는 다양한 식물 유효태 침출법 (0.1 M Ca(NO3)2, 0.1 M (NH4)2HPO4, 0.5 M EDTA, Mehlich 3, and 0.5 M NaHCO3)을 이용하여, 폐광산 주변 농경지에서 생산되는 벼 (백미), 고추 및 콩의 비소 함량과 토양 중 식물 유효태 농도간 상관관계를 밝히고, 작물의 가식부 비소농도를 예측하기 위한 가장 적합한 침출법을 모색하고자 한다.
Materials and Methods
공시재료 본 실험을 위해 국내 폐광산 지역을 선정한 후 (Fig. 1), 이 지역에서 현재 농경지로 이용되고 있는 20 지점 (경상도: 6 지점, 전라도: 3 지점, 충청도: 11 지점)을 선정하고 각 지점에서 약 50 kg의 표토 (0~20 cm)를 채취하였다. 채취한 토양을 서울시립대학교 온실로 운반하여 식물 뿌리 등을 제거하고 4 mm 체로 균일하게 체거름 한 후, 포트실험에 이용했다. 재배작물로 우리나라의 대표 작물종인 고추 (Capsicum annuum L.), 콩 (Glycine max L.) 및 벼 (Oryza sativa L.)를 선정하였다.
온실실험 포트 (직경 20 cm, 높이 30 cm)에 각 지역의 토양 약 3 kg을 채운 뒤, 고추, 콩, 및 벼 종자를 약 3 cm 깊이에 파종하여, 각각의 작물 가식부가 수확이 가능할 때까지 약 3개월 동안 서울시립대학교 온실에서 재배하였다. 토양 pH 및 유기물 함량의 변화가 비소의 식물 유효도에 미치는 영향을 알아보기 위해, 두 처리구 (2% 석회처리 및 2% 석회 + 3% 퇴비 처리구를 추가하였다. 총 180개 (20 지점 × 3 작물 × 3 처리구)의 포트를 온실 바닥에 임의로 배치하여 가식부의 수확이 가능할 때까지 작물을 재배하였다.
토양 분석 토양 이화학성을 분석하기 위해 토양을 풍건한 후, 2 mm 체로 체거름하였다. 토양 pH와 전기전도도 (electrical conductivity, EC)는 토양과 증류수를 1:5 비율로 혼합하여 한 시간 동안 교반 후, 각각 pH 측정기 (MP220, Mettler Toledo, Switzerland)와 EC 측정기 (MC226, Mettler Toledo, Switzerland)로 측정하였다. 토양 유기물 함량은 500°C 오븐에서 5시간 태워 강열감량법 (NAAS, 2010)으로 측정하였고, 점토 함량은 마이크로피펫법 (Miller and Miller, 1987)으로 측정하였다. 토양 중 용존유기탄소 (dissolved organic carbon, DOC) 분석은 토양시료 5 g과 증류수 25 mL를 50 mL 시험관에서 1시간 동안 교반하고, 3000 rpm으로 원심분리한 뒤 유리섬유 필터 (< 0.45 µm)로 여과한 용액을 TOC 분석기 (2100S, Analytik Jena, Germany)로 측정했다. 토양 중 비소 총함량 측정을 위해 막자사발로 곱게 간 토양 시료 1 g에 9 mL의 왕수 (aqua regia)를 넣고 흑연블럭분해기 (OD-98-001, ODLAB, Korea)로 분해하였으며 (NAAS, 2010), 분해 용액을 Whatman No. 42 여과지 (pore size 2.5 µm)로 거른 후 용액 중 비소의 함량을 ICP-OES (8300DV, Perkin Elmer, USA)로 측정하였다. 토양 분석의 정확도를 검정하기 위해 표준시료 (Montana Soil SRM 2711, National Institute of Standards &Technology)와 공시료를 분석 세트에 포함시켜 분해가 적절히 완료되었는지를 점검하였다.
토양 중 비소 식물유효도는 총 5가지 추출용액 [Mehlich 3, 0.05 M EDTA, 0.5 M NaHCO3, 0.01 M Ca(NO3)2, 및 0.1 M (NH4)2HPO4]으로 추출한 후 추출액 중 비소 농도를 ICP-OES (8300DV, Perkin Elmer, USA)으로 측정하였다. Mehlich 3 추출을 위하여 토양 2 g에 20 mL의 추출용액 (0.2 N acetic acid; 0.25 N NH4NO3; 0.015 N NH4F; 0.013 N HNO3; 0.001 M EDTA)을 취하여 5분간 진탕 후 Whatman No. 42 여과지로 여과하였다 (Mehlich, 1984). EDTA 침출법에서는 토양 5 g에 0.05 M EDTA용액 50 mL를 넣고 1시간 진탕한 뒤 여과하였다 (Manouchehri et al., 2006). NaHCO3 용액 침출법을 위해 토양 3 g에 0.5 M NaHCO3 30 mL를 넣고 2시간 진탕 후 여과하여 측정에 사용하였다 (Huang et al., 2005). Ca(NO3)2 침출법에서는 토양 10 g에 0.01 M Ca(NO3)2 용액 20 mL를 넣고 2시간 진탕 후 여과하였으며 (Si et al., 2006), (NH4)2HPO4 침출법 (Gallardo et al., 2001)에서는 토양 1 g에 0.1 M (NH4)2HPO4 용액 25 mL를 넣고 2시간 진탕 후 여과하여 측정하였다. 모든 침출법에서 사용된 여과지는 Whatman No. 42이고, 여과된 추출액은 ICP-OES (8300DV, Perkin Elmer, USA)를 이용한 비소농도 측정이전까지 4°C 이하에서 냉장보관하였다.
식물체 분석 식물체는 각 작물의 가식부 수확시기에 맞춰 3종 작물 (고추, 벼, 콩)의 가식부를 모두 수확하여 분석에 이용하였다. 고추는 수돗물과 증류수로 씻고, 70°C 오븐에서 1주일 동안 건조 후 분쇄하여 분석용 시료로 이용하였으며, 수분함량 측정을 위해 시료 건조 전과 후에 식물체 무게를 측정하였다. 콩과 벼 (백미)는 상온에서 일주일간 자연건조 후 분쇄하여 식물체 분석을 실시하였다. 식물체 비소 햠량은 식물체 시료 0.5 g과 진한 HNO3 10 mL를 분해관에 넣고 블록분해기 (OD-98-001, ODLAB, Korea)를 이용하여 완전히 분해한 후 Whatman No. 42 여과지로 여과하여 ICP-OES (8300DV, Perkin Elmer, USA)로 측정하였다.
데이터 분석 본 연구에서는 통계적 차이 및 상관관계를 알아보기 위해 Minitab 16 software (Minitab Inc., State College, Pennsylvania, USA)를 이용하였다. 서로 다른 처리 (무처리, 석회 처리, 석회 및 퇴비 처리)에 따라 작물 가식부 중 비소농도, 토양 중 전함량 및 유효태 비소 농도, 그리고 토양 특성 (pH, EC, 및 DOC)이 어떻게 영향을 받았는지 알아보기 위해 One-way ANOVA Fisher’s LSD (Least-Significant-Difference) 분석을 수행하였다 (n = 20; p < 0.05). 또한, 작물 가식부 중 비소농도, 토양 이화학성, 토양 중 전함량 및 각각의 유효태 비소 농도간 어떠한 연관성이 있는지 알아보기 위해 상관관계 분석 (correlation coefficient)를 수행하였다.
Results and Discussion
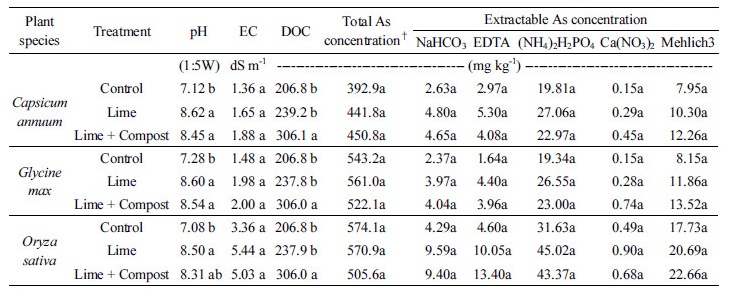
폐광산 주변 농경지 20 지점 토양의 이화학적 특성은 Table 1과 같다. 채취된 토양의 산성도는 pH 3.4에서 pH 8.0 사이에 고르게 분포하였다. 토양 pH 평균값은 6.4로 우리나라 농경지 평균인 pH 5.9보다 높았다 (Kang et al., 2012). 채취된 토양 중 유기물 함량은 평균 4.9% (2.9~13.9)이고, 모든 토양에서 국내 농경지 토양의 평균 (2.6%)보다 많은 유기물 함량이 측정되었다 (Kang et al., 2012). 채취된 토양 중 총 비소 농도의 평균은 361.6 mg kg-1으로 최대 2657.3 mg kg-1에서 최소 3.4 mg kg-1로 지역에 따라 매우 큰 차이를 보였다. 특히, 20지점 중 토양환경보전법상 토양오염 우려기준 (1지역: 25 mg kg-1)을 초과한 지역이 15지점, 그리고 이 중 대책기준 (1지역: 75 mg kg-1)을 초과한 지역이 11지점으로 많은 농경지가 광산으로부터 유출된 비소로 인해 심각하게 오염되었음을 확인할 수 있었다. 총 비소농도의 분포로 볼 때 본 연구에서 선정한 광산주변 농경지 20 지점의 토양은 토양 중 비소농도와 식물체에 흡수된 비소농도간의 상관관계를 밝히는데 적합한 것으로 판단되었다. 또한, 채취된 토양의 다양한 pH와 유기물 함량 분포는 식물의 재배기간 동안 석회 및 석회+퇴비 처리가 각 침출법의 비소 유효태 농도에 영향에 대한 추가적인 연구를 가능하게 하였다.
작물별 가식부에 축적된 비소농도를 Fig. 2에 나타내었다. 고추의 처리별 가식부 비소 농도는 무처리가 0.45 mg kg-1, 석회처리가 0.39 mg kg-1, 그리고 석회와 퇴비를 처리한 처리구가 0.51 mg kg-1로 퇴비를 처리한 처리구의 비소농도가 높게 나타났으나 각 처리에 따른 통계적 유의성은 없었다 (p > 0.05). 콩과 벼 역시 처리구별 가식부 비소농도는 각각 무처리가 0.74 mg kg-1, 0.41 mg kg-1, 석회처리 0.74 mg kg-1, 0.39 mg kg-1, 석회와 퇴비를 처리한 처리구가 0.95 mg kg-1, 0.76 mg kg-1으로 고추와 마찬가지로 퇴비를 처리한 처리구에서 평균 농도가 높게 나타났으나 각 처리에 따른 통계적 유의성은 없었다 (p > 0.05). 작물별 가식부 비소 농도는 콩 (0.84 mg kg-1)에서 가장 높고, 벼 (0.53 mg kg-1), 고추 (0.47 mg kg-1) 순이었으나, 통계적 유의성은 없는 것으로 나타났다 (p > 0.05). 벼의 비소 농도를 벼 (백미)의 식품공전 비소 기준 (0.2 mg kg-1)과 비교해보면 벼는 7개의 처리구를 제외하고 전부 높게 나타났다. 직접적인 비교는 어렵지만 동일한 기준을 고추와 콩에 적용한 결과 고추는 11개, 콩은 7개의 처리구를 제외하고 대부분이 기준치를 초과하는 것으로 나타났다. 비슷한 연구 사례로, Yoon et al. (2015)은 비소 오염토양에서 12가지 작물을 재배 후 이들의 가식부 중 비소농도를 비교한 결과, 콩, 벼, 그리고 고추 순으로 비소가 많이 검출되었다. 또한, 작물별 중금속 전이계수를 연구한 Kim et al. (2012)의 결과에서도 콩에서 벼 (백미)보다 높은 비소농도가 측정되었다. 본 연구 및 Yoon et al. (2015) 연구결과에서, 다른 작물보다 고추 가식부에서 상대적으로 낮은 비소농도가 측정된 것은 작물별 가식부 비소농도 계산 시 식물체 기준무게를 생체중으로 설정하였기 때문에 상대적으로 수분함량이 많은 고추열매에서 낮게 검출된 것으로 판단할 수 있다.
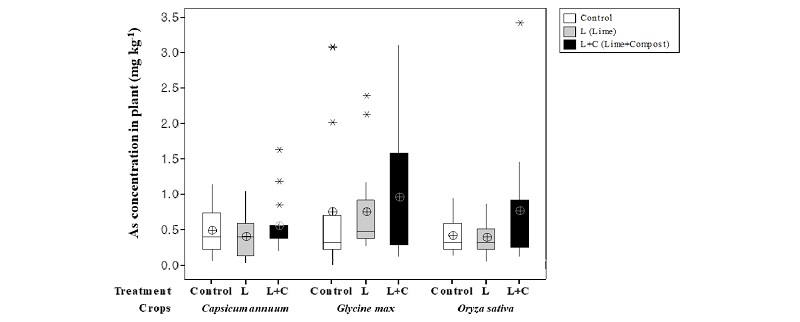
Fig. 2.
As concentration in edible part of Capsicum annuum (pepper), Glycine max (soybean), and Oryza sativa (polished rice) after 3 month greenhouse experiment. Each crop was cultivated in three different substrates such as bulk (n = 20), lime-amended (n = 20), and lime plus compost-amended (n = 20) soil.
작물 수확 후 각 토양에 대한 pH와 EC, DOC, 전함량 및 유효태 비소 농도 분포를 살펴본 결과는 Table 2와 같다. 각 작물별 토양의 pH는 석회처리에 따라 증가하였으나 EC는 변화가 없었다. DOC는 퇴비를 처리한 처리구에서 무처리구와 석회처리구보다 높게 나타나 퇴비로 인해 DOC가 증가하였음을 알 수 있다. 전함량 및 유효태 중금속 역시 처리에 따른 통계적 유의성은 없었으나, 유효태 중금속은 평균값이 무처리구보다 석회나 석회와 퇴비를 처리한 처리구의 평균농도가 높게 나타났다. 각 유효태 침출법으로 침출한 비소 함량의 평균치를 비교했을 때 침출법에 따라 차이가 있었으며, 침출액의 비소 농도가 높은 침출법은 (NH4)2H2PO4 침출법이고, Mehlich 3, EDTA, NaHCO3, Ca(NO3)2 침출법 순으로 비소 농도가 낮아졌다. 침출법 중 (NH4)2H2PO4을 이용한 침출법이 가장 높은 비소 농도를 보인 것은 인산염 (phosphate)과 비산염 (arsenate)의 화학적 형태가 유사하고 토양 흡착에도 경쟁적이므로, 인산으로 인해 토양 중 비소 침출이 증가한 것으로 판단된다 (Kim et al., 2015; Woolson et al., 1971). 비소농도가 가장 낮았던 Ca(NO3)2 침출법에서는 고추, 벼, 콩을 재배한 총 180개 토양 중 42%에서 비소가 검출되지 않았다. 이것으로 보아 Ca(NO3)2 침출법은 비소 농도가 낮은 토양에 대한 유효태 분석에는 적합하지 않은 분석법으로 판단된다. 다양한 침출법으로 토양 중 비소를 분석했던 Johnston and Barnard (1979)의 결과에서도 (NH4)2H2PO4 침출법이 Ca(NO3)2, NaHCO4, NH4F 등 다른 중성염 혹은 산 침출방법보다 비소 침출효과가 높은 것으로 보고되었다. 중성염과 산이 아닌 EDTA와 Mehlich 3 침출법은 중간 정도의 수치를 나타냈으며, 분포범위도 넓어서 식물과 유효태 비소와의 관계를 설명하기에 적합한 것으로 판단된다. EDTA로 침출한 비소의 농도가 다른 중성염 침출 비소농도보다 높게 나타난 것은 Oh et al. (2015)의 결과에서도 확인할 수 있었다. 본 연구결과에서 Mehlich 3 침출법이 EDTA나 다른 중성염 침출법보다 비소 농도가 높게 나온 것은 Mehlich 3 침출법이 토양 중 다양한 성분들을 한 번에 침출하여 분석하기 위해 개발된 침출법으로 0.2 N acetic acid와 0.25 N NH4NO3, 0.015 N NH4F, 0.013 N HNO3, 0.001 M EDTA으로 구성된 복합 침출액이라 농도가 높게 나타난 것으로 보인다 (Mehlich, 1984).
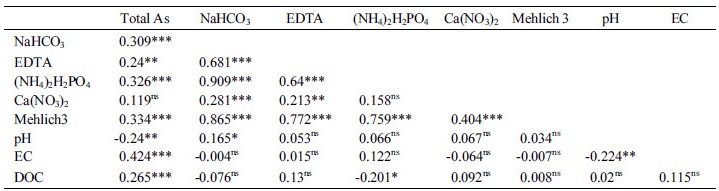
토양의 pH와 EC, DOC, 전함량 중금속, 유효태 중금속 그리고 식물체 가식부 비소농도간의 상관관계를 살펴본 결과는 Table 3과 같다. 식물체 비소 농도는 pH와 EC, DOC, 전함량 중금속과 상관관계가 없는 것으로 나타났고, Ca(NO3)2를 제외한 모든 유효태 비소와 고도로 유의한 상관관계가 있었다 (p < 0.01). 토양 특성인 토양 pH, EC, DOC는 토양의 전함량 비소와 유의한 상관관계가 있는 것으로 나타났지만, 작물별 재배토양의 토양특성과 전함량 비소 농도는 상관관계가 보이지 않았다. 유효태 비소도 토양 특성과 상관관계가 없는 것으로 나타났다 (p > 0.05). 토양 중 전함량 비소와 유효태 비소농도는 Ca(NO3)2을 제외하고 모두 고도로 유의한 상관관계에 있음을 보였다. 이는 Oh et al. (2015)과 Song (2011)이 보고한 토양의 전함량 비소와 추출태 비소간의 상관관계가 유의성이 없다는 것과 반대의 결과로 본 연구에서 사용한 토양의 전함량 농도 범위 (3.39~2657.27 mg kg-1)가 Oh et al. (2015) (4.22~536.2 mg kg-1)과 Song (2011) (2.63~52.77 mg kg-1)보다 넓어 이에 따른 결과로 판단된다. 유효태 비소간의 상관관계는 Ca(NO3)2와 (NH4)2H2PO4간의 상관관계 (p > 0.05)를 제외하고 모두 고도로 유의한 상관관계가 있었다 (p < 0.01). 토양 특성과 유효태 비소농도간의 상관관계는 pH-NaHCO3 (p < 0.05)와 DOC-(NH4)2H2PO4 (p < 0.05)를 제외하고 모두 유의성이 없는 것으로 나타나 단일 토양 특성과 유효태 비소간의 상관관계는 없는 것으로 판단된다.
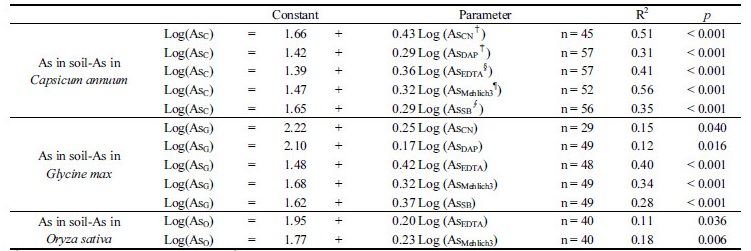
Table 4에 각 작물의 가식부 비소함량과 토양 중 유효태 비소 분석법으로 추출한 비소 농도 분석결과로 선형회귀분석을 실시한 결과를 나타내었다. 고추를 재배한 토양에서는 모든 침출법으로 분석한 유효태 비소 농도와 식물체 비소농도간에 고도로 유의한 상관성 (p < 0.001)이 있었다. 식물체 비소농도와 상관성이 가장 높은 침출법은 Mehlich 3 (R2: 0.56)였고, 이어서 Ca(NO3)2 (R2: 0.51), EDTA (R2: 0.41), NaHCO3 (R2: 0.35), (NH4)2H2PO4 (R2: 0.31) 순으로 상관성이 감소하였다. 콩 재배토양은 EDTA (R2: 0.40), Mehlich 3 (R2: 0.34), NaHCO3 (R2: 0.28) 순으로 고도로 유의한 상관성 (p < 0.001)이 있는 것으로 나타났고, 벼 재배토양은 Mehlich 3 (R2: 0.18, p: 0.006)와 ETDA (R2: 0.11, p: 0.036)가 유의한 상관관계가 있는 것으로 밝혀졌으나 R2값이 다른 작물보다 낮게 나와 상관성이 고추나 벼보다는 낮은 것으로 나왔다. 본 연구에서 본 유효태 비소농도와 식물체 비소농도간에는 농작물과 토양 비소 추출법간의 상관성이 없다고 보고한 Oh et al. (2015)의 결과와 달리 유의한 상관성이 있었다. 이는 유효태 비소농도와 다양한 작물 82점 전체 비소농도 간의 상관관계를 보고한 Oh et al. (2015)의 연구와 달리 본 연구에서는 세 가지 작물별 상관관계를 분석하였기 때문인 것으로 판단된다. 토양 중 유효태 비소농도와 세 가지 작물의 비소 농도 간 상관관계가 차이 나는 이유는 작물별 비소의 흡수형태는 다양하며, 가식부의 경우 식물체 내에서 흡수 이동형태에서 따라 작물별로 전이되는 양상이 현격하게 다르기 때문이다 (Kim et al., 2012; Klocke et al., 1984). 총 비소 함량과 가식부 비소와의 관계를 살펴본 결과에서도 고추재배 토양에서만 상관관계 (R2: 0.09, p < 0.001)가 있는 것으로 나타났고, 콩과 벼 재배토양에서는 상관관계가 없는 것으로 나타났다. 그러나 상관관계가 있는 고추재배 토양에서도 R2이 0.09로 낮아 전체적으로 토양 중 총 비소와 가식부 비소간의 관계가 다른 유효태 비소와의 관계보다 상관성이 낮은 것으로 볼 수 있으며, 이는 현재 토양 중 비소 관리 형태인 총 비소로의 토양 관리보다는 유효태 비소 기반의 토양관리가 안전한 작물 재배에 있어서 더 중요하다는 점을 나타내는 것으로 판단된다.
Conclusions
식물 유효도 기반 비소 오염토양 관리방안을 마련하기 위해서는 토양 중 비소의 유효태 침출법을 선정하는 것이 중요하다. 또한, 작물에 따라 비소 흡수 형태가 다를 수 있으므로 작물별 토양 중 식물 유효태 비소와 가식부 비소 농도의 상관관계를 검토하는 것이 필요하다. 따라서 본 연구에서는 비소 오염 농경지 토양에 고추, 벼, 콩을 재배하여 토양의 식물 유효태 비소와 작물의 가식부 비소를 분석하고, 이들간의 상관관계를 밝혀 식물유효도에 근거한 비소 추출법을 비교하였다. 식물체 분석결과 콩이 고추와 벼 (백미) 보다 높게 나타났고, 백미의 식품공전 기준인 2 mg kg-1을 초과하는 시료가 콩과 벼에서 일부 검출되었다. 재배토양의 유효태 비소 분석결과 (NH4)2H2PO4 침출법이 비소농도가 가장 높게 나타났고, 그 다음부터는 Mehlich 3, EDTA, NaHCO3, Ca(NO3)2 순으로 나타났다. 이 분석결과를 바탕으로 식물체 비소와 유효태 비소의 상관관계를 분석한 결과 EDTA와 Mehlich 3 침출법이 고추, 벼, 콩 모두 유의성을 나타냈고, 고추를 재배한 토양은 모든 침출법이 유의성이 있는 것으로 나타났다. 본 연구를 통해 EDTA와 Mehlich 3 침출법이 다양한 작물에 사용하기 적합한 토양 중 비소 침출법인 것으로 판단되므로 추후 이 방법의 근채류나 엽채류에 대한 적용여부를 검토해야 할 것이다. 그리고 상관관계 분석을 통해 얻어진 회귀식은 작물의 가식부 내 비소 농도를 예측하는 모델식으로 활용될 수 있을 것이다.