Effects of soil chemical properties on inorganic and organic carbon contents in organic, calcareous, and reclaimed-tidal soils
© 2025 The Korean Society of Soil Science and Fertilizer
ABSTRACT
Introduction
Materials and Methods
지형, 모재 및 토양 특성
토양 이화학성 분석
통계 분석
Results and Discussion
토양 탄소
토양 pH와 양이온 및 양이온치환용량
SOC와 SIC 함량 특성
토양 탄소 함량과 화학성과의 상관 특성
Conclusions
Introduction
지구의 탄소 (C)는 서로 연결된 5개의 영역 (대기권, 생물권, 토양권, 수권, 암석권)에서 순환한다 (Kim et al., 2006). 토양권 (pedosphere)은 암석권 (lithosphere)과 수권 (hydrosphere) 다음으로 가장 큰 탄소 저장고이며, 토양이 보유할 수 있는 탄소량은 생물권 (biosphere)과 대기권 (atmosphere)이 보유할 수 있는 탄소의 함량을 합친 것의 약 2배이다. 육지생태계에서 토양 탄소는 지구 탄소 순환과 기후 변화에서 중요한 역할을 한다 (Johnston et al., 2004).
토양 탄소 (total carbon, T-C)는 62%의 토양 유기 탄소 (soil organic carbon, SOC)와 38%의 토양 무기 탄소 (soil inorganic carbon, SIC)로 구성되어 있다 (Lal, 2004). SOC는 습한 지역과 반습한 지역에 많이 축적되며, SIC는 건조 및 반건조 지역 (연 강수량이 500 mm 이하인 지역)에 주로 분포한다 (Lal, 2016). SOC와 SIC 함량은 토양 특성과 농경지 관리에 따라 달라진다 (An et al., 2019; Park et al., 2023). 유기 농경지는 관행 농경지보다 SOC 함량이 많다고 알려져 있는데 (Kim et al., 2023), 이는 유기질 비료 (유박이나 가축분퇴비)를 이용한 양분 관리와 최소경운 및 윤작 등으로 SOC 함량이 증가하게 된다 (Bhattacharyya et al., 2022). 석회질 토양은 무기 탄소 형태인 탄산칼슘 (CaCO3)이 15% 이상을 차지하므로 SIC 함량이 높다 (Bontpart et al., 2024). 반면에 탄산염이 침전되면서 토양 미생물의 서식 공간이 감소되어 상대적으로 SOC가 저장되는 것이 저해될 수 있다 (Hu et al., 2021). 간척지 토양은 높은 pH 및 염분 집적으로 식물의 생육 저해와 토양에 환원되는 유기물 함량이 적어서 SOC 함량이 일반적으로 낮다 (Zhang et al., 2016). 또한 토양이 알칼리성일 때, 용존 유기 탄소 (dissolved organic carbon)의 침출 및 유기 탄소와 점토가 결합된 화합물을 제한하기 때문에 표토의 유기 탄소가 손실되는 결과를 초래하지만 (Andersson and Nilsson, 2001; Vermeer et al., 1998; Abate and Masini, 2003), SIC 함량은 CaCO3와 Ca(H2CO3)2로 인해 높은 수준을 보인다 (Zhang et al., 2019).
SIC는 토양에서 탄산 (H2CO3), 중탄산 이온 (HCO3-) 및 탄산 이온 (CO32-)이 금속 양이온 (M+, M2+)과 결합한 탄산염광물 형태 (MCO3, MHCO3)로 존재한다고 알려져 있다 (Batool et al., 2024). 일반적으로 탄산염광물은 석회암 모재에서 유래되거나 다양한 토양 pH 범위에서 물 (H2O)과 이산화탄소 (CO2)의 순차적 반응으로 2차 탄산염의 침전으로 형성된다. 이렇게 생성된 무기 탄소는 연간 토양 깊이 1.6 m에 0.12 - 0.38 Mg C ha-1 정도가 저장되므로 토양 탄소격리에 중요한 역할을 한다는 결과가 보고되었다 (Lal, 2016; Raza et al., 2021).
IPCC (Intergovernmental Panel on Climate Change) 가이드라인은 모든 토지 이용 부문에 적용할 수 있는 토지 이용 및 관리 방법별 토양 CO2 배출량과 흡수량의 산정방법론을 제공하고 있다 (Solomon et al., 2007). LULUCF (land use, land use change and forestry)의 농경지 부문에서 토양 탄소 축적량은 토양 표면 잔재물 (식물잔사 등)과 토양 유기 탄소를 포함하지만, 앞서 언급했듯이, 토양 유기 탄소와 무기 탄소의 함량은 6 : 4의 비율로 탄산염광물로 저장되는 토양 무기 탄소 축적량을 간과할 수 없다. 더구나, 석회암 유래 토양과 하해혼성 또는 해성 토양인 간척지는 국토 면적의 10% 이상을 차지하므로 잠재적인 토양 탄소 축적량으로 고려할 만하다. 그럼에도 불구하고, 국내 토양 탄소 축적에 관한 연구는 주로 유기 탄소이며, 무기 탄소에 관한 연구는 전무한 실정이다. 따라서, 본 연구는 작물이 재배되고 있는 유기 농경지와 석회질 및 간척지 토양에서 SOC와 SIC 함량을 비교 평가하고 SOC와 SIC 함량에 영향을 미치는 토양 화학성 인자를 상관 분석을 통해 규명하고자 한다.
Materials and Methods
지형, 모재 및 토양 특성
유기 농경지, 석회암지대 및 간척지의 지형, 모재 및 토양 특성은 농촌진흥청의 흙토람 (http://soil.rda.go.kr)을 이용하여 조사하였다. 유기 농경지로 사용되고 있는 토양의 지형은 충적 평탄지 (alluvial plain), 구릉지 (hilly zone), 해성평탄지 (marine plains), 산록경사지 (mountain foot slopes), 곡간지 (valleys)였으며, 모재는 충적층 (alluvium), 화강암 (granite), 하해혼성 충적층 (fluvio - marine deposit)이었다. 토양목 (soil order)은 4개이며 토양통 (soil series)은 12개로 분류되었다. 토성은 사양토에서 양토까지 다양했다 (Table 1).
Table 1.
Description of soil sampling site in organic farming soils.
|
Address
|
Crop
|
Topography
|
Parent material
|
Soil order
|
Soil series
|
Soil texture
|
|
219-11, Dori-ri, Daewol-myeon, Icheon-si
|
Ginger
|
Mountainous areas
|
Granite
|
Cambisols
|
SAMGAG
|
Loamy Sand
|
|
189, Samseong-ri, Namjong-myeon, Gwangju-si
|
Onion
|
Velleys
|
Alluvium
|
Anthrosols
|
WOLGOG
|
Sandy Loam
|
|
151-9, Samseong-ri, Namjong-myeon, Gwangju-si
|
Soybean
|
Velleys
|
Alluvium
|
Anthrosols
|
WOLGOG
|
Sandy Loam
|
|
270-11, Hogok-ri, Ujeong-eup, Hwaseong-si
|
Sudan grass
|
Hilly zone
|
Granite
|
Alisols
|
SONGJEONG
|
Sandy Loam
|
|
270-17, Hogok-ri, Ujeong-eup, Hwaseong-si
|
Sudan grass
|
Hilly zone
|
Granite
|
Alisols
|
SONGJEONG
|
Loam
|
|
San 20-4, Hogok-ri, Ujeong-eup, Hwaseong-si
|
Sudan grass
|
Hilly zone
|
Granite
|
Cambisols
|
YESAN
|
Sandy Loam
|
|
San17-8, Hogok-ri, Ujeong-eup, Hwaseong-si
|
Perilla
|
Hilly zone
|
Granite
|
Cambisols
|
YESAN
|
Sandy Loam
|
|
317-3, Baegu-ri, Baeksa-myeon, Icheon-si
|
Perilla
|
Velleys
|
Alluvium
|
Cambisols
|
SANGJU
|
Sandy Loam
|
|
363-4, Songchon-ri, Joan-myeon, Namyangju-si
|
Onion
|
Alluvial plain
|
Alluvium
|
Fluvisols
|
JUNGDONG
|
Sandy Loam
|
|
347, Songchon-ri, Joan-myeon, Namyangju-si
|
Onion
|
Alluvial plain
|
Alluvium
|
Fluvisols
|
JUNGDONG
|
Silt Loam
|
|
327, Songchon-ri, Joan-myeon, Namyangju-si
|
Onion
|
Alluvial plain
|
Alluvium
|
Fluvisols
|
JUNGDONG
|
Sandy Loam
|
|
324-1, Songchon-ri, Joan-myeon, Namyangju-si
|
Garland chrysanthemum
|
Alluvial plain
|
Alluvium
|
Fluvisols
|
JUNGDONG
|
Sandy Loam
|
|
579, Songchon-ri, Joan-myeon, Namyangju-si
|
Pumpkin
|
Mountain foot slope
|
Granite
|
Anthrosols
|
CHILGOG
|
Sandy Loam
|
|
33-9, Jinjung-ri, Joan-myeon, Namyangju-si
|
Pumpkin
|
Mountain foot slope
|
Granite
|
Alisols
|
ANRYONG
|
Sandy Loam
|
|
166-1, Jinjung-ri, Joan-myeon, Namyangju-si
|
Perilla
|
Mountain foot slope
|
Granite
|
Anthrosols
|
CHILGOG
|
Sandy Loam
|
|
771, Joan-ri, Joan-myeon, Namyangju-si
|
Potato
|
Velleys
|
Alluvium
|
Anthrosols
|
WOLGOG
|
Silt Loam
|
|
260, Gaekhyeon-ri, Jeokseong-myeon, Paju-si
|
Potato
|
-
|
-
|
-
|
-
|
Sandy Loam
|
|
283-2, Sin-ri, Oseong-myeon, Pyeongtaek-si
|
Rape
|
Marine plains
|
Fluvio-marine deposits
|
Anthrosols
|
MANGYEONG
|
Silt
|
|
246-2, Buyong-ri, Yangseo-myeon, Yangpyeong-si
|
Red pepper
|
Velleys
|
Alluvium
|
Anthrosols
|
SUBUG
|
Loamy Sand
|
|
494-6, Buyong-ri, Yangseo-myeon, Yangpyeong-si
|
Schisandra
|
Velleys
|
Alluvium
|
Anthrosols
|
WOLGOG
|
Sandy Loam
|
|
141, Unsim-ri, Gangha-myeon, Yangpyeong-si
|
Potato
|
Velleys
|
Granite
|
Anthrosols
|
SACHON
|
Sand
|
|
250-89, Wondeok-ri, Yangpyeong-eup, Yangpyeong-si
|
Green onion
|
Alluvial plain
|
Alluvium
|
Anthrosols
|
GANGSEO
|
Sandy Loam
|
|
87-4, Samseong-ri, Yongmun-myeon, Yangpyeong-si
|
Rape
|
Mountain foot slope
|
Granite
|
Alisols
|
ANRYONG
|
Sandy Loam
|
|
615, Sinwon-ri, Pogok-eup, Cheoin-gu, Yongin-si
|
Sudan grass
|
Velleys
|
Granite
|
Anthrosols
|
MAEGOG
|
Loamy Sand
|
관행 농경지로 사용되고 있는 석회질 토양은 산악지 (mountainous areas), 산록경사지, 곡간지에 위치한다. 모재는 모두 석회암이었다. 토양목은 5개이며 토양통은 9개로 분류되었다. 토성은 미사질양토에서 식양토까지 다양하였다 (Table 2).
Table 2.
Description of soil sampling site in calcareous soils.
|
Address
|
Crop
|
Topography
|
Parent material
|
Soil order
|
Soil series
|
Soil texture
|
|
Jangnim-ri, Daegang-myeon, Danyang
|
Soybean
|
Mountain foot slopes
|
Limestone
|
Luvisols
|
PYEONGAN
|
Clay loam
|
|
Dueum-ri, Daegang-myeon, Danyang
|
Garlic
|
Mountain foot slopes
|
Limestone
|
Luvisols
|
PYEONGAN
|
Clay loam
|
|
Hasi-ri, Maepo-eup, Danyang
|
Rice
|
Velleys
|
Limestone
|
Anthrosols
|
YULGOG
|
Silt loam
|
|
Hasi-ri, Maepo-eup, Danyang
|
Rice
|
Mountain foot slopes
|
Limestone
|
Anthrosols
|
OGGYE
|
Loam
|
|
Hasi-ri, Maepo-eup, Danyang
|
Rice
|
Velleys
|
Limestone
|
Anthrosols
|
YULGOG
|
Silt loam
|
|
Hasi-ri, Maepo-eup, Danyang
|
Rice
|
Mountain foot slopes
|
Limestone
|
Anthrosols
|
OGGYE
|
Loam
|
|
Hasi-ri, Maepo-eup, Danyang
|
Rice
|
Velleys
|
Limestone
|
Anthrosols
|
YULGOG
|
Silt loam
|
|
Hasi-ri, Maepo-eup, Danyang
|
Garlic
|
Mountain foot slopes
|
Limestone
|
Luvisols
|
PYEONGJEON
|
Loam
|
|
Yeongcheon-ri, Maepo-eup, Danyang
|
Chinese cabbage
|
Mountain foot slopes
|
Limestone
|
Luvisols
|
PYEONGAN
|
Clay loam
|
|
Yeongcheon-ri, Maepo-eup, Danyang
|
Soybean
|
Mountainous areas
|
Limestone
|
Luvisols
|
PYEONGCHANG
|
Clay loam
|
|
Yeongcheon-ri, Maepo-eup, Danyang
|
Garlic
|
Mountain foot slopes
|
Limestone
|
Luvisols
|
PYEONGJEON
|
Loam
|
|
Sangsi-ri, Maepo-eup, Danyang
|
Rice
|
Mountain foot slopes
|
Limestone
|
Anthrosols
|
OGGYE
|
Loam
|
|
Sangsi-ri, Maepo-eup, Danyang
|
Garlic
|
Mountain foot slopes
|
Limestone
|
Haplic Phaozems
|
MITAN
|
Loam
|
|
Yeongcheon-ri, Maepo-eup, Danyang
|
Corn
|
Mountain foot slopes
|
Limestone
|
Luvisols
|
PYEONGAN
|
Clay loam
|
|
Yeongcheon-ri, Maepo-eup, Danyang
|
Garlic
|
Mountainous areas
|
Limestone
|
Cambisols
|
JANGSEONG
|
Silty clay loam
|
|
Sangsi-ri, Maepo-eup, Danyang
|
Red pepper
|
Mountain foot slopes
|
Limestone
|
Luvisols
|
PYEONGAN
|
Clay loam
|
|
Andong-ri, Maepo-eup, Danyang
|
Rice
|
Velleys
|
Limestone
|
Anthrosols
|
YULGOG
|
Silt loam
|
|
Yeongcheon-ri, Maepo-eup, Danyang
|
Garlic
|
Mountain foot slopes
|
Limestone
|
Luvisols
|
PYEONGJEON
|
Loam
|
|
Andong-ri, Maepo-eup, Danyang
|
Rice
|
Mountainous areas
|
Limestone
|
Luvisols
|
MOSAN
|
Clay loam
|
|
Andong-ri, Maepo-eup, Danyang
|
Soybean
|
Mountainous areas
|
Limestone
|
Luvisols
|
PYEONGCHANG
|
Clay loam
|
|
Andong-ri, Maepo-eup, Danyang
|
Garlic
|
Mountain foot slopes
|
Limestone
|
Haplic Phaozems
|
MITAN
|
Loam
|
|
Dodam-ri, Danyang-eup, Danyang
|
Soybean
|
Mountainous areas
|
Limestone
|
Luvisols
|
PYEONGCHANG
|
Clay loam
|
|
Samgok-ri, Maepo-eup, Danyang
|
Rice
|
Velleys
|
Limestone
|
Anthrosols
|
YULGOG
|
Silt loam
|
|
Samgok-ri, Maepo-eup, Danyang
|
Soybean
|
Mountain foot slopes
|
Limestone
|
Alisols
|
ANMI
|
Loam
|
|
Samgok-ri, Maepo-eup, Danyang
|
Garlic
|
Mountain foot slopes
|
Limestone
|
Luvisols
|
PYEONGAN
|
Clay loam
|
간척지의 지형은 구릉지 (hilly zone)와 해성평탄지 (marine plains)였다. 모재는 충적층과 화강암이었다. 토양목과 토양통은 모두 2개였다 (Table 3).
토양목과 토양통은 FAO/WRB (Food and Agriculture Organization/World Reference Base)의 기준으로 분류하였다.
Table 3.
Description of soil sampling site in reclaimed tidal soils.
|
Address
|
Crop
|
Topography
|
Parent material
|
Soil order
|
Soil series
|
Soil texture
|
|
503-1, Yangsan-ri, Gyehwa-myeon, Buan-gun
|
Forage crop
|
-
|
-
|
-
|
-
|
-
|
|
1097-2, Changje-ri, Gwanghwal-myeon, Gimje-si
|
-
|
-
|
-
|
-
|
-
|
|
1097-2, Changje-ri, Gwanghwal-myeon, Gimje-si
|
-
|
-
|
-
|
-
|
-
|
|
1521, Daeseok-ri, Seongdeok-myeon, Gimje-si
|
Fluvio-marine plain
|
Alluvium
|
Anthrosol
|
JEONBUG
|
Silt loam
|
|
1097-2, Changje-ri, Gwanghwal-myeon, Gimje-si
|
-
|
-
|
-
|
-
|
-
|
|
1097-2, Changje-ri, Gwanghwal-myeon, Gimje-si
|
-
|
-
|
-
|
-
|
-
|
|
1097-2, Changje-ri, Gwanghwal-myeon, Gimje-si
|
-
|
-
|
-
|
-
|
-
|
|
Yangsan-ri, Gyehwa-myeon, Buan-gun
|
-
|
-
|
-
|
-
|
-
|
|
san 8-2, Myora-ri, Seongdeok-myeon, Gimje-si
|
Hilly area
|
Granite
|
Alisol
|
JEONNAM
|
Silty clay loam
|
토양 이화학성 분석
본 연구에 사용한 토양 시료는 총 58점으로 유기 농경지 24점 (밭 토양), 석회질 토양 25점 (논 토양 9점, 밭 토양 16점) 및 간척지 토양 9점 (밭 토양)이었다. 토양 시료는 2022년부터 2023년 사이에 토양 시료 채취기 (soil auger)를 사용하여 표토 (토심 15 cm)를 채취하였다. 유기 농경지는 3년 이상 유기농업 인증을 받은 농경지에서 토양을 채취하였고, 석회질 토양은 식량 작물과 소득 작물이 재배되고 있는 관행 농경지에서 채취하였다. 간척지 토양은 1991년부터 간척을 시작하여 2006년에 방조제가 완공된 새만금 간척지에서 채취하였으며, 사료작물이 재배되고 있는 농경지였다. 채취한 토양은 한경국립대학교 부속 농장에서 일주일간 풍건 후 2 mm 체로 자갈 및 협잡물을 제거한 후 토양 화학성 분석에 사용하였다.
토양의 화학적 특성은 농촌진흥청의 토양 및 식물체 분석법 (RDA, 2000)을 기준으로 분석하였다. 총 탄소 (T-C), 총 질소 (T-N) 및 SOC는 2 mm 체거름한 토양시료를 막자사발로 갈고 0.075 mm 체를 통과한 시료를 사용했다. T-C와 T-N는 900°C 온도 조건에서 원소 분석기 (Vario MAX CN, elementar, Germany)로 측정하였다. SOC 함량은 SIC를 토양 : 4N-HCl : 증류수 = 1 : 4 : 2의 비율로 혼합하여 4시간 동안 CO2를 제거한 후 Tyurin 법으로 분석하였다. SIC 함량은 T-C에서 SOC를 제외하여 산출하였다. pH는 1:5 H2O 법으로 pH meter (Orion STAR A214, Thermo Fisher Scientific, USA)를 이용하였다. 4대 양이온 (Exch. cations)은 1N NH4OAc (pH 7.0)으로 추출하여 ICP-OES (5800 ICP-OES, Agilent Technologies, USA)로 분석하였으며, 양이온치환용량 (CEC)은 간이 측정법을 이용하여 분석하였다. 토성은 비중계법으로 분석하였다. 모든 실험은 3 반복으로 수행하였다.
통계 분석
유기 농경지, 석회질 및 간척지 토양의 T-C와 SOC 및 SIC의 함량 차이와 토양 화학적 특성을 비교하기 위하여 ANOVA 및 Duncan의 다중 범위 사후 검정을 SAS (version 9.4, SAS Institute Inc. Cary, USA)를 활용하여 5% 유의 수준에서 평가하였다. 토양 화학적 인자와 유기 및 무기 탄소 함량과의 상관관계는 소프트웨어 Microsoft Excel Add-in (XLSTAT)을 사용하여 분석하였다.
Results and Discussion
토양 탄소
유기 농경지, 석회질 및 간척지 토양들의 평균 T-C 함량은 각각 2.09, 2.87, 및 0.81%로 분석되었으며 5% 유의 수준에서 차이를 보였다 (Fig. 1). 토양 유기 탄소 함량 (SOCC)은 유기 농경지, 석회질 및 간척지 토양에서 각각 1.98, 1.46 및 0.24%로 분석되었으며, 유기 농경지에서 가장 높고 석회질과 간척지 순으로 낮았다. T-N의 함량은 유기 농경지가 1.25%였으며, 석회질과 간척지 토양에서는 0.22%와 0.03%로 유기 농경지 토양보다 10배에서 40배 정도 낮았다.
토양 유기물은 C와 N을 골격으로 한 생분해성 또는 난분해성 유기화합물로 토양 비옥도의 척도를 나타내는 지표이다. 유기 농경지에서 T-C 함량이 석회질 토양보다 낮았지만, SOC와 T-N의 함량이 유의적으로 높게 나타났다 (Fig. 1). Kim et al. (2012)와 Lee et al. (2012)의 보고에 의하면, 유기 농경지 토양은 화학비료와 화학농약의 투입이 제한되는 농경지로 질소의 함량이 높고 탄질율이 낮은 유기물질을 시비함으로써 작물의 생산성을 유지하므로 상대적으로 높은 T-N 함량이 낮은 탄질율의 결과를 초래한다고 하였다. 반면에, 관행 농법이 적용되는 석회질 토양에서는 SOC와 T-N의 함량이 1.46%와 0.22%로 농촌진흥청에서 제시하고 있는 농경지의 적정범위 (SOC: 1.16 - 1.74%)에 있으며, 탄질율은 6.66이었다. 간척지 토양의 SOC와 T-N의 함량은 0.24%와 0.03%로 아주 척박한 토양으로 나타났으며, 탄질율은 7.35이었다. 간척지 토양은 염류 (예, 염분)의 과다 집적으로 인해 숙전화가 진행 중인 토양으로서 식량작물 또는 소득작물의 재배가 어려운 토양으로 평가된다 (Kim et al., 2022). 따라서, 간척지와 같은 염분이 집적되어 있는 토양은 C와 N의 함량이 낮았다 (Kim et al., 2011; Ko et al., 2014).
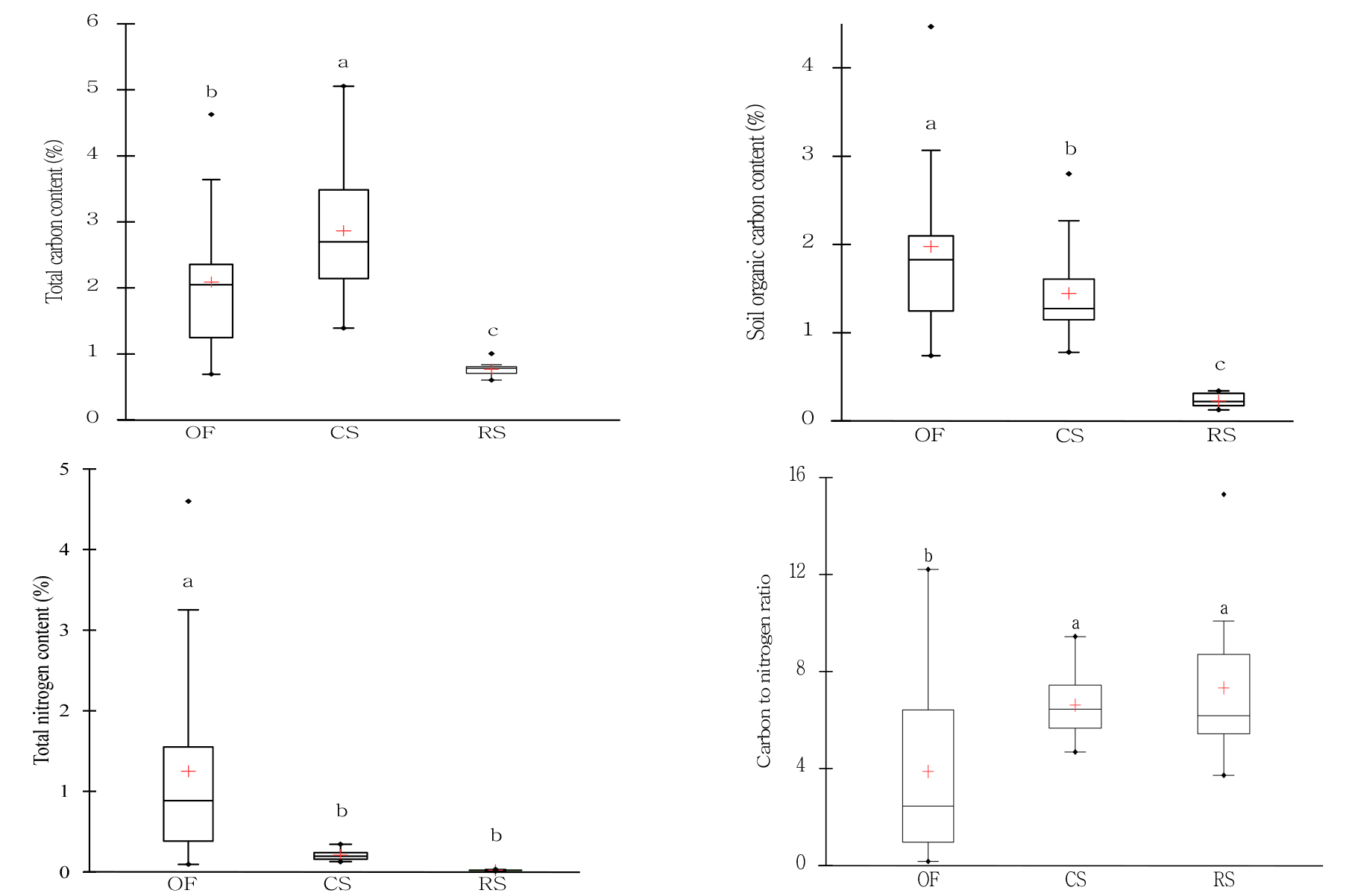
Fig. 1.
Total carbon, soil organic carbon, total nitrogen, and carbon to nitrogen (C/N) ratios in the soils. Statistical differences (P < 0.05) are indicated by different letters above the boxes. The boxes represent the interquartile range (IQR), spanning from the first quartile (Q1) to the third quartile (Q3), while the vertical lines within the boxes indicate median values. The "+" symbol represents the mean, while the "◆" symbol represents outliers. The upper and lower whiskers indicate the minimum and maximum values, excluding outliers.
토양 pH와 양이온 및 양이온치환용량
토양의 pH는 유기 농경지, 석회질 토양 및 간척지에서 각각 7.02, 8.01 및 7.72로 분석되어 중성과 약알칼리성으로 나타났다. 모든 토양에서 칼륨 (K+)과 마그네슘 (Mg2+) 이온의 농도는 유의적인 차이를 보이지 않았으나, 칼슘 (Ca2+) 이온의 농도는 석회질 토양 (12.6 cmolc kg-1)에서 가장 높았고 나트륨 (Na+) 이온의 농도는 간척지 토양에서 높았다. 유기 농경지는 유박이나 가축분 퇴비와 같은 유기질 비료의 시비로 인해 토양 pH, 양이온 (Ca2+, K+, Mg2+)의 함량 및 CEC가 높았는데, 이는 토양에 환원된 유기물의 무기화와 부식화에 기인한 것으로 사료된다. 선행 연구결과, Kim et al. (2000)은 유기물 공급원으로서 퇴비를 시용하면 시용년차와 시용량이 많을수록 토양 pH와 EC가 증가된다고 보고하였는데, 이는 유기물의 무기화 과정에서 토양에 공급되는 양이온 (Ca2+, K+, Mg2+)과 H+ 이온과의 교환 반응이 pH를 증가시키기 때문으로 사료된다 (Clark et al., 1998; Whalen et al., 2000).
석회암 유래 토양은 약 15% 이상이 탄산칼슘 (CaCO3)으로 구성되어 있어 Ca2+ 이온의 농도가 높다. 탄산칼슘 퇴적물로 인해 만들어진 토양은 배수가 불량해 토양의 pH가 7.5 - 8.5까지 높아진다 (Taalab et al., 2019). 반면, 우리나라 서 ‧ 남해안에 분포하는 간척지 토양 (예, 새만금 간척지)은 해수의 유입으로 심토에 염분 (NaCl)이 많이 집적된다. 결국, 해수에 의한 염분의 침투와 높은 증발량에 의한 모세관 현상은 표토의 Na+ 농도를 증가시킨다. 또한, 표토에 집적된 Na+는 점토의 분산과 수리 전도도를 감소시켜 토양의 pH를 약알칼리성 또는 알칼리성으로 증가시킨다 (Kim et al., 2011).
양이온치환용량 (CEC)은 유기 농경지 17.45 cmolc kg-1, 석회질 15.44 cmolc kg-1 및 간척지 6.07 cmolc kg-1으로 분석되었다. 우리나라 평균 토양의 CEC는 10 cmolc kg-1 인 것에 비해, 유기 농경지와 석회질 토양의 CEC는 높게 나타났다. Kim et al. (2023)의 연구 결과에서 유기 농경지가 관행 농경지보다 CEC가 높게 분석되었는데, 이는 가축분 퇴비와 같은 유기물을 토양에 시용하면 유기물의 부식화로 부식의 집적됨에 따라 CEC도 증가된다고 하였다 (Yao et al., 2007; Gil et al., 2008). 더구나, 석회질 토양에서 SIC 형태로 존재하는 탄산염광물도 CEC 증가에 영향을 미친다는 연구결과도 보고되었다 (Wang et al., 2005).
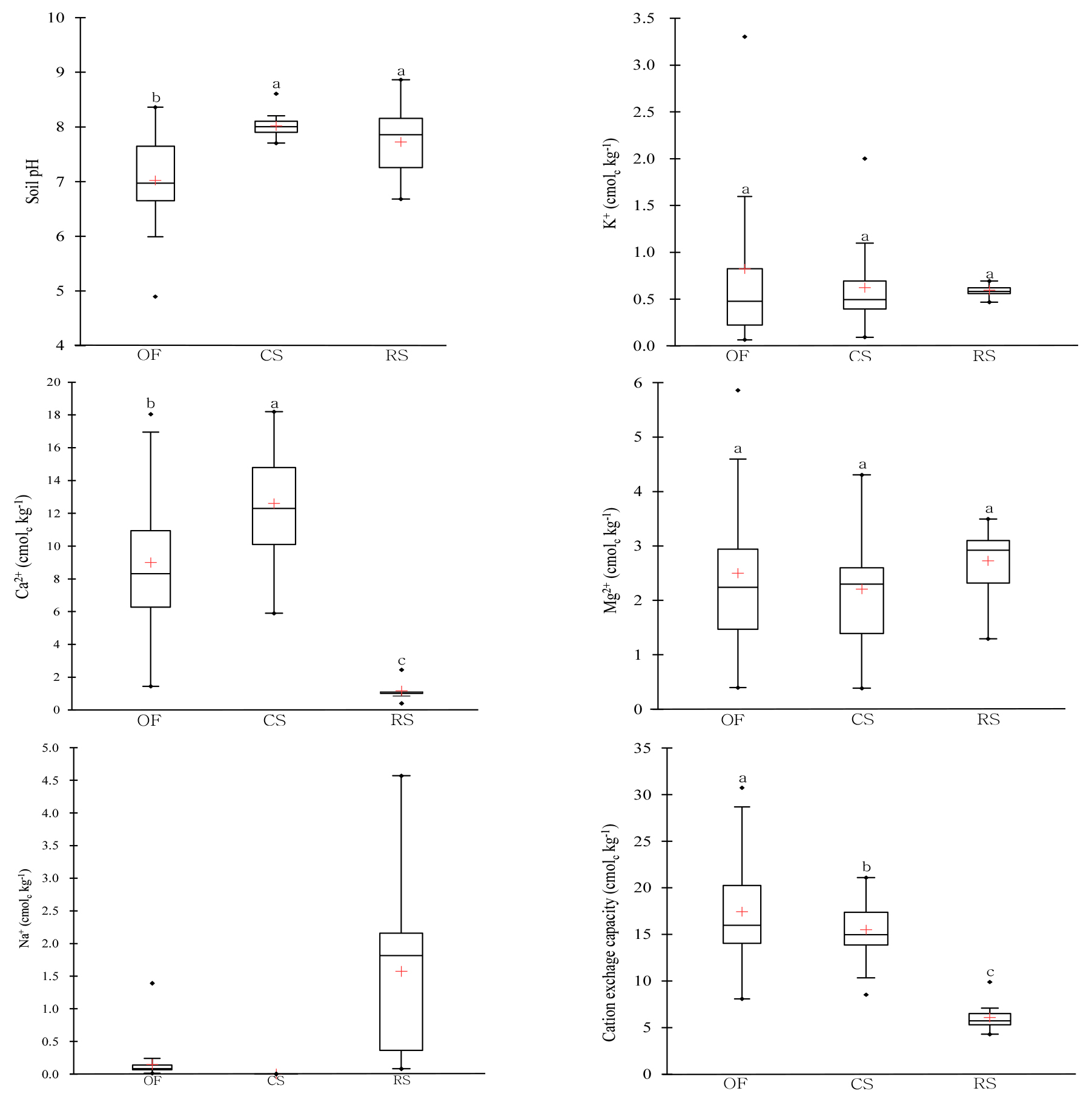
Fig. 2.
Box plot of soil chemical properties (pH, 4 exchangeable cations and CEC) in the organic farming soil (OF), calcareous soil (CS), and reclaimed tidal soil (RS). Statistical differences (P < 0.05) are indicated by different letters above the boxes. The boxes represent the interquartile range (IQR), spanning from the first quartile (Q1) to the third quartile (Q3), while the vertical lines within the boxes indicate median values. The "+" symbol represents the mean, while the "◆" symbol represents outliers. The upper and lower whiskers indicate the minimum and maximum values, excluding outliers.
SOC와 SIC 함량 특성
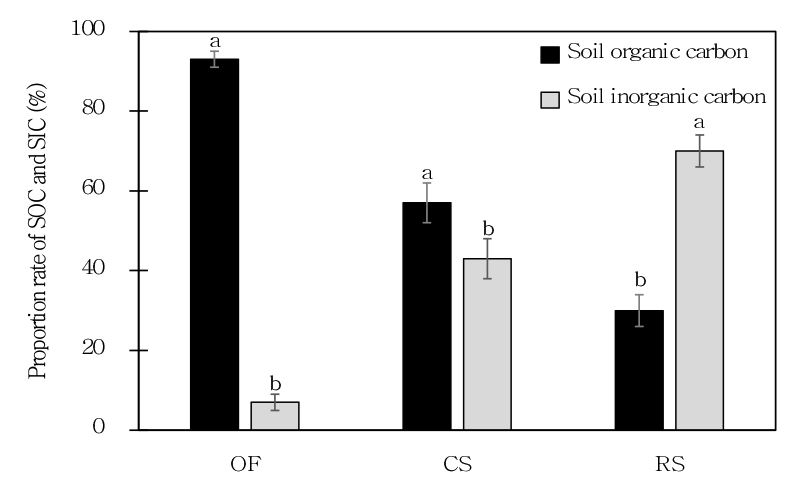
T-C 중 유기 탄소 함량 (SOCC)과 무기 탄소 함량 (SICC)의 비율은 유기 농경지에서 93%와 7%, 석회질 토양에서 57%와 43% 및 간척지 토양에서 30%와 70%로 나타났다 (Fig. 3).
농경지 토양의 SOCC은 주로 경작관리 방법 (유기물 투입량, 경운, 윤작, 물관리 등)과 미생물과 효소의 활성 등에 의해서 달라진다 (Belmonte et al., 2018). SICC은 토양의 모재와 2차 광물인 탄산염광물 (CaCO3, MgCO3)의 형성 과정에 따라 달라진다. 유기 농경지 토양의 모재는 화강암 (granite)과 충적 퇴적물 (alluvium)로 이루어져 있다. 일반적으로 화강암 유래 토양은 산성 토양으로 Ca2+나 K+의 함량이 적지만, 충적토는 유기 탄소의 농도가 다소 높은 특징을 나타낸다 (Boettinger, 2005). 유기 농경지는 화학비료 및 농약 사용이 제한되어 유기물질의 투입과 윤작 및 무경운 또는 최소경운으로 토양을 관리하기 때문에 토양 미생물 군집의 다양성 및 개체의 증가로 토양 탄소 대부분이 유기 탄소로 축적된다고 알려져 있다 (Bhattacharyya et al., 2022). 석회질 토양은 CO32-의 용해와 재침전으로 토양 공극이나 SOC 표면에 2차 탄산 이온 광물이 축적되어 난분해성 유기탄소 (mineral associated organic carbon, MOC)가 증가하지만, CO32-의 침전은 SOC가 축적되는 것을 저해할 수 있는데, 이는 탄산염의 침전으로 토양 미생물의 서식 공간이 감소하기 때문으로 밝혀졌다 (Hu et al., 2021). 앞서 언급했듯이, 석회암 유래 토양입자의 15% 이상이 탄산염광물 (CaCO3)로 존재한다 (Bontpart et al., 2024). 이는 높은 Ca2+의 함량이 SIC 함량 증가에 기여한다는 결과와 일치한다 (Taalab et al., 2019). 이로 인해, 석회질 토양의 SOCC와 SICC은 비슷한 수준을 나타내었다. 간척지 토양은 화강암 유래 토양의 객토와 조수의 작용으로 침식된 모재가 퇴적되어 이루어진 해성 충적토이다. 이러한 토양은 해수의 유입으로 가용성 염류와 치환성 나트륨이 과다하게 함유되어 있다 (Ryu et al., 2019). 염류 농도가 높은 토양은 가용성 알칼리금속 (K+, Na+)과 알칼리토금속 (Ca2+, Mg2+)의 영향으로 높은 pH를 보인다. 간척지 토양의 높은 pH와 탄산염 이온 (HCO3-, CO32-) 및 가용성 금속 양이온 (Na+, K+, Ca2+, Mg2+)은 탄산염의 용해 및 침전 등의 화학반응으로 높은 SICC를 나타내었다. 낮은 pH 조건 (pH < 6.35)의 토양에서 탄산염은 주로 H2CO3 형태로 존재하여 탄산염을 형성하는데 필요한 HCO3-, CO32- 이온이 충분히 존재하지 않는 반면, 높은 pH 조건 (pH > 6.35)의 토양에서는 탄산염 이온과 금속 2가 양이온 (M2+)과의 침전반응 ()으로 SICC가 증가한다고 알려져 있다 (Batool et al., 2024).
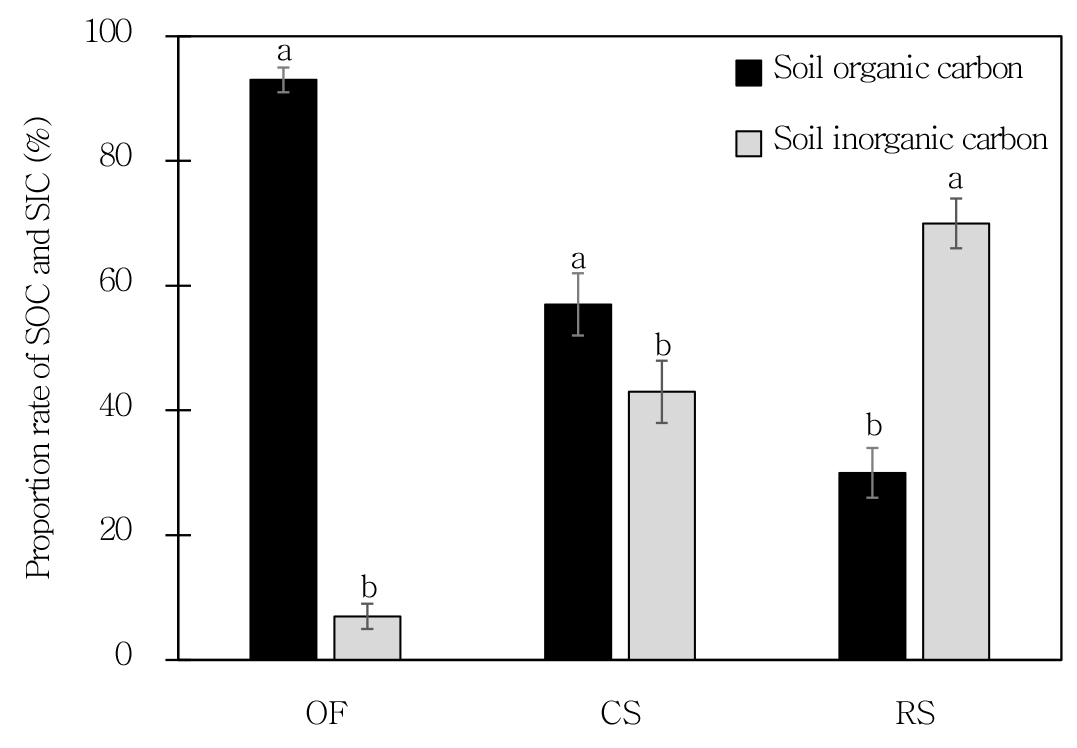
Fig. 3.
Proportion rate of soil organic and inorganic carbon contents in organic farming soils (OF), calcareous soils (CS), and reclaimed tidal soils (RS). Statistical differences (P < 0.05) are indicated by different letters above the boxes.
토양 탄소 함량과 화학성과의 상관 특성
유기 농경지 토양은 T-C 중 93%가 SOCC로 존재하므로 T-C와 SOCC가 높은 정의 상관관계를 보였다. SOCC는 Ca2+, K+, Mg2+ 및 CEC와 유의적으로 정의 상관관계; SICC는 CEC와 정의 상관관계를 나타냈다 (Table 4). 이러한 결과는 유기질 비료가 토양에 매년 시비됨으로써 SOC가 축적되고 미생물의 유기물 분해에 의한 무기 양분 공급에 의한 것으로 판단된다. 한편, 석회질 토양에서 T-C는 SICC 및 CEC와 정의 상관을 보였으나, SOCC와 통계적으로 상관관계가 없었다. 석회암지대에서는 토양의 발달 강도 (evolvement intensity)가 증가함에 따라 미생물 활성과 SOC 축적량이 감소한다는 연구 결과가 보고되었다 (Yang et al., 2021). 간척지 토양은 T-C의 함량이 0.81%로 토양비옥도가 상당히 척박한 토양으로 나타났으며, SOCC는 30%로 SICC (70%)보다 상당히 낮았다. 따라서, 간척지 토양의 T-C는 주로 SICC에 영향을 받는 것으로 분석되었다 (Table 6). 한편, SICC는 Mg2+과 정의 상관관계를 보였는데, 이는 알칼리성의 토양 pH (7.72) 조건에서 Mg2+ 이온이 토양 용액 중 탄산염 (CO32- 또는 HCO3-이온)과의 침전반응으로 증가한 결과로 사료된다. Guo et al. (2016)에 의하면, pH 8 부근 및 토양수분이 충분한 조건에서 SIC는 가용성 2가 양이온 (Ca2+ 또는 Mg2+)과 침전반응으로 MgCO3 또는 CaCO3을 생성한다고 하였다. 본 연구에 사용된 간척지 토양의 화학성 분석 결과에서 Ca2+ 농도는 1.18 cmolc kg-1으로 오히려 Mg2+의 농도 (2.73 cmolc kg-1) 보다 낮은 수준이었다. 따라서, 간척지 토양에서 SICC에 기여한 탄산염 광물의 침전반응은 으로 판단되어 MgCO3을 생성한 것으로 사료된다. 한편, Zhang et al. (2019)에 의하면, 매립된 기간이 길어질수록 SOC 함량이 증가하고 SIC 함량은 감소한다고 보고하였으며, 유기물 환원 등 농경지 관리에 의해 SOC 함량이 증가 될 수 있다고 보고하였다.
Table 4.
Correlation coefficient of the selected parameters for organic farming soils (n = 24).
|
Variables
|
T-C
|
SOCC |
SICC |
pH
|
Exch. Ca
|
Exch. K
|
Exch. Mg
|
Exch. Na
|
|
SOCC |
0.88***
| | | | | | | |
|
SICC |
0.56**
|
0.13
| | | | | | |
|
pH
|
-0.07
|
-0.05
|
-0.03
| | | | | |
|
Exch. Ca
|
0.54**
|
0.45*
|
0.37
|
0.55**
| | | | |
|
Exch. K
|
0.66***
|
0.79***
|
0.06
|
0.10
|
0.35
| | | |
|
Exch. Mg
|
0.68***
|
0.75***
|
0.17
|
0.18
|
0.62***
|
0.67***
| | |
|
Exch. Na
|
-0.14
|
-0.06
|
-0.14
|
-0.14
|
-0.08
|
-0.04
|
0.02
| |
|
CEC
|
0.79***
|
0.71***
|
0.45*
|
0.04
|
0.73***
|
0.65***
|
0.84***
|
0.04
|
Table 5.
Correlation coefficient of the selected parameters for calcareous soil (n = 25).
|
Variables
|
T-C
|
SOCC |
SICC |
pH
|
Exch. Ca
|
Exch. K
|
Exch. Mg
|
|
SOCC |
-0.02
| | | | | | |
|
SICC |
0.91***
|
-0.43*
| | | | | |
|
pH
|
-0.10
|
-0.14
|
-0.03
| | | | |
|
Exch. Ca
|
0.17
|
0.16
|
0.09
|
0.44*
| | | |
|
Exch. K
|
0.19
|
0.25
|
0.07
|
-0.19
|
0.24
| | |
|
Exch. Mg
|
0.06
|
0.40*
|
-0.11
|
-0.42*
|
-0.05
|
0.24
| |
|
CEC
|
0.49*
|
-0.06
|
0.46*
|
-0.40*
|
0.11
|
0.20
|
0.42*
|
Table 6.
Correlation coefficient of the selected parameters for reclaimed tidal soil (n = 9).
|
Variables
|
T-C
|
SOCC |
SICC |
pH
|
Exch. Ca
|
Exch. K
|
Exch. Mg
|
Exch. Na
|
|
SOCC |
-0.16
| | | | | | | |
|
SICC |
0.85**
|
-0.65
| | | | | | |
|
pH
|
-0.56
|
0.22
|
-0.55
| | | | | |
|
Exch. Ca
|
-0.10
|
0.44
|
-0.31
|
0.25
| | | | |
|
Exch. K
|
0.18
|
-0.65
|
0.48
|
-0.57
|
-0.54
| | | |
|
Exch. Mg
|
0.72*
|
-0.28
|
0.70*
|
-0.48
|
-0.41
|
0.42
| | |
|
Exch. Na
|
0.24
|
-0.16
|
0.27
|
0.17
|
-0.49
|
0.40
|
0.49
| |
|
CEC
|
0.65
|
-0.01
|
0.51
|
-0.00
|
-0.18
|
0.17
|
0.64
|
0.81**
|
Conclusions
토양 탄소 축적에 관한 연구는 작물의 생산성과 환경 영향에 중점을 두어 주로 유기물 (유기 탄소)에 집중되어 있으나, 토양 중 잔존하는 무기 탄소에 관한 연구는 상당히 미흡한 실정이다. 따라서, 본 연구는 작물이 경작되고 있는 유기 농경지, 석회질 및 간척지 토양에서 SOC와 SIC 함량을 비교 평가하고 SOC와 SIC 함량에 영향을 미치는 토양 화학성 인자를 상관 분석을 통해 규명하고자 하였다. 유기 농경지의 T-C의 함량은 석회질 토양 (2.87%) > 유기 농경지 토양 (2.09%) > 간척지 토양 (0.81%) 순이었다. 한편, SOCC는 유기 농경지, 석회질 및 간척지 토양에서 각각 1.98%, 1.46% 및 0.24%로 나타났던 반면, SICC는 각각 0.21%, 1.41%, 0.57%로 나타났다. T-C 중 SOCC과 SICC의 비율은 유기 농경지 토양이 93%와 7%, 석회질 토양이 57%와 43% 및 간척지 토양이 30%와 70%으로 석회질 토양과 간척지 토양에서 SICC의 비율이 현저히 높았다. 특히, 간척지 토양의 SICC는 Mg2+과 유의적으로 정의 상관관계를 나타내어 탄산염과 금속 양이온의 화학반응으로 MgCO3이 생성되었기 때문으로 판단된다. 따라서, 작물이 경작되고 있는 모든 농경지를 대상으로 토양 무기 탄소를 포함한 토양 탄소 축적량의 평가가 필요할 것으로 사료된다. 특히, 국토 면적의 10% 이상을 차지하는 석회암지대와 간척지를 대상으로 잠재적인 토양 무기 탄소 축적량을 고려한다면 국내 농경지 부문 토양 탄소 축적량에 대한 산정방법론의 개선을 시사하는 바이다.
Funding
This work was carried out with the support of “Cooperative Research Program for Agriculture Science and Technology Development (Project No. RS-2022-RD010404)” Rural Development Administration, Republic of Korea.
Conflict of Interest
The authors declare that they have no known competing financial interests or personal relationships that could have appeared to influence the work reported in this paper.
Author Contribution
Kim AR: Data curation, Writing-original draft, Visualization, Ku HH: Supervision, Conceptualization, Writing-review & editing.
Data Availability
Data will be provided on reasonable request.
References
Abate G, Masini JC. 2003. Influence of pH and ionic strength on removal processes of a sedimentary humic acid in a suspension of vermiculite. Colloid. Surface. A. 226:25-34. https://doi.org/10.1016/S0927-7757(03)00418-7
10.1016/S0927-7757(03)00418-7Andersson S, Nilsson SI. 2001. Influence of pH and temperature on microbial activity, substrate availability of soil-solution bacteria and leaching of dissolved organic carbon in a mor humus. Soil Biol. Biochem. 33:1181-1191. https://doi.org/10.1016/S0038-0717(01)00022-0
10.1016/S0038-0717(01)00022-0Batool M, Cihacek LJ, Alghamdi RS. 2024. Soil inorganic carbon formation and the sequestration of secondary carbonates in global carbon pools: a review. Soil Systems. 8:15. https://doi.org/10.3390/soilsystems8010015
10.3390/soilsystems8010015Belmonte SA, Luisella C, Stahel RJ, Bonifacio E, Novello V, Zanini E, Steenwerth KL. 2018. Effect of long-term soil management on the mutual interaction among soil organic matter, microbial activity and aggregate stability in a vineyard. Pedosphere. 28:288-298. https://doi.org/10.1016/S1002-0160(18)60015-3
10.1016/S1002-0160(18)60015-3Bhattacharyya SS, Ros GH, Furtak K, Iqbal HM, Parra-Saldívar R. 2022. Soil carbon sequestration-an interplay between soil microbial community and soil organic matter dynamics. Sci. Total Environ. 815:152928. https://doi.org/10.1016/j.scitotenv.2022.152928
10.1016/j.scitotenv.2022.15292834999062Boettinger JL. 2005. Alluvium and alluvial soils. Encyclopedia of Soils in the Environment (2nd ed.). 417-423. Academic Pres. New York.
10.1016/B978-0-12-822974-3.00196-8Bontpart T, Weiss A, Vile D, Gérard F, Lacombe B, Reichheld JP, Mari S. 2024. Growing on calcareous soils and facing climate change. Trends Plant Sci. S1360-1385:00069-4. https://doi.org/10.1016/j.tplants.2024.03.013
10.1016/j.tplants.2024.03.01338570279Gil MV, Carballo MT, Calvo LF. 2008. Fertilization of maize with compost from cattle manure supplemented with additional mineral nutrients. J. Waste Manage. 28:1432-1440.https://doi.org/10.1016/j.wasman.2007.05.009
10.1016/j.wasman.2007.05.00917624756Guo Y, Wang X, Li X, Wang J, Xu M, Li D. 2016. Dynamics of soil organic and inorganic carbon in the cropland of upper yellow river delta, china. Sci. Rep. 6:36105. https://doi.org/10.1038/srep36105
10.1038/srep3610527782204PMC5080587Hu P, Zhang W, Chen H, Li D, Zhao Y, Zhao J, Xiao J, Wu F, He X, Luo Y, Wang K. 2021. Soil carbon accumulation with increasing temperature under both managed and natural vegetation restoration in calcareous soils. Sci. Total Environ. 767:145298. https://doi.org/10.1016/j.scitotenv.2021.145298
10.1016/j.scitotenv.2021.14529833636790Johnston CA, Groffman P, Breshears DD, Cardon ZG, Currie W, Emanuel W, Gaudinski J, Jackson RB, Lajtha K. Nadelhoffer K, Jr DN, Post WM, Retallack G, Wielopolski L. 2004. Carbon cycling in soil. Front. Ecol. Environ. 2:522-528. https://doi.org/10.1890/1540-9295(2004)002[0522:CCIS]2.0.CO;2
10.1890/1540-9295(2004)002[0522:CCIS]2.0.CO;2Kim GH, Kim GY, Kim JG, Sa DM, Suh JS, Son BG, Yang JU, Eom KC, Lee SE. 2006. Soil science(2nd ed.). 258. Hyangmunsa, Seoul, Korea.
Kim HJ, Kim GR, Woo HN, Park SH, Shin JH, Choi YC, Chung DY. 2011. Properties and fate of nitrogen in a reclaimed tidal soil. Korean J. Agric. Sci. 38:301-307.
Kim HW, Choi HS, Kim BH, Kim HJ, Choi KJ, Chung DY, Kuk YI, Lee SM. 2012. Effects of organic nutrient sources on characteristics of a paddy soil and rice production. J. Korean Soc. Int. Agric. 24:1-5.
Kim JG, Lee KB, Lee SB, Lee DB, Kim SJ. 2000. The effect of long-term application of different organic material sources on chemical properties of upland soil. Korean J. Soil Sci. Fert. 33:416-431.
Kim JW, Hong YK, Lee CR, Kim SC. 2023. Comparison of physicochemical and biological soil properties in organic and conventional upland fields. Korean J. Soil Sci. Fert. 56:77-89. https://doi.org/10.7745/KJSSF.2023.56.1.077
10.7745/KJSSF.2023.56.1.077Kim JY, Shin JK, Lee CH, Song JH, Shin CH. 2022. A study on the change of vegetation dynamics in saemangeum exposed reclaimed land - a case study of samangeum national arboretum -. TJOKI. 34:151-165 https://doi.org/10.26840/JKI.34.2.151
10.26840/JKI.34.2.151Ko ES, Joung JA, Kim CH, Lee SH, Sa T, Choi JH. 2014. Relationship between chemical property and microbial activity of reclaimed tidal lands at western coast area in Korea. Korean J. Soil Sci. Fert. 47:254-261.
10.7745/KJSSF.2014.47.4.254Lee Y, Choi HS, Lee SM, Jung JA, Kuk YI. 2012. Effects of organic materials on changes in soil nutrient concentrations and nutrient uptake efficiency in sorghum- sudangrass hybrid (Sorghum bicolor (L.) Moench). J. Bio-Env. Con. 21:108-113.
Park YL, Kim YJ, Hyun JG, Jung JS, Yoo G. 2023. Assessing soil organic carbon stock and stability in volcanic grasslands: implications for climate change mitigation potential and management levels. Korean J. Soil Sci. Fert. 56:342-353.
10.7745/KJSSF.2023.56.4.342Raza S, Zamanian K, Ullah S, Kuzyakov Y, Virto I, Zhou J. 2021. Inorganic carbon losses by soil acidification jeopardize global efforts on carbon sequestration and climate change mitigation. J. Clean Prod. 315:128036. https://doi.org/10.1016/j.jclepro.2021.128036
10.1016/j.jclepro.2021.128036Ryu JH, Lee SH, Oh YY, Lee JT. 2019. Soil chemical properties of reclaimed tide lands under government management in Korea: results of 4-years monitoring. KJEA, 38:273-280. https://doi.org/10.5338/kjea.2019.38.4.37
10.5338/KJEA.2019.38.4.37Solomon S, Qin D, Manning M, Marquis M, Averyt K, Tignir MMB, Miller, HLJ, Chen Z. 2007. Intergovernmental panel on climate change IPCC 2007: the scientific basis contribution of working group I to the fourth assessment report of the intergovernmental panel on climate change IPCC. Cambridge Univ, New York, NY, USA.
Taalab AS, Ageeb GW, Siam HS, Mahmoud SA. 2019. Some characteristics of calcareous soils. A review. CRW. 8:96-105.
Vermeer AWP, Riemsdijk WHV, Koopal LK, 1998. Adsorption of humic acid to mineral particles. 1. Specific and electrostatic interacions. Langmuir 14:2810-2819.
10.1021/la970624rWang Q, Li Y, Klassen W. 2005. Determination of cation exchange capacity on low to highly calcareous soils. Commun. Soil. Sci. Plan. 36:1479-1498.https://doi.org/10.1081/CSS-200058493
10.1081/CSS-200058493Whalen JK, Chang C, Clayton GW, Carefoot JP. 2000. Cattle manure amendments can increase the pH of acid soils. Soil Sci. Soc. Am. J. 64:962-966. https://doi.org/10.2136/sssaj2000.643962x
10.2136/sssaj2000.643962xYang H, Xie Y, Zhu T, Zhou M. 2021. Reduced organic carbon content during the evolvement of calcareous soils in karst region. JFS, 12:221. https://doi.org/10.3390/f12020221
10.3390/f12020221Yao LX, Li GL, Tu SH, Sulewski G, He ZH. 2007. Salinity of animal manure and potential risk of secondary soil salinization through successive manure application. Sci. Total Environ. 383:106-114. https://doi.org/10.1016/ j.scitotenv.2007.05.027
10.1016/j.scitotenv.2007.05.02717572477Zhang H, Wu P, Yin A, Yang X, Zhang X, Zhang M, Gao C. 2016. Organic carbon and total nitrogen dynamics of reclaimed soils following intensive agricultural use in eastern China. Agric. Ecosyst. Environ. 235: 193-203. https://doi.org/10.1016/j.agee.2016.10.017
10.1016/j.agee.2016.10.017Zhang H, Yin A, Yang X, Wu P, Fan M, Wu J, Gao C. 2019. Changes in surface soil organic/inorganic carbon concentrations and their driving forces in reclaimed coastal tidal flats. Geoderma 352:150-159. https://doi.org/10.1016/j.geoderma.2019.06.003
10.1016/j.geoderma.2019.06.003