Introduction
경제발전과 인구증가로 인해 음식물류 폐기물의 발생량은 지속적으로 증가되어왔다. 2014년 기준 음식물류 폐기물의 발생량은 연간 약 4,999천 톤으로 전체 생활폐기물의 약 27.4%를 차지하고 있다 (MOE, 2014). 이러한 음식물류 폐기물 중 농수산물 시장에서 발생하는 폐기물의 발생량은 연간 약 134천 톤이며 수산물, 축산 폐기물을 포함한 전체 농수산물 폐기물 중 청과류 폐기물은 약 80%를 차지하고 있다.
이러한 많은 양의 음식물 폐기물을 처리하는 방법에는 매립과 소각, 자원화 등 여러 방법이 있다. 1990년대 까지만 해도 음식물 폐기물의 약 95%이상은 매립 처리하였으나 매립지 내의 악취와 침출수의 문제점이 주로 발생하였다 (Jang et al., 1997). 따라서 2005년부터 음식물류 폐기물의 직접 매립이 전면 금지되어 음식물 폐기물의 사료화 및 퇴비화 등의 자원화 처리에 대한 연구가 활발히 진행되고 있다 (Ryu et al., 2004). 2013년을 기준으로 음식물류 폐기물의 총 발생량 중 93.2%가 전국 240개소의 자원화 시설에서 처리되고 있으며 자원화 비율은 각각 사료화 51.6%, 퇴비화 43.9%, 에너지화 4.5% 순으로 활용되고 있다 (MOE, 2013).
음식물 폐기물의 다양한 자원화 방법 중 퇴비화에 관한 연구는 가장 활발하게 진행되고 있으며 주로 부자재별 혼합 영향에 관한 연구 (Park, 2003; Han et al., 2007), 퇴비화 중 미생물에 관한 연구 (Shin et al., 2009; Park et al., 2008), 그리고 퇴비 시용에 관한 연구 (So et al., 2007) 등이 있다.
하지만 현재까지는 음식물 폐기물에 대한 연구만이 진행되었을 뿐 채소 부산물과 같은 청과류 폐기물의 퇴비화 연구는 비교적 미흡한 실정이다. 채소 부산물의 퇴비화에 관한 선행연구를 살펴보면 Choi and Wan (1994)의 채소 부산물과 나무조각, 낙엽의 부자재를 이용한 연구의 경우 채소 부산물을 단독으로 퇴비화한 결과 높은 수분함량과 유기물의 부족으로 인해 퇴비화에 적합하지 않아 채소 부산물에 약 20%의 유기물을 첨가할 것을 제안하였고 (Choi and Wan, 1994), 배추와 무청 부산물을 이용한 연구의 경우 56일 이후 안정화됨을 보고하였다 (Jang et al., 1997). 또한 Park et al. (1998)의 배추와 볏짚을 이용한 연구의 경우 28일 간 퇴비화 한 결과 C/N율이 20이하로 나타나 퇴비화가 완료되었다고 판단하였다. 이러한 선행연구들은 배추 등의 채소 부산물만을 이용한 것이 대부분이었으며 농수산물 시장에서 발생하는 과일, 채소 부산물이 혼합된 청과류 폐기물의 퇴비화 연구는 아직 미비하였다.
유기성 폐기물의 처리방법 중 퇴비화는 미생물의 생분해 활동을 이용하여 유기물을 안정화하는 방법이다 (Chen et al., 2014). 안정된 폐기물 퇴비는 양분 공급과 토양의 물리성 개선, 미생물 접종의 농업적 이익이 있으며, 현재 퇴비의 작물 생장의 촉진과 질병 억제에 대한 연구도 진행되고 있다 (Ventorino et al., 2016; Martin and Brathwaite, 2012). 청과류 폐기물은 유기성 자원으로서 중금속 등의 외부 오염물질로부터 비교적 안전하여 이러한 퇴비화의 원료로서 가치가 있다 (Kim and Shin, 2009; Ntougias et al., 2008). 본 연구에서는 청과류 폐기물의 퇴비화 가능성을 평가하였다. 최적의 퇴비화 조건을 도출하기 위해 부자재 선정 및 혼합 비율을 산정하고 생산된 부숙 유기질 비료의 영양 성분과 부숙도 및 안정성을 평가하였다.
Materials and Methods
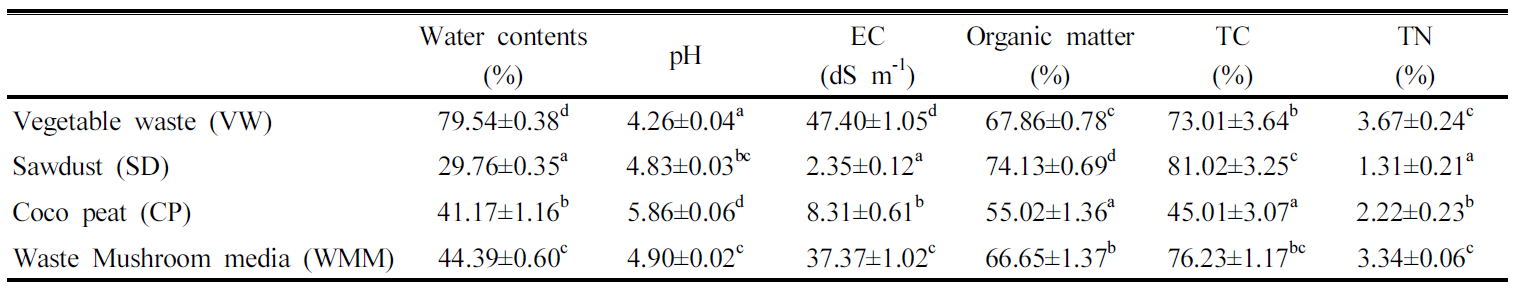
퇴비화 원료 퇴비화에 이용된 청과류 폐기물은 2016년 6월 대전소재 농수산물 시장에서 채취하였으며 시장에서 자체적으로 1차 분쇄, 탈수 처리된 시료를 이용하였다. 수분조절 및 탄소원으로 부재료인 톱밥, 코코피트, 버섯폐배지를 이용하였으며 톱밥, 코코피트는 온라인 판매업체를 통해 구입하였고, 버섯폐배지는 대전소재 버섯농가에서 수거하였다.
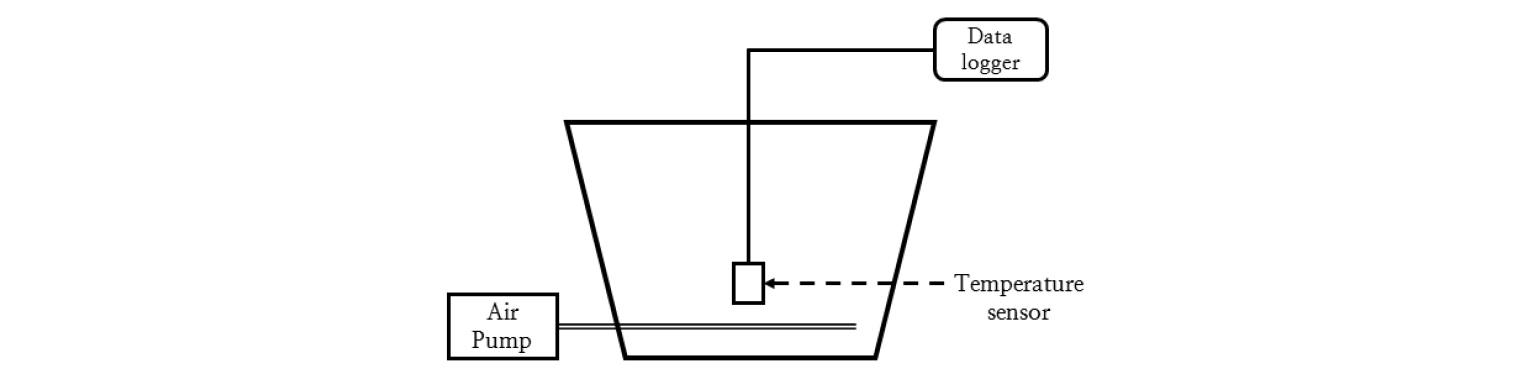
퇴비화 장치 및 방법 본 연구에 이용된 퇴비화 반응기는 약 61 L의 아이스박스 (W36×L61×H30 cm)를 이용하였다. 반응기 내부 바닥에는 공기 주입기 (MA-200, wave point, USA)에 연결된 튜브를 고정하여 퇴비시료에 1.67 L min-1의 공기가 지속적으로 공급되도록 하였고, 온도센서 (EM50, Decagon devices, USA)를 퇴비더미의 하단에 설치하여 4시간 간격으로 온도를 측정하였다. 반응기의 모식도는 Fig. 1 에 나타내었다.
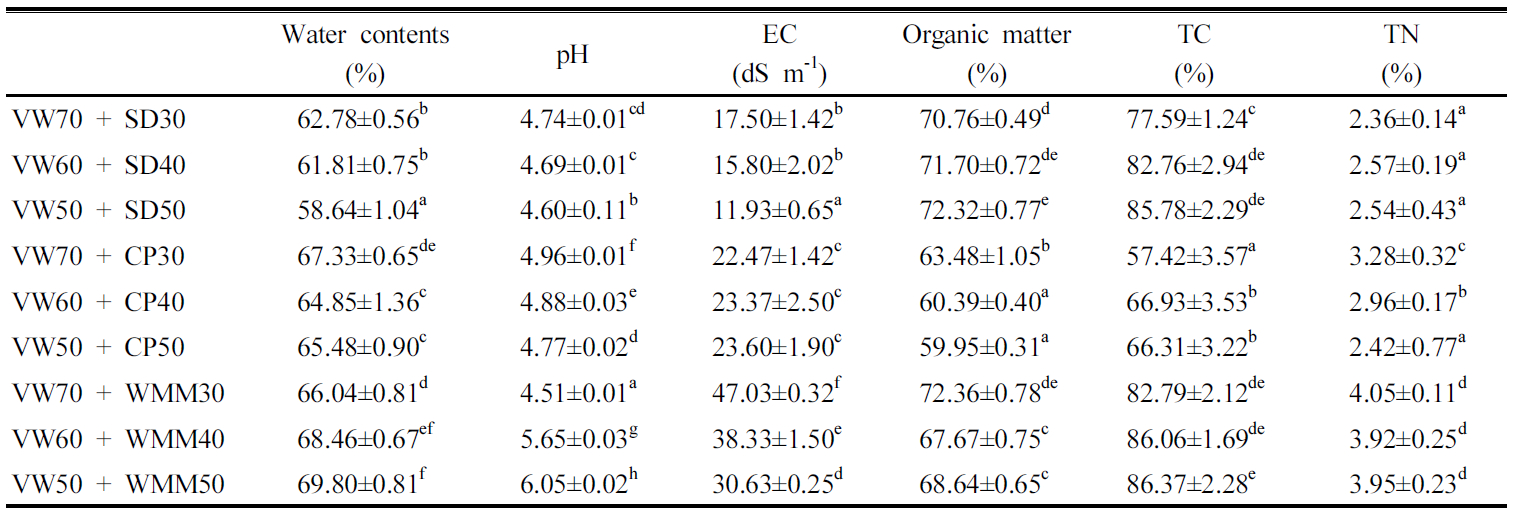
청과류 폐기물과 부자재의 혼합 비율별 퇴비화를 평가하기 위해 청과류 폐기물과 부자재 (톱밥, 코코피트, 버섯폐배지)를 각각 70 : 30, 60 : 40, 50 : 50의 무게비 (w/w)로 혼합하였으며 대조구는 부자재를 혼합하지 않은 청과류 폐기물의 단독 처리로 설계하였다. 혼합 비율은 퇴비화를 위한 최적 수분함량인 50~60%를 고려하여 설정하였다 (Bernal et al., 2009). 퇴비화 시험은 2016년 6월부터 8월까지 약 35일간 진행되었으며 처리구 설치 후 5일 간격으로 교반하였다. 시료채취는 플라스틱 샘플백에 약 200 g의 시료를 채취한 후 실험실로 옮겨 오븐에서 40°C로 건조 후 파쇄하여 성분 분석에 사용 하였다.
퇴비 성분 분석 퇴비 시료의 분석은 농촌진흥청에서 고시한 비료의 품질검사방법 및 시료채취기준에 준하여 분석하였다. 수분함량은 105°C에서 5시간 건조하여 감량을 측정하였고 pH와 전기전도도 (EC)는 시료와 증류수를 각각 1 : 10 (w/v)으로 혼합하여 1시간 교반 후 pH meter (MP 220, Mettler Toledo, Switzerland)와 EC meter (S230, Mettler toledo, Switzerland)로 측정하였다. 유기물 측정은 회화법을 이용하였으며 600°C에서 약 2시간 가열한 후 강열함량을 계산하였다. 퇴비의 총 탄소와 질소는 자동원소분석기 (EA1112, Thermo Fisher Scientific, USA)을 이용해 분석하였다. 또한 퇴비의 중금속 함량을 조사하기 위해 1 g의 시료를 삼각 플라스크에 취하여 진한 질산 20 mL을 가하고 하루 간 정치한 후 가열하여 건고시켰다. 또한 냉각 후 질산, 황산, 과염소산을 각각 10 : 1 : 4의 비율로 혼합한 Ternary solution 20 mL 가하여 분해한 후 ICP-AES (Icap 7000, Thermo fisher scientific, USA)로 분석하였다 (RDA, 1997).
부숙도 평가 제조된 퇴비의 부숙도를 평가하기 위해 비료의 품질검사방법 및 시료채취기준에 명시되어 있는 기계적부숙도 측정법 (Solvita)과 종자발아시험을 이용하였다. Solvita 측정법은 제조사에서 제공한 시험방법을 바탕으로 측정용기에 표시된 부분까지 퇴비를 약 50 g 채우고 이산화탄소와 암모니아 반응 패드를 꽃아 25°C에서 4시간 방치 후 색깔변화를 표준차트와 비교하여 분석하였다. 종자발아시험은 시료 1 g에 증류수 50 mL 가하여 80°C에서 2시간 열수 침탕하였다. 추출된 용액은 여과한 후 무 종자 (Raphanus sativus L.) 30립을 넣은 90 mm 페트리디시 (petri dish)에 가하여 상온에서 5일간 배양하여 발아율과 뿌리길이를 조사하였다. 대조구는 추출용액 대신 증류수를 이용하여 동일하게 배양한 무 종자의 발아를 이용하였다. 종자발아지수 (Germination Index, GI)는 발아율 (Germination rate, GR)과 뿌리길이 (Root extension, RE)을 이용하여 지수화 한 것으로 다음의 식을 이용한다 (Lee et al., 2015).
GI = (GR × RE)
GR = (발아율 / 대조구 발아율) × 100
RE = (뿌리길이 / 대조구 뿌리길이) × 100
통계분석 방법 본 연구는 각 처리구에서 3반복으로 시료를 채취하여 진행하였으며 결과값은 평균과 표준편차를 구하여 one-way analysis of variance (ANOVA)와 최소 유의차 검정 (Least Significant Difference, LSD)의 통계분석법을 통해 처리구간의 유의적인 차이 (p<0.05)가 있는지 확인하였다. 통계적 분석은 Duncan test를 이용하였으며 SPSS 22.0 소프트웨어로 분석하였다.
Results and Discussion
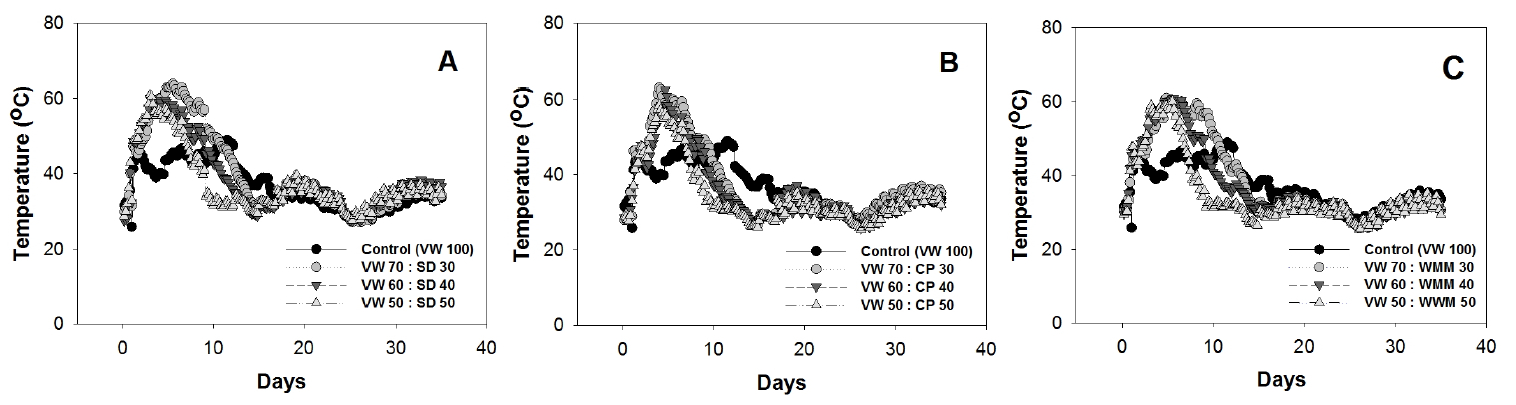
퇴비화 과정 중 온도변화 호기성 퇴비화에서 온도변화는 퇴비화 반응의 미생물의 대사활동의 지표로서 이용되며 최적온도는 45~55°C이다 (de Bertoldi et al., 1983). 본 연구의 퇴비화 과정 중 온도변화는 Fig. 2에 나타내었다. 각 처리구별 퇴비화 과정 중 온도변화를 모니터링한 결과 대조구를 제외한 모든 처리구에서 퇴비화 1일차부터 온도가 상승하였으며, 약 5일차에 최고점에 도달하였다. 그 후 서서히 온도가 하강하여 약 15일 이후로 모든 처리구에서 30°C부근에 안정화 되었다. 최고온도는 톱밥, 코코피트, 버섯폐배지 처리구에서 각각 60~64°C, 58~63°C, 60~62°C도로 나타났고 톱밥 30% 처리구에서 가장 높은 온도상승을 보였다. 대조구에서는 2일차부터 약 10일간 39~49°C의 온도를 유지하였다. 이러한 온도 변화는 미생물에 의한 발효가 아닌 외부 온도 및 부패에 의한 온도상승으로 사료되었으며 또한 높은 수분함량으로 인해 퇴비내부의 통기가 제한되어 혐기화 되었기 때문으로 판단된다 (Choi and Wan, 1994).
온도변화는 원료의 특성과 부자재와의 혼합비, 수분함량, 공기공급 조건에 의해 크게 달라질 수 있다 (Bueno et al., 2008; Yu and Chang, 1998). 가축분과 음식물류 폐기물의 퇴비화에 대한 선행 연구결과를 참조한 결과, 대부분 퇴비화 2~5일째에 최고온도가 약 50~70°C까지 상승하였으며 15~20일 이후로 온도변화가 크게 나타나지 않았다. 특히 가축분의 경우 퇴비화 시작 1~5일째에 약 53.8~78°C의 온도까지 상승하여 1~7일째에 42~70°C의 최고온도를 보인 음식물류 폐기물의 퇴비화보다 비교적 빠른시간에 더 높은 온도까지 상승함을 보였다. 본 연구에서는 일반적인 음식물류 폐기물과 가축분 퇴비에 비해 초기에 온도상승이 비교적 더딘 경향이 있었으며 이는 퇴비화 원료의 낮은 pH로 인해 미생물 활성이 초기에 저해되었기 때문으로 판단된다 (Kazemi et al., 2016). 또한 가축분 퇴비와 음식물류 퇴비에서 축분이나 음식물 별 온도차이보다 원료에 혼합된 부자재의 특성, 통기방식에 따른 차이가 더욱 크게 나타나, 퇴비화 조건이 퇴비화에 많은 영향을 끼침을 알 수 있었다 (Chang et al., 2008; Sohn et al., 1996; Lee et al., 2001; Park, 2003; Namkoong et al., 2002).
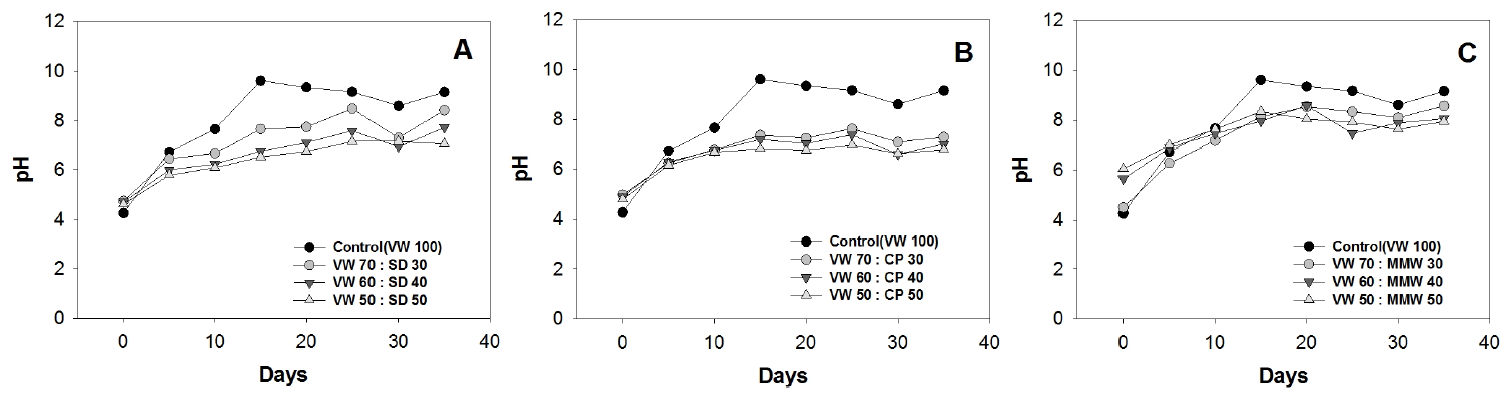
pH 및 EC변화 퇴비화에서 pH는 퇴비부숙의 간접적 지표로 이용될 수 있으며 퇴비화 미생물 활성의 최적범위는 6~9 정도이다 (Miller, 1992). 가축분은 대부분 최적범위 내의 pH를 나타내나 7.5 이상의 비교적 높은 pH를 나타내어 암모니아 휘산을 통한 질소손실이 나타나는 경우가 많다 (Bernal et al., 2009). 반면 음식물류 폐기물에서는 초기에 산성 pH를 나타내는 경우가 많은데 이는 퇴비화 과정에서 발생하는 유기산의 영향 때문이라는 선행 연구 결과가 있다 (Lee et al., 2004; Chang et al., 1995). 특히 이러한 낮은 pH에서는 퇴비화에 관여하는 세균, 방선균 등의 미생물 활성이 저해될 수 있다.
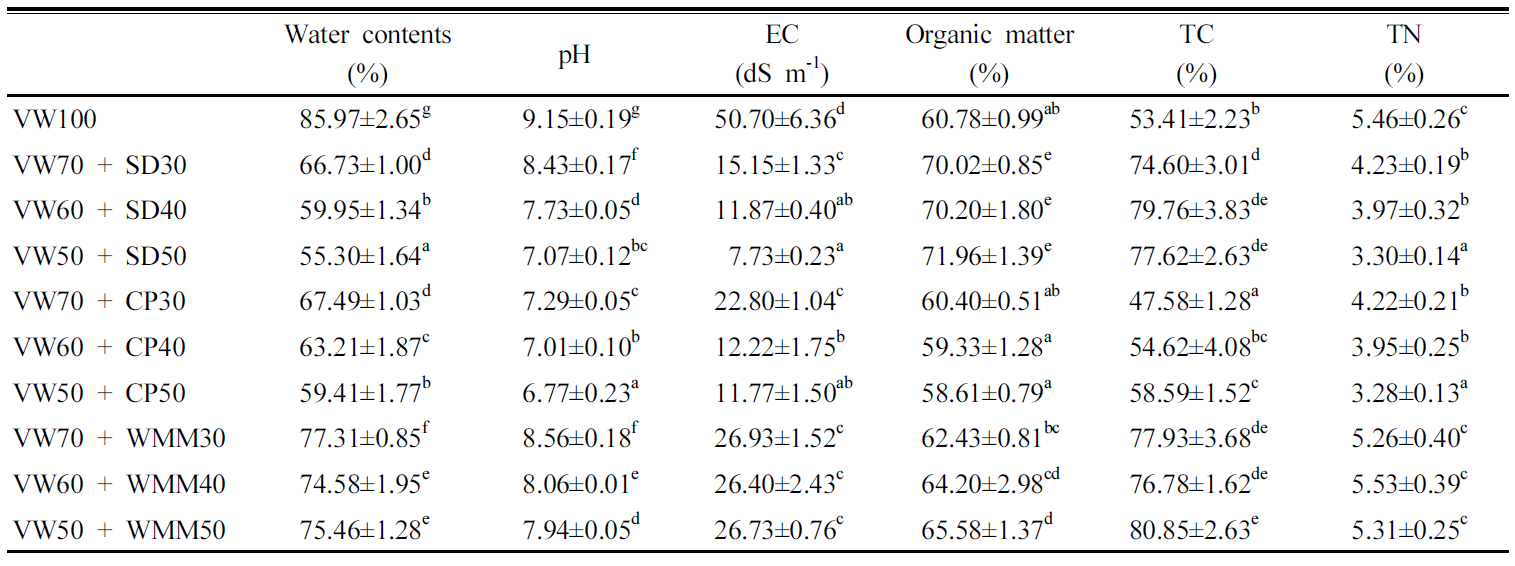
본 퇴비화 시험의 pH, EC변화는 Fig. 3, Fig. 4에 나타내었다. pH의 경우, 대조구와 톱밥, 코코피트 처리구에서 초기 4.26~4.96, 버섯폐배지 처리구에서 4.51~6.05로 나타나 모두 산성을 나타내었다. 퇴비화 과정에서 대조구는 시험 15일차부터 급격히 상승하여 8.60~9.61을 유지한 반면 대조구를 제외한 나머지 모든 처리구의 pH는 6.77~8.56까지 완만하게 상승하였다. 이때 pH의 상승은 에어펌프와 교반으로 인해 산소공급이 지속적으로 이루어져 호기적 조건이 유지되면서 시료 내의 유기산의 분해와 단백질로부터 암모니아의 생성이 진행되었기 때문이다 (Said-pullicino et al., 2007). 최종퇴비의 pH는 대조구에서 9.15 나머지 처리구에서 6.77~8.56으로 나타났으며 대조구를 제외한 모든 처리구에서 안정화된 퇴비의 pH인 7~8의 범위로 조사되어 (Joo et al., 2007) 퇴비화의 적정 pH가 유지된 것으로 조사되었다.
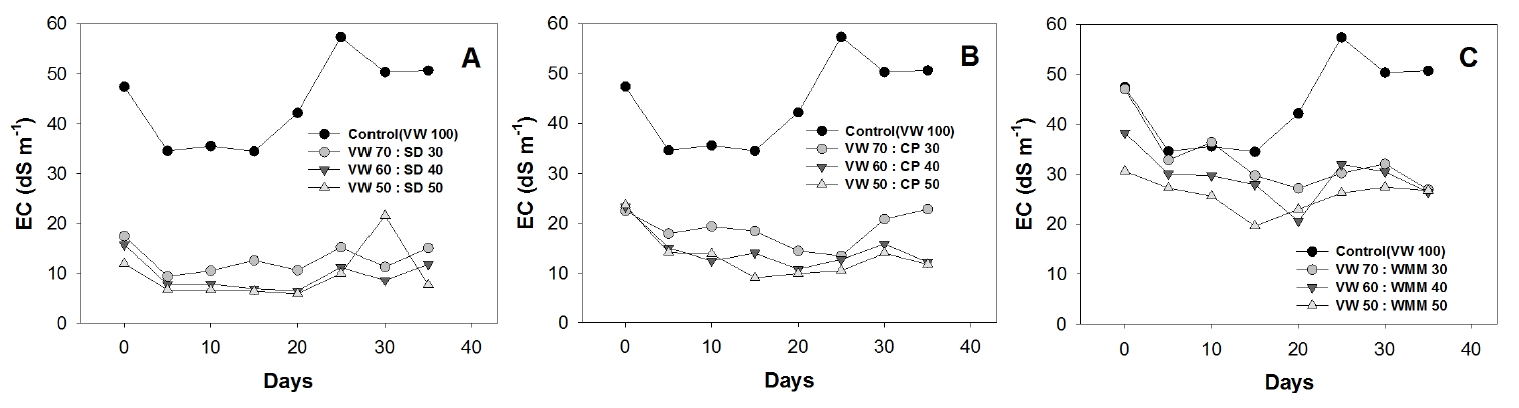
퇴비화에서 전기전도도(EC)의 변화는 미생물에 의해 유기물이 분해되며 생성되는 이온들과 관련이 있으며 (Yun et al., 2012) 토양에 시용하였을 때 식물독성을 나타낼 수 있는 가능성을 평가 할 수 있다 (Petric et al., 2012). 시험 초기 대조구와 버섯폐배지 처리구의 EC 값은 다른 처리구 보다 비교적 높은 30.6~47.4 dS m-1로 나타났고 이는 버섯폐배지에 함유된 폐화석에서 기인한 것으로 판단된다. 퇴비화 과정동안 EC는 감소하였다가 다시 증가하는 경향을 보였으며 최종 퇴비에서 대조구 (50.7 dS m-1)를 제외한 모든 처리구에서 퇴비화 이전보다 소폭 감소한 7.7~26.7 dS m-1로 일반적인 퇴비의 EC 범위 (25~50 dS m-1)에 포함되는 것으로 조사되었다 (Chang et al., 2003)
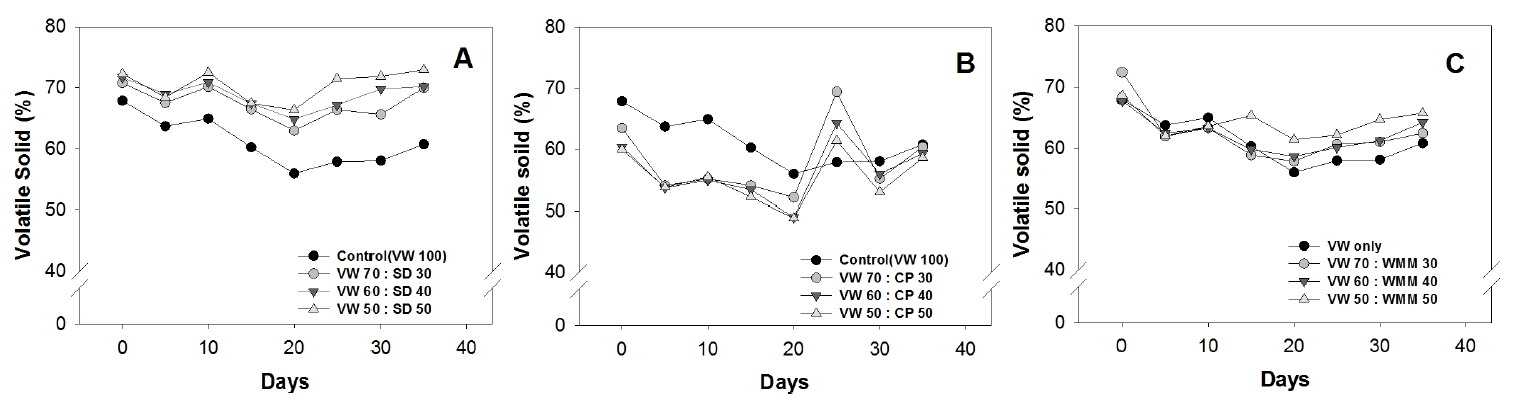
유기물 및 총 질소 함량 비료공정규격에 의하면 유기물은 퇴비 주성분 필수함량으로서 최소 30%이상이며 유기물/질소 비가 45이하이어야 한다 (Nam et al., 2010; 농촌진흥청, 2013). 선행 연구에서는 퇴비화 과정동안 퇴비의 유기물 함량과 유기물/질소 비는 감소하는 경향을 나타내었으며 (Yun et al., 2012), 본 연구의 결과도 선행연구와 마찬가지로 퇴비화 기간 동안 소폭 감소하여 최종퇴비에서 유기물함량과 유기물/질소 비는 각각 58.61~71.96%, 11.13~21.81%로 나타나 비료 공정규격 상의 기준을 충족하였다. 유기물 함량 변화는 Fig. 5에 나타내었다.
퇴비화에서 탄소는 미생물의 유기물 분해를 위한 에너지원으로 이용되며 미생물의 생장에 필요한 단백질 합성을 위해 질소가 이용된다 (Lee et al., 2005). 따라서 퇴비화 과정동안 미생물에 의한 분해과정에서 이산화탄소 발생에 의하여 탄소함량이 감소하는 경향을 보이게 된다 (Chang et al., 1995). 본 연구의 퇴비화에서 탄소함량은 대조구에서 19.6%, 처리구에서 2.18~13.2% 감소하였고 반면에 질소함량은 최종퇴비에서 증가하는 추세를 보여 최종퇴비에서 0.28~1.87% 증가하였다. 이러한 질소의 증가는 유기물의 무기화로 인해 일어난 것으로 판단된다 (Sanchez-Monodero et al., 2001).
퇴비의 C/N비는 초기 17.5~33.8로 나타나 퇴비화에 적합한 C/N비 범위 25~35 부근으로 나타났으며 (Bernal et al., 2009) 퇴비화 과정에서 감소하여 시험종료후 대조구에서 가장 낮은 9.79, 나머지 처리구에서 11.27~20.0으로 나타났다.
가장 많은 C/N 변화를 보인 처리구는 톱밥 30% 처리구로 초기 32.98에서 최종 17.63으로 감소하였다.
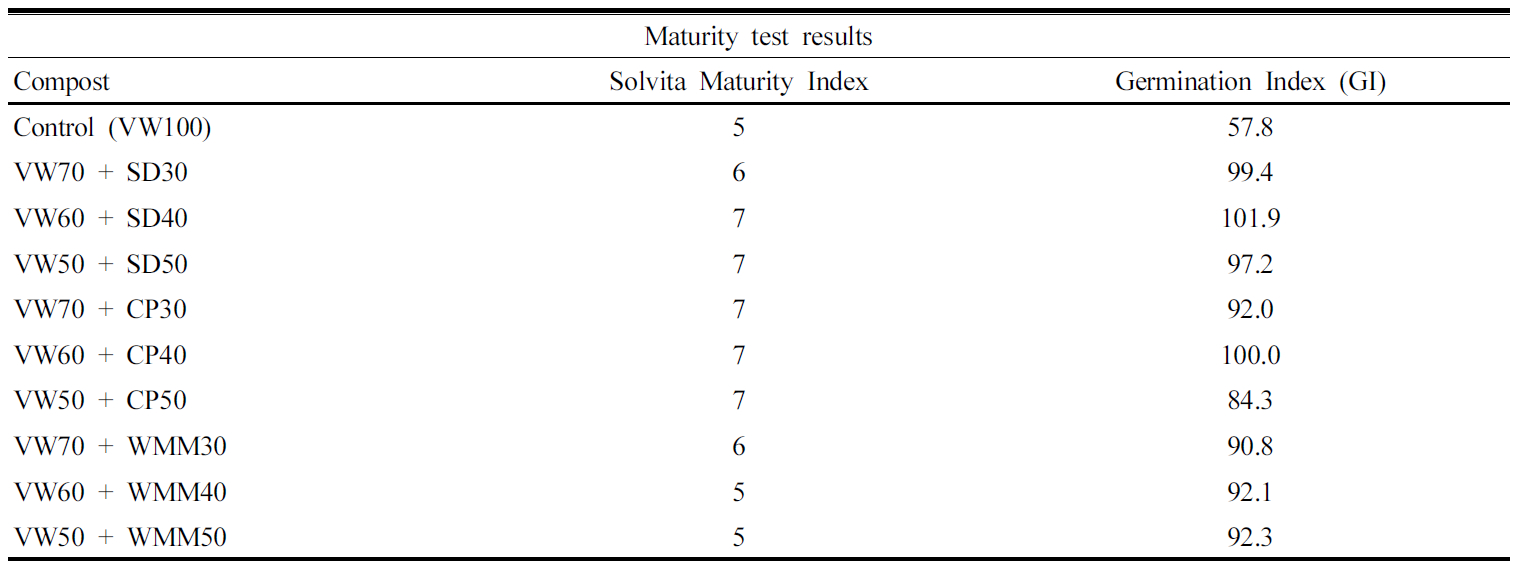
퇴비 부숙도 부숙된 퇴비는 미생물의 활동이 안정화 되고 식물독성을 나타내는 물질이 없는 퇴비로 미숙 퇴비에서는 작물의 생장을 억제하게 된다 (Zucconi et al., 1985). 영국의 퇴비 연합회 (UK Composting Association, 2001)에서는 부숙도란 ‘퇴비원료의 생물학적 분해가 이루어진 정도’로 정의했다 (Bernal et al., 2009). 본 연구에서는 퇴비화 종료 후 시료에 대해 비료의 품질검사방법 및 시료채취기준에 준하여 기계적 부숙도 측정방법 (Solvita)과 종자발아시험을 이용하여 부숙도를 측정하였으며 그 결과를 Table 4 에 나타내었다. Solvita 부숙도 측정법은 퇴비의 암모니아와 이산화탄소 방출량을 조사하여 미생물에 의한 반응이 안정되었는지 확인함으로써 부숙도를 측정하는 방법이다. 부숙지수 (Maturity Index) 4~6은 부숙후기, 7~8은 부숙완료 단계로 4 이상일 때 부숙된 것으로 판정한다. Solvita를 이용한 분석결과 대조구와 톱밥 30%, 버섯폐배지 30~50% 처리구에서 부숙후기, 나머지 처리구에서는 부숙완료로 판정되어 비료공정규격을 만족하였다. 또한 무종자 (Raphanus sativus L.) 발아시험 결과 발아율과 뿌리길이를 통해 산출한 발아지수 (GI)는 대조구에서 57.8, 처리구에서 82.24~101.1로 조사되어 비료공정규격의 부숙기준 70이상을 충족하였다. 기계적 부숙도 측정과 발아시험을 통해 조사된 부숙도 값은 서로 유사한 경향을 보였으나, Solvita에서 부숙완료로 판정되었던 코코피트 50% 처리구에서 종자발아지수는 다른 처리구에 비해 낮은 82.24로 나타났다. 이는 생 코코피트에 함유된 식물독성을 나타내는 물질이 코코피트의 함량이 높아지면서 뿌리생장에 영향을 끼쳤기 때문으로 판단된다 (Yau and Murphy. 2000).
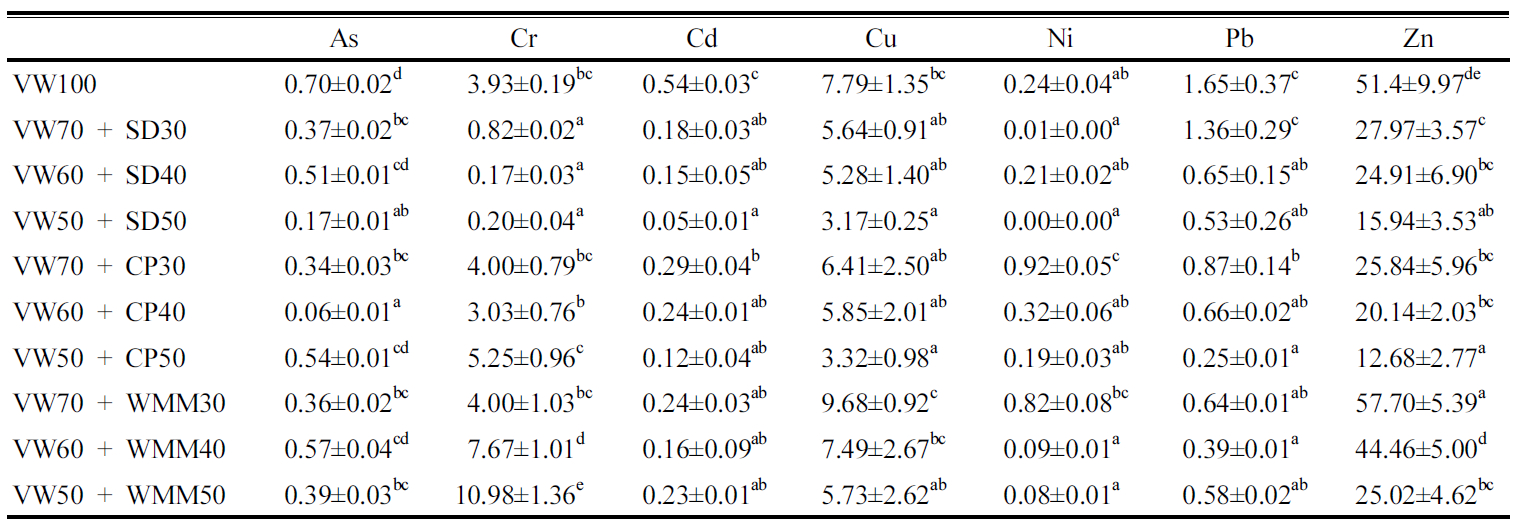
중금속 함량 중금속은 이동성이 적어 퇴비 시용에 의해 토양에 축적되어 작물에 위해성을 나타낼 수 있다. 따라서 비료 공정규격에서는 퇴비와 그 원료에 대해 As, Cd, Hg, Pb, Cr, Cu, Ni, Zn의 중금속 함량 기준을 명시하고 있으며 각각의 함량 기준은 As 45 mg kg-1, Cr 200 mg kg-1, Cd 5 mg kg-1, Cu 360 mg kg-1, Ni 45 mg kg-1, Pb 130 mg kg-1, Zn 900 mg kg-1 Hg 2 mg kg-1이다. 퇴비화 종료 후 최종퇴비에서 중금속 함량을 조사한 결과는 Table 5에 나타내었으며, 각각 As 0.06~0.70 mg kg-1, Cr 0.17~10.98 mg kg-1, Cd 0.05~0.54 mg kg-1, Cu 3.17~9.68 mg kg-1, Ni 0.01~0.92 mg kg-1, Pb 0.39~1.65 mg kg-1, Zn 12.68~57.70 mg kg-1 (Hg 검출한계 이하)으로 모든 처리구에서 중금속 함량은 기준 미만으로 나타나 퇴비로서 안전한 것으로 나타났다.
Conclusion
본 연구에서는 농수산물 시장에서 발생하는 청과류 폐기물의 퇴비화 가능성을 평가하였다. 퇴비화 최적조건을 확인하기 위해 부자재 (톱밥, 코코피트, 버섯폐배지)를 각각 30, 40, 50% (w/w) 혼합하여 처리하였으며, 부자재를 혼합하지 않은 청과류 폐기물을 대조구로 설정하여 약 35일 간 퇴비화 하였다.
퇴비화 과정 중 이화학적 특성을 조사한 결과, 최고온도는 톱밥 30% 처리구에서 64°C로 측정되었다. pH는 퇴비화 초기 모든 처리구에서 4.26~6.05로 비교적 낮은 pH를 보였다가 이후 상승하여 최종 퇴비에서 대조구와 처리구에서 각각 9.15, 6.77~8.56으로 조사되어 안정된 퇴비의 pH를 나타내었다. 모든 처리구의 유기물 함량은 초기 60.0~72.3%에서 최종퇴비 58.6~72.0%로 소폭 감소하였다. 퇴비화 과정 중 모든 처리구와 대조구를 비교하였을 때, 온도와 pH변화에서 유의한 차이가 있었으며, 각각의 부자재 30% 처리구에서 퇴비화가 가장 활발하게 진행되었다. 퇴비화 완료 후 최종 품질조사 결과 총 탄소함량은 최종 퇴비에서 초기보다 대조구에서 19.6%, 처리구에서 2.18~13.2% 감소하였고 반면 질소함량은 퇴비화 과정 중 0.28~1.87% 증가하였다. 처리구 중 버섯폐배지 혼합 처리구에서 가장 많은 질소함량 (5.26~5.53%)이 측정되었으며, 이는 버섯폐배지의 원료 특성에 의한 것으로 판단된다. 최종퇴비의 EC는 대조구 (50.7 dS m-1)를 제외한 모든 처리구에서 톱밥과 코코피트 처리구에서 퇴비의 일반적인 EC범위 (25~50 dS m-1)로 조사되었다. 퇴비의 부숙도는 기계적 부숙도 측정방법 (Solvita)과 종자발아시험을 이용해 조사하였다. 그 결과 대조구를 제외한 모든 처리구에서 비료공정규격 상의 부숙기준을 만족하여 안정된 퇴비로 판단된다. 반면 청과류 폐기물을 단독 처리한 대조구에서는 선행연구에서의 결과와 같이 퇴비화가 원활하게 진행되지 않았다. 퇴비에 함유된 중금속 함량을 조사하기 위해 비료공정규격상의 중금속 함량을 측정한 결과, 기준보다 낮게 측정되어 중금속 위해성이 없는 것으로 판단된다.
본 연구 결과 농수산물 시장에서 발생하는 청과류 부산물과 유기물을 혼합하여 퇴비 생산이 가능하며 생산된 퇴비의 품질은 비료공정규격을 만족하여 농업적으로 이용할 수 있을 것으로 사료된다. 향후 청과류 폐기물을 이용한 유기질 비료의 시용에 따른 작물 영향평가가 필요할 것으로 판단된다.