Introduction
동물용 항생제는 주로 동물의 질병 치료 또는 생육을 촉진시키는 용도로 사용되어 진다 (Wegener, 2003). 이러한 동물용 항생제는 목적에 따라 동물에 투여된 후 약 10~20% 만이 체내에서 사용되어지고 나머진 80~90%는 체외로 배출 된다 (Elmund et al., 1971; Halling-Sorensen et al., 2002; Sarmah et al., 2006). 따라서 동물용 항생제는 가축의 분뇨을 통해 직접 토양에 유입되거나 분뇨을 이용하여 제조한 퇴비의 형태로 토양에 유입된다. 토양에 잔류하는 항생제의 농도는 여러 연구에서 발표되고 있다. 토양 내 잔류하는 항생제의 평균 농도는 약 0.20~60.1 µg kg-1의 농도이며 항생제의 종류에 따라 토양에 잔류하는 특성이 매우 다르다.
토양에 잔류하는 항생제는 식물의 뿌리로 흡수되어 작물에 전이가 가능하며 선행 연구에 의하면 다양한 종류의 작물체 내에 잔류하는 항생제의 농도는 1.0~10.0 mg kg-1의 범위이다 (Boxall et al., 2006; Ferro et al., 2010; Hillis et al., 2011). 항생제의 작물 전이는 항생제의 구조적 특징에 의해 발생한다. 대부분의 항생제는 이온화 될 수 있는 작용기를 가진 극성 분자이기 때문에 다양한 환경 변화 (pH, 수분, 및 미생물 활동 등)에 의해 이온화되어 작물로 전이 된다 (Pan and Chu, 2017).
작물로 전이된 항생제는 식물의 뿌리 또는 잎에서의 생리 작용에 저해를 나타낸다 (Hills et al., 2011; Michelini et al., 2012). 선행 연구에 의하면 설폰아마이드 계열의 항생제인 sulfadimethoxine이 작물에 전이되었을 경우 뿌리의 형태를 변형시켜 작물의 생장을 저해하였으며 (Michelini et al., 2013) sulfadiazine을 10, 200 mg kg-1의 농도로 토양에 인위적으로 주입한 후 작물을 재배하였을 때 잎에서는 탄질비 (C/N ratio)와 chlorophyll의 농도를 저감시켜 작물의 생장에 저해를 준다는 보고가 있다 (Michelini et al., 2012).
본 연구에서는 토양에서의 거동 특성이 다른 2종류의 항생제 종류인 테트라사이클라인과 설폰아마이드 계열의 항생제를 대상으로 토양에 인위적으로 주입한 후 작물에 흡수된 항생제의 잔류 특성과 작물의 생장에 대한 저해를 평가하였다.
Materials and Methods
시약 및 재료
동물용 항생제가 작물에 미치는 영향을 평가하기 위해 대표적인 동물용 항생제 계열인 테트라사이클라인 (tetracycline)과 설폰아마이드 (sulfonamide) 계열의 항생제 중 가장 많이 사용되는 클로르테트라사이클라인 (CTC, chlorotetracycline hydrochloride, 64-72-2, SIGMA-ALDRICH, USA)과 설파메타진 (SMZ, sulfamethazine, 57-68-1, SIGMA-ALDRICH, USA)을 사용하였다. 시료의 추출용매로 사용된 메탄올 (DAEJUNG, 67-56-1, Korea)과, 아세토나이트릴 (DAEJUNG, 75-05-8, Korea)은 HPLC 등급을 사용하였다. 고형상 추출법 (SPE, solid phase extraction)에 사용된 카트리지는 Oasis HLB 카트리지(Waters, 30 cc, 60 mg, USA)를 사용하였으며 내부 표준물질로는 simeton (P-501S, 100 µg mL-1, USA)을 사용하였다. 내부표준물질인 simeton은 10 mg L-1으로 희석하여 냉장보관 하였으며, 실험을 위해서는 0.24 mg L-1로 제조하여 사용하였다.
작물재배 시험
재배 시험에 사용한 토양은 충남대학교 농업생명과학대학 부속 농장 내 밭토양 (잔류 항생제의 농도가 검출 한계 미만)을 사용하였다. 토양 내 항생제 (CTC, SMZ)의 농도가 0.05, 0.5, 5.0 mg L-1이 되도록 습윤 토양 약 1.6 kg에 증류수 50 mL를 사용하여 균질화한 후 하루 동안 상온 보관하여 작물 재배 시험에 사용하였다. 재배 시험 작물은 적상추 (Lactuca sativa)로 선정하였으며 약 3 cm 자란 묘를 포트 (Φ23 × 18 cm)에 정식 후 총 5주 동안 시험 재배하였다 (Fig. 1). 대조구 (잔류 항생제 농도가 검출 한계 미만)를 포함한 각 처리구는 3반복으로 처리 후 임의배열 방식으로 배열하여 재배하였으며 매일 정해진 시간에 물주기를 실시하였다. 정식 후 5주가 경과한 뒤 재배가 끝난 적상추는 가식부와 뿌리로 분리하여 분석에 사용하였다. 토양의 경우 암조건에서 풍건한 뒤 2 mm로 체거름하여 분석에 사용하였다.
토양의 이화학적 특성 및 작물 생장 분석
토양의 이화학적 특성인 토양 pH, 전기전도도 (EC), 유기물함량, 유효인산에 대한 분석은 농촌진흥청 토양화학분석법에 준하여 실시하였다. 토양 pH 와 EC는 풍건토양 10 g에 증류수 50 mL를 가하여 1시간동안 150 rpm으로 진탕 후 Whatman No2 여과지를 이용하여 여과시켜 각각 pH (MP 220 Mettler Toledo, USA)와 EC (Mettler Toledo, S230, USA)기기를 이용하여 측정하였다. 유기물함량(Organic Matter)과 유효인산은 각각 Walkley & Black법과 Bray No.1법을 적용하였으며 함량 분석은 spectrophotometer (UVmini-1240, SHIMADZU)를 이용하여 660과 610 nm에서 비색정량 하였다.
작물의 생육 조사는 작물 재배가 끝난 뒤 각 처리구에서 엽장이 가장 긴 3장을 선별한 후 토양을 완전 제거하기 위해 가식부와 뿌리를 증류수로 3회 세척하였으며 뿌리의 경우 토양을 최대한 분리하기 위해서 초음파세척기 (Powersonic 420, Hwasin, Korea)를 활용하여 세척 후 생육조사를 실시하였다. 세척한 작물은 종이 타올을 이용하여 물기를 완전 제거한 후 한 장씩 분리하여 생중량과 엽장을 측정하였다.
토양 및 작물체의 항생제 분석
토양 및 작물체 내 잔류 항생제 분석은 풍건된 토양과 동결 건조 후 분말의 형태로 파쇄한 작물체 시료를 이용하였다. 추출 방법은 시료 (토양 1 g, 작물체 0.1 g)를 칭량하여 50 mL 원심 분리기용 튜브에 담은 후 Mcllvain Buffer 20 mL, 5% EDTA 250 µL를 넣은 후 진탕기 (JSOS-500, JSR, Japan)를 사용하여 150 rpm에서 15분간 진탕하였다. 진탕된 시료는 원심분리기 (MF 80, Hanil, Gimpo, Korea)를 이용하여 4,000 rpm으로 15분 동안 원심분리 후 상등액은 여과지 (0.45 µm)로 감압 여과하여 250 mL 삼각플라스크에 옮겨 담았다. 상등액을 분리한 후 남은 시료는 위의 추출방법을 1회 반복하여 동일한 플라스크에 수집 후 상등액 약 40 mL에 증류수 80 mL를 추가하여 총 120 mL가 되도록 한 후 최종적으로 0.2 µm Cellulose Acetate Membrane Filter (Adventec, Japan)를 이용하여 감압여과하고 그 여과액은 고형상 추출법으로 정제하였다.
고형상 추출법은 Oasis HLB Extraction Catridge (3 cc/60 mg, Waters, USA)를 사용하였다. 카트리지를 활성화 시킨 후 전처리가 끝난 시료를 Teflon Tube와 연결하여 카트리지에 항생물질을 포집한 후 초순수를 3 mL 씩 3회 흘려보내주어 카트리지를 세척하였다. 세척 후 각각의 튜브에 0.24 mg L-1 simeton 을 50 µL씩 넣어 준 후 카트리지에 methanol을 2.5 mL 씩 2번 가하여 항생물질을 용리 (elution)하여 튜브에 수집하였다. 용리된 항생물질은 질소농축기 (N-EVAP-11, OASYS, MA, USA)를 사용하여 항온 수조 50°C에서 50 µL까지 농축한 후 mobile phase A (0.1 formic acid + 99.9% HPLC grade water (v/v))를 70µL 넣고 진동 혼합 후 0.22 µm Nylon filter가 포함된 1.5 mL centrifuge (spin-x centrifuge tube filter, COSTAR, NY, USA)에 전량 넣고 15,000 rpm으로 3분 동안 원심분리 하였으며, 그 여과액 120 µL를 2 mL 갈색 vial에 옮겨 담고 –20°C 냉동고에 보관 후 분석에 사용하였다.
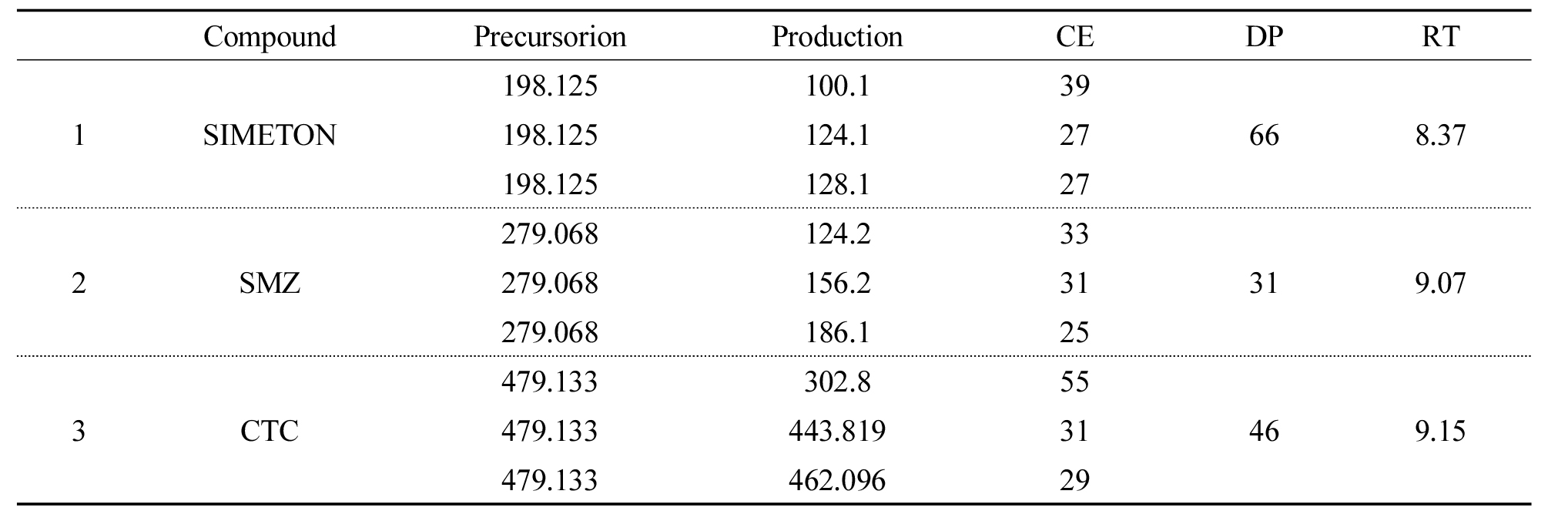
항생제의 분석에 사용된 기기는 충남대학교 공동실험실습관의 High Performance Liquid Chromatography Tandem Mass Spectrometer (HPLC/MS/MS, 4000 Q trap, ABSCIEX, CA)를 이용하여 분석하였다. 분석기기 조건 및 최적화된 생성이온은 Tables 1, 2에 정리하였다.
Table 1. Parameters of high performance liquid chromatography-MS/MS for quantification of veterinary antibiotics in soil and crops.
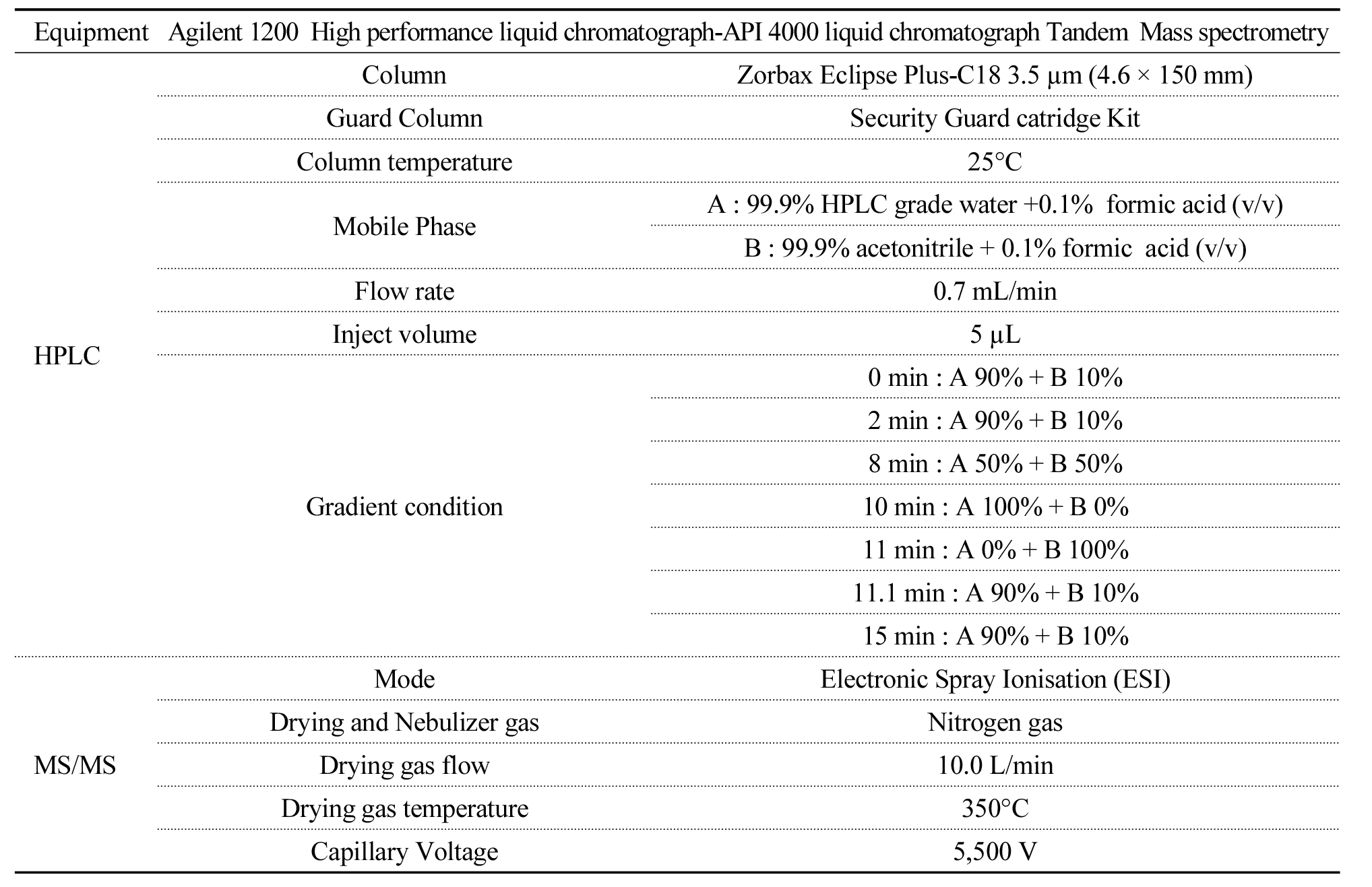
Table 2. Fragmented ions of four veterinary antibiotics depending on collosion energy and deculstering energy.
작물체 전해질 손실 (electrolyte leakage) 분석
항생제 농도에 따른 작물체의 전해질 손실량을 산출하기 위해 비이커에 3차 증류수 500 mL와 가식부 3장을 담은 후 6시간동안 150 rpm에서 교반하여 전기전도도 (EC)를 측정하여 초기 EC 측정값으로 정하였다. 그 후 가식부가 담긴 비이커를 90°C 오븐에 넣고 2시간 가열한 후 상온에서 냉각시켜 EC를 측정하였다. 각각의 초기 EC값과 오븐에서 가열한 후 측정한 EC값의 비율을 이용하여 항생제 농도에 따른 작물체의 전해질 손실을 분석하였다.
EC Leakage = (Initial EC value)CO / (EC value after heating at 90°C in oven)Ci (Eq. 1)
통계적 기법
본 연구에서 수행한 실험은 3반복으로 진행하였으며, 통계분석은 SPSS (IBM SPSS ver. 22) 프로그램을 사용하여 duncan’s multiple range test로 분석 후 각 실험 처리구간의 유의성을 검정하였다. 실험 처리구 간의 유의성은 95% 신뢰수준 (p=0.05)에서 분석하였다.
Results and Discussion
토양 특성 및 항생제 분석
QA/QC 작물 재배에 사용된 공시 토양의 화학적 특성은 토양 pH: 6.2±0.1, EC: 0.55±0.05 dS m-1, 유기물 함량: 8.44±0.87 g kg-1, 유효인산: 17.31±0.55 mg kg-1이었으며 토성은 사양토 (sandy loam)로서 작물 재배에 적합한 토양이었다. 토양과 작물체의 항생제 분석에 대한 회수율은 CTC의 경우 83%, 54% 였으며 SMZ의 경우 91%, 30%를 나타내었다 (Park et al., 2016). 선행연구의 경우 고압용매추출법을 사용하여 항생제를 추출하였을 때 약 46~52%의 작물체 내 항생제 회수율을 나타내었다. 검출한계 (Maximum Detection Limit)와 정량한계 (Limit of Quantification)는 CTC의 경우 0.19, 0.50 µg kg-1 과 SMZ의 경우 0.15, 0.04 µg kg-1로 산출되었다 (Park et al., 2016).
토양 및 작물체 내 항생제 농도
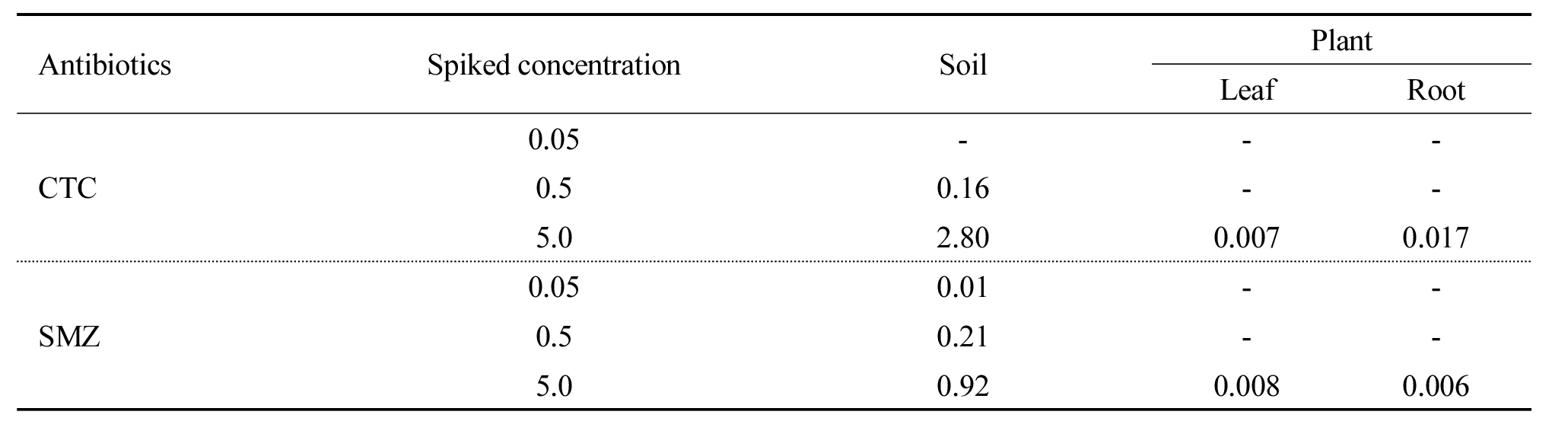
작물의 생육이 끝난 후 각 처리구의 토양 및 작물체 내 항생제의 농도는 Table 3에 나타내었다. 토양 내 잔류 농도는 초기 처리 농도에 따라 CTC의 경우 0.16~2.80 mg kg-1의 농도를 나타내었으며 SMZ의 경우 0.01~0.92 mg kg-1의 농도를 나타내었다. 두 종류의 항생제를 각각 5.0 mg kg-1 처리하였을 경우 SMZ보다는 CTC의 잔류 특성이 높은 것으로 나타났다. CTC를 5.0 mg kg-1의 농도로 처리하였을 경우 전체 농도의 약 56%인 2.80 mg kg-1의 농도가 잔류하였으며 SMZ의 경우 5.0 mg kg-1을 처리하였을 경우 약 2%인 0.92 mg kg-1의 농도가 잔류하였다. Boxall et al. (2006)의 연구에 의하면 CTC와 같은 테트라사이클라인 계열의 항생제는 2가 양이온과의 결합이 강하여 토양에 잔류하는 특성이 강하며 SMZ와 같은 설폰아마이드 계열의 항생제는 자연적인 토양 환경 조건에서 이동성이 높은 특성이 있다. 이와 같이 두 종류의 항생제가 고형상에 잔류하는 특성이 상이하여 같은 농도를 처리하였을 경우에도 서로 다른 토양 내 잔류 특성을 나타내었다.
작물로 전이되는 항생제의 농도를 조사한 결과 CTC와 SMZ 모두 0.05와 0.5 mg kg-1을 처리하였을 경우 작물체의 잎과 뿌리에서는 항생제가 검출되지 않았다. 하지만 CTC와 SMZ를 5.0 mg kg-1으로 처리하였을 경우 잎에서는 0.007, 0.008 mg kg-1이 검출되었고 뿌리에서는 0.017, 0.006 mg kg-1의 농도로 검출되었다. 작물체의 부위별 검출 농도는 통계적 유의성이 없었으며 작물체 내에서 가장 높은 항생제는 뿌리에서 검출된 CTC로 조사되었다. Pan and Chu (2017)의 총설 연구에 의하면 CTC와 SMZ의 작물체 내 검출 농도는 상추의 경우 잎에서 약 n.d-0.001, n.d-1.120 mg kg-1의 농도로 검출되었으며 뿌리에서는 두 종류의 항생제 모두 검출되지 않았다.
항생제 농도에 따른 작물 생장 영향
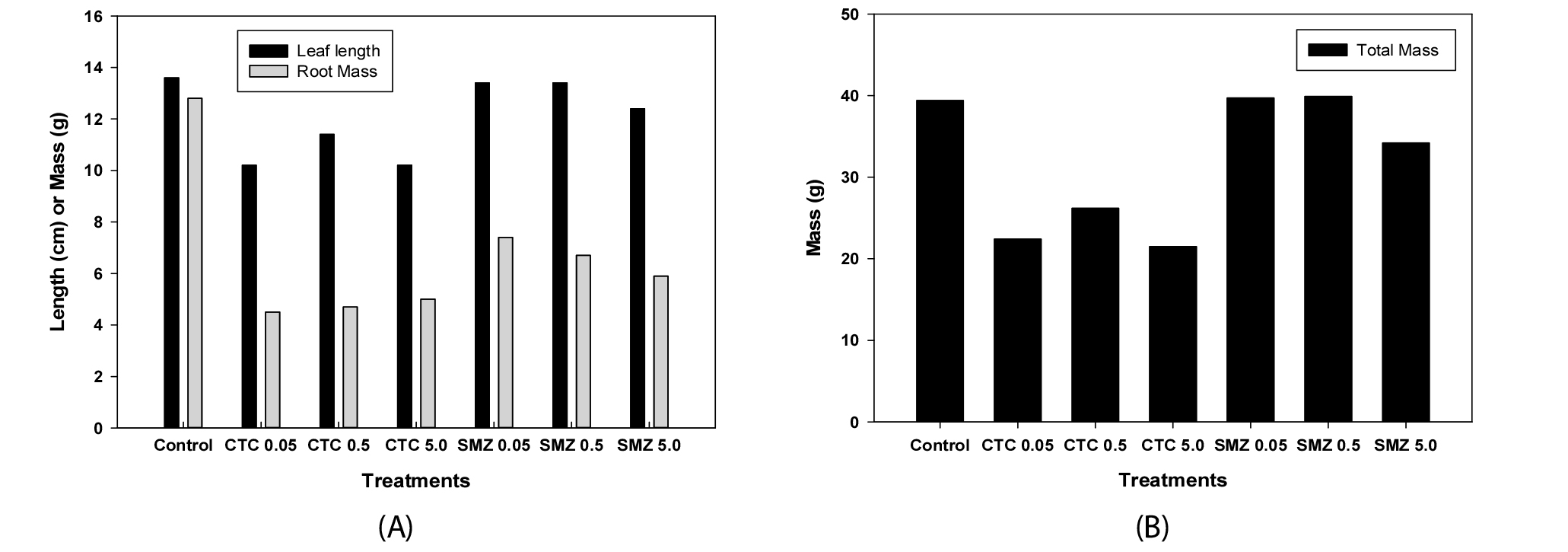
항생제의 농도에 따른 적상추의 엽장 길이와 뿌리 및 작물체의 전체 무게를 Fig. 2에 정리하였다. 각 처리구별 가장 긴 3장의 엽장 평균 길이 (cm)는 대조구: 13.6, CTC 0.05:10.2, CTC 0.5: 11.4, CTC 5.0: 10.2, SMZ 0.05: 13.4, SMZ: 0.5: 13.4, SMZ: 5.0: 12.4 였으며 엽장 길이의 경우 대조구와 각기 다른 농도를 처리한 항생제 처리구를 비교하였을 때 95% 신뢰수준에서의 통계적 유의성은 없었다 (p=0.07). 하지만 CTC의 경우 대조구와 비교하였을 때 엽장의 길이가 2.5~3.4 cm 정도 짧았으며 농도에 따른 경향은 나타나지 않았다.
작물의 생장 요소 중 뿌리의 무게와 전체 적상추의 무게는 대조구와 비교하여 CTC 처리의 경우 통계적으로 유의성이 있었으며 (p=0.02) SMZ의 경우 대조구와 비교하였을 때 통계적 유의성은 없었다 (p=0.21). Michelini et al. (2012)의 연구에 의하면 설폰아마이드 계열의 항생제인 sulphadiazine을 각각 10, 200 mg L-1의 농도로 처리하였을 경우 작물체 내 (Willow와 Maize)의 탄질비 (C/N ratio)와 클로로필의 함량이 각각 40~88%, 13~30% 정도 감소하는 결과를 도출하였다. 특히 sulphadiazine의 농도가 200 mg L-1를 처리하였을 경우 작물 생장의 저해가 더 뚜렷하였다. 고농도의 항생제를 처리하였을 경우 뿌리의 생장이 대조구에 비해 저해되었으며 그 결과 작물체 내 수분 흡수가 저하되어 작물의 생장이 저해됨을 보고하였다. 본 연구에서도 선행연구와 같이 CTC 처리구에서 뿌리의 생장에 저해를 나타내 전체 작물체의 중량이 대조구에 비해 통계적으로 유의하게 낮은 값을 나타내었다.
항생제 농도에 따른 전해질 누출
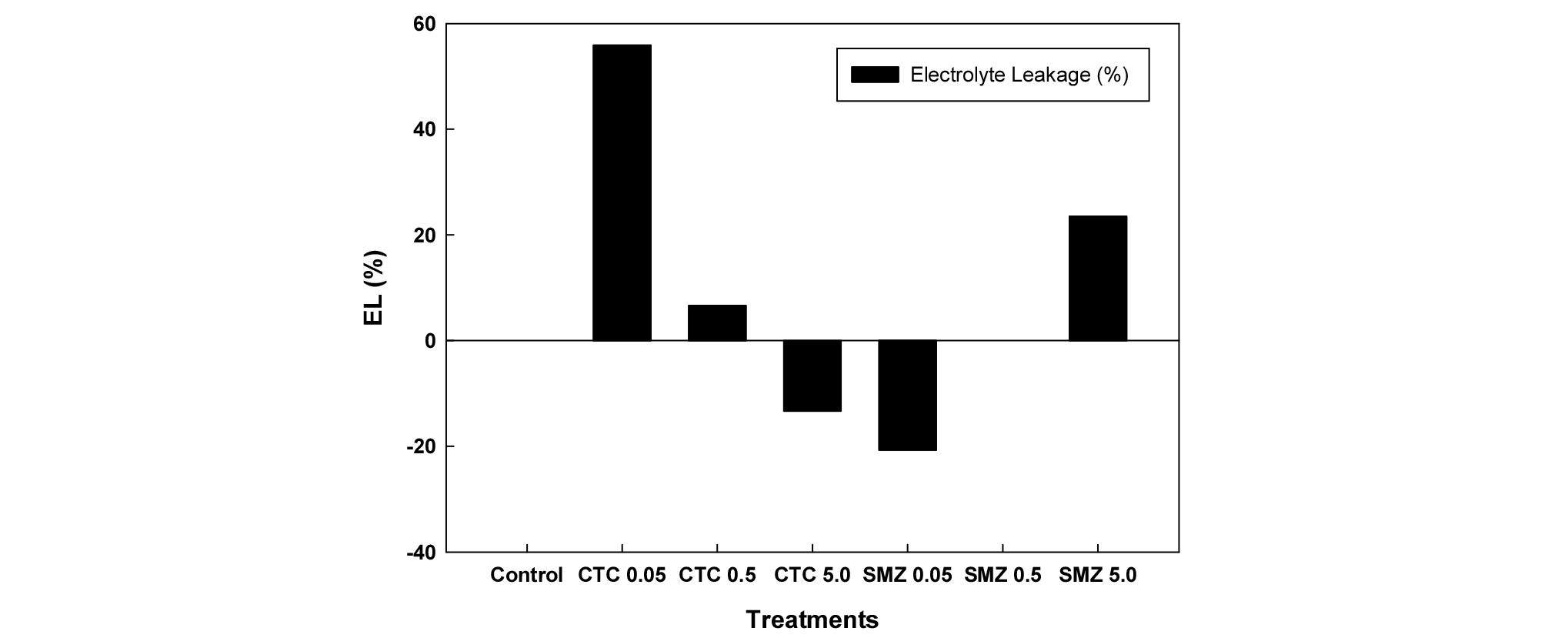
작물체의 스트레스에 따른 생장 저해 요인 중 전해질의 누출을 평가하기 위해 각 처리구의 전해질 누출비를 대조구와 비교하였다 (Fig. 3). 적상추 잎에서의 전해질 누출비를 평가한 결과 CTC의 경우 처리 농도에 따라 0.05 mg kg-1 (55.9%) > 0.5 mg kg-1 (6.6%) > 5.0 mg kg-1 (-13.3%)의 누출비를 나타냈으며 SMZ의 경우 5.0 mg kg-1 (23.5%) > 0.5 mg kg-1 (0.0%) > 0.05 mg kg-1 (-20.7%)의 누출비를 나타내었다. Michelini et al. (2013)의 연구에 의하면 설폰아마이드 계열의 항생제인 sulfadimethoxine (SDM)과 sulfamethazine (SZ)를 약 10 mg L-1로 처리하였을 경우 27시간이 지난 뒤 뿌리에서의 전해질 누출비가 대조구에 비해 56~92% 높았다. 이는 주로 K+ 이온의 누출에 의한 것으로 SDM과 SZ의 영향에 의해 뿌리 세포가 상해되어 결국 대조구에 비해 높은 전해질 누출비를 나타내었다. 본 연구에서는 누출된 전해질의 성분은 확인이 되지 않았으나 전해질 누출비가 가장 높았던 CTC 0.05 mg kg-1 처리구의 경우 엽면 길이 (10.2 cm)와 뿌리의 무게 (4.5 g)가 다른 처리구에 비해 가장 낮은 값을 나타내었다. 따라서 CTC의 경우 높은 농도 (5.0 mg kg-1)에 노출되었을 때보다는 오히려 낮은 농도 (0.05 mg kg-1)에 노출되었을 경우 작물 저해가 더 심한 것으로 나타났다. SMZ의 경우 CTC와는 반대로 높은 농도 (5.0 mg kg-1)에 노출되었을 경우 전해질 누출이 가장 높았으며 낮은 농도에서의 전해질 누출은 나타나지 않았다. 하지만 작물 생육적 측면에서는 전해질 누출이 가장 높았던 높은 농도에서의 엽면 길이 (12.4 cm)와 뿌리의 무게 (5.9 g)가 대조구의 엽면 길이 (13.6 cm)와 뿌리의 무게 (12.8 g)에 비해 낮은 값을 나타내었다. 이와 같이 CTC와 SMZ의 작물저해와 전해질 누출 양상이 농도에 따라 서로 다른 이유는 명확하지 않으나 Michelini et al. (2013)의 연구에 의하면 Kd값이 높을수록 작물의 뿌리에 저해가 크며 CTC와 SMZ를 비교하였을 경우 CTC의 Kd (L kg-1) 값이 약 680~1,030으로 STZ의 0.6~3.21 보다 훨씬 커서 SMZ 보다는 CTC의 작물 저해가 더 큰 것으로 사료된다 (Tolls, 2002). 또한 항생제의 특성 중 Kow 값이 높을 경우 소수성 특징이 있어 세포의 지질층에 잔류할 수 있는 확률이 높아 식물의 세포 발달에 저해를 미칠 수가 있다 (Michelini et al., 2013).
Conclusion
동물용 항생제의 토양 잔류에 따른 작물 생장의 저해를 평가하기 위해 2종류의 서로 다른 계열의 항생제인 CTC와 SMZ를 인위적으로 토양에 각각 0.05, 0.5, 5.0 mg kg-1으로 처리하여 항생제의 작물전이 및 생장저해를 평가하였다. 작물에 전이되는 항생제의 농도는 CTC와 SMZ 모두 고농도인 5.0 mg kg-1의 농도로 토양에 처리하였을 경우 잎에서는 0.007~0.008 mg kg-1, 뿌리에서는 0.006~0.017 mg kg-1의 낮은 농도가 검출되었다. 항생제의 작물 잔류에 따른 생장을 평가한 결과 SMZ의 경우 작물의 뿌리 및 잎의 생장에 저해가 적은 반면 CTC의 경우 높은 농도보다는 낮은 농도인 0.05 mg kg-1의 농도로 토양에 처리하였을 경우 뿌리의 생장 및 전체 작물의 무게에 가장 많은 저해를 나타냈다. 작물에 저해를 미치는 항생제의 가장 큰 특성은 Kow와 Kd의 특성에 따라 Kow 값이 높을수록 세포의 지질층에 잔류되어 세포의 발달에 저해를 미치며 Kd 값이 높을수록 뿌리 입자에 흡착되어 뿌리의 생장을 저해하게 된다 (Michelini et al., 2013). 본 연구의 결과를 바탕으로 동물용 항생제의 작물 저해 메커니즘을 이해하는 기초를 마련하였으며 추후 작물의 뿌리에 대한 형태 변화 또는 작물의 유전체 변이에 대한 연구가 필요할 것으로 사료된다.