Introduction
생강은 우리나라 음식에 많이 사용되는 향신료로 국내 생강 생산량은 2000년 989 kg 10a-1에서 2015년 1,418 kg 10a-1로 증가되었으며, 이후 일정 수준을 유지하고 있다 (KOSIS, 2025). 생강은 고온 다습한 조건에서 잘 자라며, 정식 후 토양이 건조해지지 않도록 주기적인 관개가 필요하고, 생육 기간이 길어 (4월 정식, 11월 수확) 추비를 2 - 3회 하여야 한다 (RDA, 2018). 이러한 재배 관리 방식을 고려하였을 때 관비는 노동력을 줄이고 (Lee et al., 2022), 양분 이용효율을 증대시켜 (Lee and Sung, 2023) 관행 무기질비료 시비의 대안이 될 수 있다. 하지만 생강 재배 시 관비 처리에 따른 생강 생육 및 토양 생물화학적 특성 변화에 대한 연구는 미흡하다.
토양 미생물 활성도 및 생체량과 토양 효소는 유기물 분해 및 양분 순환과정에서 능동적인 주체로서 핵심적인 촉매 역할을 한다 (Burns et al., 2013; Powlson, 1994). 자연 상태의 토양과 달리 인위적으로 관리되는 농경지의 비료 시비는 시비 방식에 따라 양분유효도, 수분함량, 뿌리 삼출물 등 토양 환경 변화와 함께 미생물 생체량과 효소 활성에 영향을 준다 (Moeskops et al., 2010). 적정량 시비는 양분유효도를 증가시키고, 관비는 토양 수분함량을 유지시켜 미생물과 효소 활성을 증가시킬 수 있다 (Wang et al., 2022). 반면, 많은 양의 비료를 한번에 주는 관행 무기질비료 시비는 급격한 양분 함량 증가로 인해 미생물에 스트레스로 작용할 수 있으며 (Geisseler and Scow, 2014), 무기 양분만 투입되고 미생물의 에너지원인 탄소는 공급하지 않아 미생물 생체량을 감소시킬 수 있다 (Cameron et al., 2013; Gong et al., 2009; Zhong et al., 2010). 특히 토양 효소 활성은 탄소, 질소, 인과 같은 원소의 화학양론에 의해서도 영향을 받는다 (Jian et al., 2016). 질소 시비로 토양의 질소 함량이 높아지면 질소 무기화 효소 활성은 낮아지고, 탄소와 인 무기화 효소 활성은 높아진다 (Jian et al., 2016). 또한 양분 유효도가 낮은 토양의 미생물이 제한된 양분을 획득하기 위해 효소 활성을 증가시키기도 한다 (Allison and Vitousek, 2005).
하지만 기존 연구는 시비 방식에 따른 양분 이용 효율 평가에 집중되어, 토양의 생물학적 지표 (MBC 및 효소 활성)의 변화에 대한 연구는 부족하다. 따라서, 본 연구는 관행 무기질비료 시비와 관비에 따른 노지 밭의 미생물 생체량과 토양효소 활성의 변화를 조사하고자 수행하였다. 연구 목적에 따라 조사되는 효소 활성의 종류는 다양하지만, 본 연구에서는 탄소 순환과 관련된 β-1,4-glucosidase (BG) (Deng and Tabatabai, 1994), 질소 순환과 관련된 β-1,4-N-acetylglucosaminidase (NAG) (Parham and Deng, 2000), 인 순환과 관련된 acid phosphatase (AP) (Tabatabai and Bremner, 1969) 효소 활성도 변화를 평가하였다. 일반적으로 무기질비료보다는 관비의 높은 양분 이용 효율은 미생물 증식 및 활동에 유리하게 작용하는 연구 결과를 반영하여, 관비 처리에 의한 미생물 생체량 및 토양 효소 활성이 관행 무기질비료 처리에 비해 증가할 것으로 가설을 설정하였다.
Materials and Methods
포장 실험 및 시료 채취
본 연구는 생강의 주요 생산지 중 하나인 전북특별자치도 완주군 봉동읍에 위치한 노지 밭 (25.944311°N, 127.148862 °E)에서 2024년 5월 3일부터 10월 22일까지 생강 재배 실험을 통해 수행하였다. 연구지역 지난 30년 (1993 - 2023) 평균 기온은 12.5 °C, 평균 강수량은 1305.5 mm이었다 (KMA, 2025). 포장 시험 전 표토 (0 - 30 cm) 토양 초기 화학성은 pH (1:5) 6.53, 유기물 16.61 g kg-1, 유효인산 136.8 mg kg-1으로 나타났으며, 토성은 모래, 미사, 점토의 비율이 각각 46.8%, 39.0%, 14.2%인 양토 (loam)로 양호한 배수성과 통기성을 가지고 있었다 (Table 1). 토양 화학성과 물리성 모두 생강 재배 적지로 판단되었으며, 초기 토양 화학성을 이용하여 계산된 생강 검정시비량은 24-13.5-16.3 (N-P-K) kg 10a-1이었다.
Table 1.
Selected properties of soil used.
| Variables1 | Values | |
| Particle size distribution (%) | Sand | 46.8 |
| Silt | 39.0 | |
| Clay | 14.2 | |
| Texture | Loam | |
| Bulk density (mg m-3) | 1.3 | |
| pHwater | 6.53 (0.01) | |
| Organic matter (g kg-1) | 16.61 (0.08) | |
| Available P (mg P2O5 kg-1) | 136.8 (1.6) | |
| Exchangeable cations (cmolc kg-1) | Ca | 4.38 (0.04) |
| Mg | 0.94 (0.01) | |
| K | 0.18 (0.00) | |
| Na | 0.09 (0.00) | |
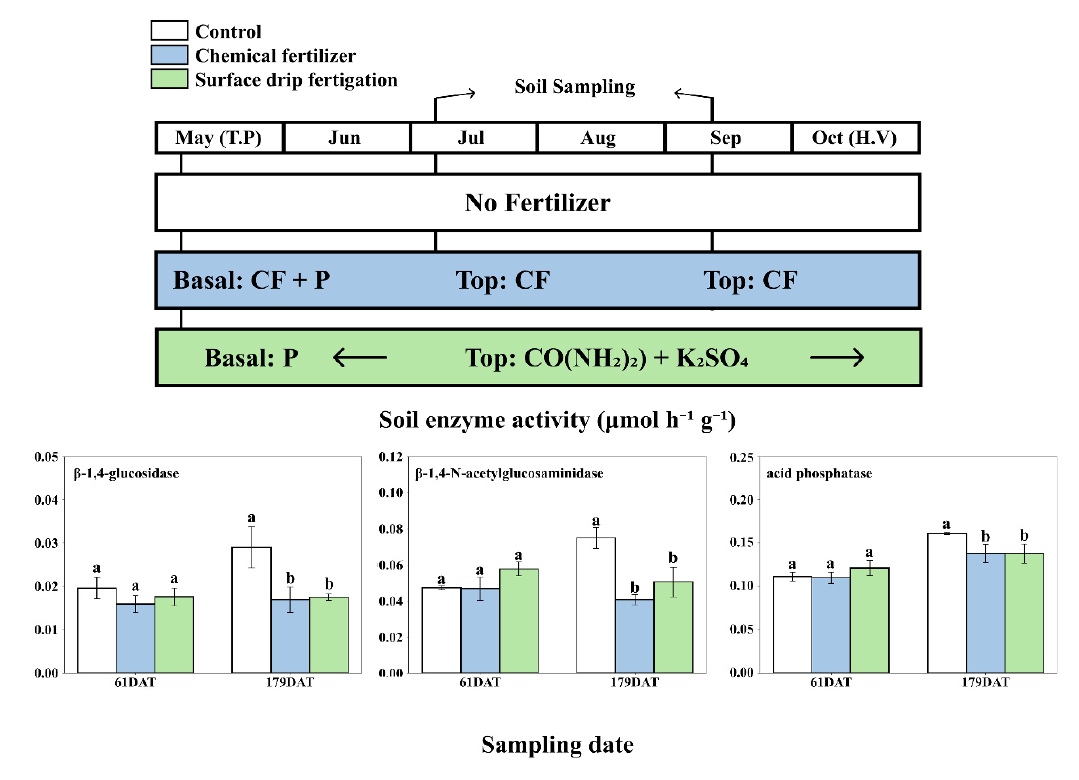
실험 포장은 무처리 (control, C)와 관행 무기질비료 (chemical fertilizer, CF), 그리고 관비 (surface drip fertigation, SDF)로 단구제 3반복 구성하였다. 각 처리구의 면적은 45 × 1.2 m이며, 처리구 간 0.4 m의 완충 구역을 설정하였다. CF 처리구는 시중에 판매하는 무기질비료 (12-6-8, N-P-K)를 2024년 4월 26일에 밑거름으로 처리구당 38.89 kg 10a-1를 표층 시비한 후, 7월 3일, 9월 10일 (2회)에 웃거름으로 처리구당 64.03 kg 10a-1을 표층 시비 (15-1-12, N-P-K)하였다. 생강의 최적 인산 요구량을 충족하기 위해 시중에 판매하는 인산가리 (0-52-34, N-P-K)를 처리구당 21.39 kg 10a-1 추가로 밑거름과 동일한 날에 표층 시비하였다. SDF 처리구에는 시중에 판매하는 요소 (N: 46%)와 황산가리 (K: 50%)를 사용하여 CF 처리구와 동일한 질소 시비량으로 시비하였다. 토양 검정 시비량 기준 (요소: 5.28 kg 10a-1, 황산가리: 3.19 kg 10a-1)으로 비료를 물 300 L에 희석시켜 원형 인라인 점적관 (지표 설치형)을 이용해 점적 관수 시비하였다. SDF 처리구도 CF 처리구와 같이 부족한 인을 보충하기 위해 인산가리를 밑거름으로 처리구당 25.97 kg 10a-1 표층 시비하였다 (Table 2). C 처리구와 CF 처리구의 관수는 SDF 처리구의 관비 일정 (12일 간격, 10회)에 맞춰 동일한 양 (300 L)의 물을 점적 관수하였다.
Table 2.
Fertilization management for each treatment.
토양 시료 채취 및 분석
토양 시료는 정식 후 61일 (61DAT)과 179일에 각 처리구 반복 별 3지점에서 표토 (0 - 20 cm)를 오거를 사용해 채취하였다. 채취한 시료는 아이스박스에 담아 실험실로 운반한 뒤, 분석 전까지 냉동 (-23°C)보관하여 토양 수분을 유지하였다. 토양은 습윤 상태로 2-mm 체질 후 분석하였다.
미생물 생체량을 측정하는 방법은 다양하지만 클로로포름 훈증-추출법 (Vance et al., 1987)으로 분석 가능한 미생물 생체량 탄소 (microbial biomass carbon, MBC)를 측정하여 시비 종류에 따른 미생물 생체량 변화를 측정하였다. 두 세트 습윤 토양 10 g을 준비하여 훈증 시료는 진공 데시케이터 내에서 암흑을 유지한 상태에서 상온에서 24시간 훈증 후 40 mL 0.5 M K2SO4 용액으로 추출하였다. 비훈증 시료는 훈증시료 훈증 시작과 동시에 K2SO4 용액으로 추출하였다. 최종 추출액 내 MBC를 총유기탄소 분석기 (TOC-L, Shimadzu, Japan)로 분석하였다. MBC는 훈증 전/후 건조토양 기준 탄소 농도 차이로 계산하였다.
토양 효소 활성도는 Sinsabaugh et al. (2003)의 분석법을 따라 분석하였다. 1 g의 습윤토를 250 mL HDPE bottle에 담아 sodium acetate buffer (50 mmol L-1) 125 mL를 투입하여 실온 상태에서 150 rpm으로 30분 동안 교반하였다. BG, NAG, 그리고 AP 활성도 분석을 위해 균질화 된 시료를 96웰 마이크로 플레이트에 각 200 µL 옮겨 담아 기질발현 물질 50 µL (200 µmol L-1)을 피펫팅하여 첨가 후 각 효소마다 3, 3, 2 시간 동안 암흑에서 항온 (20°C) 배양하였다. 배양 후 각 웰에 20 µL 0.5 mol L-1 NaOH을 주입하여 효소 반응을 멈춘 후 360 nm와 460 nm 파장에서 다기능 마이크로 플레이트 리더 장치 (SpectraMax iD3, Molecular Devices, USA)로 형광 정량하여 분석하였다.
통계분석
시비 방식에 따른 토양 효소 활성도 및 MBC의 통계 분석을 위해 Python 3.12.3 (Python Software Foundation, Wilmington, DE, USA)을 이용하여 분산의 동질성과 분포의 정규성을 확인하였다. 데이터에서 이질성은 발견되지 않았고, 정규적인 분포를 가지고 있었기 때문에 데이터 변환은 수행하지 않았다. 일원 분산분석 (One-way ANOVA)을 수행하였으며, Tukey의 HSD 검정을 이용한 사후분석을 수행하였다.
Results and Discussion
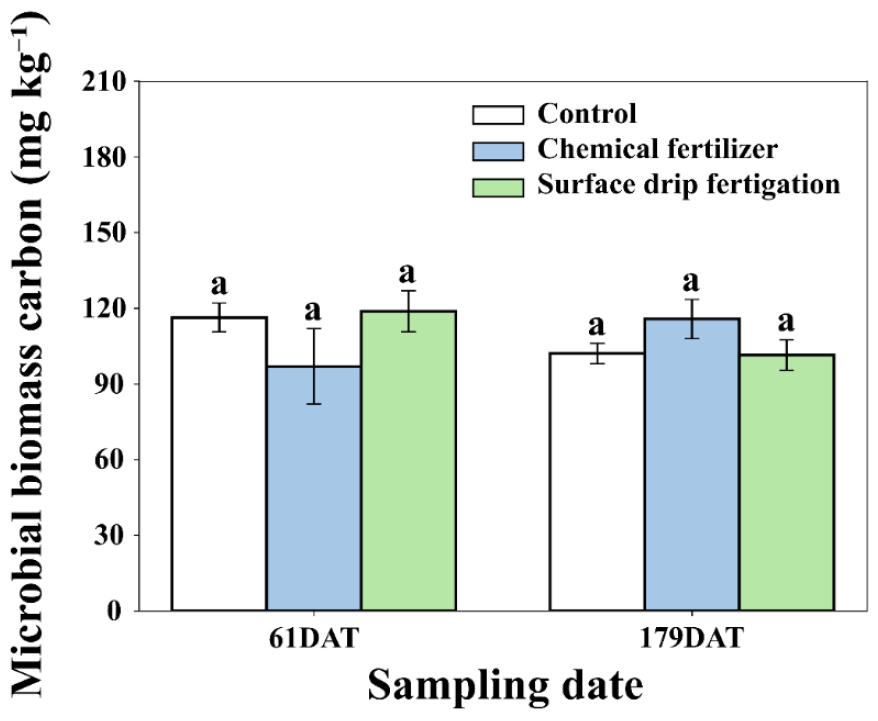
생강 정식 61일 (96.9 - 118.7 mg kg-1)과 179일 (101.4 - 115.7 mg kg-1) 후 MBC는 생육 시기 및 시비 방법에 따른 유의한 차이가 없었다 (Fig. 1). 생물 생체량 및 활성도는 수분함량 (A’Bear et al., 2014; Davidson and Janssens, 2006; Steinweg et al., 2012), 온도 (Allison et al., 2010; Baek et al., 2024; Qi et al., 2016; Wei et al., 2019), 유기물 투입 및 양분 함량 (García-Ruiz et al., 2009; Moeskops et al., 2010)과 같은 토양 조건의 영향을 받는다. 본 연구에서는 관비와 관수로 인해 토양 수분 함량이 모든 처리구에서 일정하게 유지되었다. 또한, 모든 처리구에서 유기물 투입없이 무기질비료 처리 유무 및 처리 방법만 차이가 있었다. 그 결과 토양 화학성이 처리구 간 유의미한 차이를 보이지 않았으며 (Table 3), 처리구 간 시료 채취 시기에 따른 MBC의 차이를 보이지 않은 것으로 판단된다. 또한, 생육 초반 (61DAT) 토양 시료는 첫 밑거름 시비일 이후 68일이 지난 후 채취하였으며, 수확기 (179DAT) 토양 시료는 마지막 웃거름 시비일 이후 49일, 마지막 관비 시비일 이후 11일이 지난 시점이었다. 이러한 시간 동안 작물의 흡수 및 손실로 인해 처리구 사이에 시비로 인한 양분 유효도 차이는 감소하고 미생물 활성 및 MBC에 대한 영향이 상쇄된 것으로 판단된다 (Geisseler and Scow, 2014).
Table 3.
Changes in soil chemical properties at 61 and 179 days after transplanting (DAT).
|
Sampling date | Treatment | pH1:5 |
EC1:5 (ds m-1) |
Organic matter (g kg-1) |
NH4+ (mg kg-1) |
NO3- (mg kg-1) |
Av. P2O5 (mg kg-1) | Exch. cations (cmolc kg-1) | |||
| Ca | Mg | K | Na | ||||||||
| 61 DAT | Control |
6.71 (0.06) |
0.61 (0.01) |
18.9 (0.3) |
3.59 (0.34) |
3.36 (0.32) |
215.4 (5.2) |
1.12 (0.01) |
0.40 (0.01) |
4.45 (0.06) |
0.09 (0.0) |
| CF1 |
6.22 (0.05) |
0.65 (0.03) |
19.1 (0.3) |
2.24 (1.03) |
2.01 (0.44) |
241.6 (5.3) |
0.92 (0.01) |
0.50 (0.01) |
3.95 (0.04) |
0.06 (0.0) | |
| SDF2 |
6.63 (0.07) |
0.61 (0.02) |
18.6 (0.3) |
5.16 (0.70) |
1.89 (0.10) |
290.0 (4.4) |
1.04 (0.03) |
0.48 (0.01) |
4.12 (0.08) |
0.09 (0.0) | |
| 179 DAT | Control |
6.52 (0.05) |
0.54 (0.01) |
19.3 (0.7) |
6.25 (0.63) |
0.14 (0.08) |
179.9 (3.6) |
1.03 (0.02) |
0.27 (0.03) |
4.16 (0.07) |
0.08 (0.01) |
| CF |
5.65 (0.07) |
0.89 (0.08) |
18.7 (0.5) |
6.95 (0.40) |
0.42 (0.05) |
198.8 (4.3) |
0.76 (0.01) |
0.28 (0.01) |
3.56 (0.05) |
0.05 (0.0) | |
| SDF |
6.23 (0.13) |
0.91 (0.11) |
18.1 (0.4) |
5.60 (0.52) |
0.26 (0.08) |
228.7 (8.5) |
0.99 (0.04) |
0.32 (0.03) |
4.06 (0.14) |
0.07 (0.0) | |
탄소, 질소, 인 순환 관련 효소 활성도는 생육 초기 처리구 간 차이가 없었으며, 수확기에 무처리구에서 무기질비료 처리구나 관비 처리구에 비해 유의미하게 높게 나타났다 (Fig. 2). 토양 효소는 미생물, 식물 뿌리, 잔재물 분해 과정에서 생성되어 양분의 무기화와 유효도 조절에 핵심적 역할을 한다(Burns et al., 2013). 즉, 양분 유효도가 낮을 경우 미생물과 식물이 부족한 양분을 확보하기 위해 효소 생산을 촉진시키며, 양분 유효도가 높을 경우 효소 활성도는 감소한다 (Allison and Vitousek, 2005; Geisseler and Scow, 2014; Jian et al., 2016). 수확기 토양 효소 활성도가 무처리구에서 무기질비료 처리구나 관비 처리구에서 높게 나타난 것은 비료를 시비하지 않아 부족한 양분을 확보하기 위해 효소 활성도가 증가한 것으로 판단된다 (Allison and Vitousek, 2005). 무기질비료 처리보다는 유기질 비료 처리에 의해 기질 유효도가 증가하고 MBC와 효소 활성도가 증가하는데 (García-Ruiz et al., 2009; Moeskops et al., 2010), 본 연구에서는 유기물 투입이 이루어지지 않고, 무기질비료 처리에 의한 양분 유효도 차이가 미비하여 MBC와 효소 활성도 차이가 미미한 것으로 판단된다.
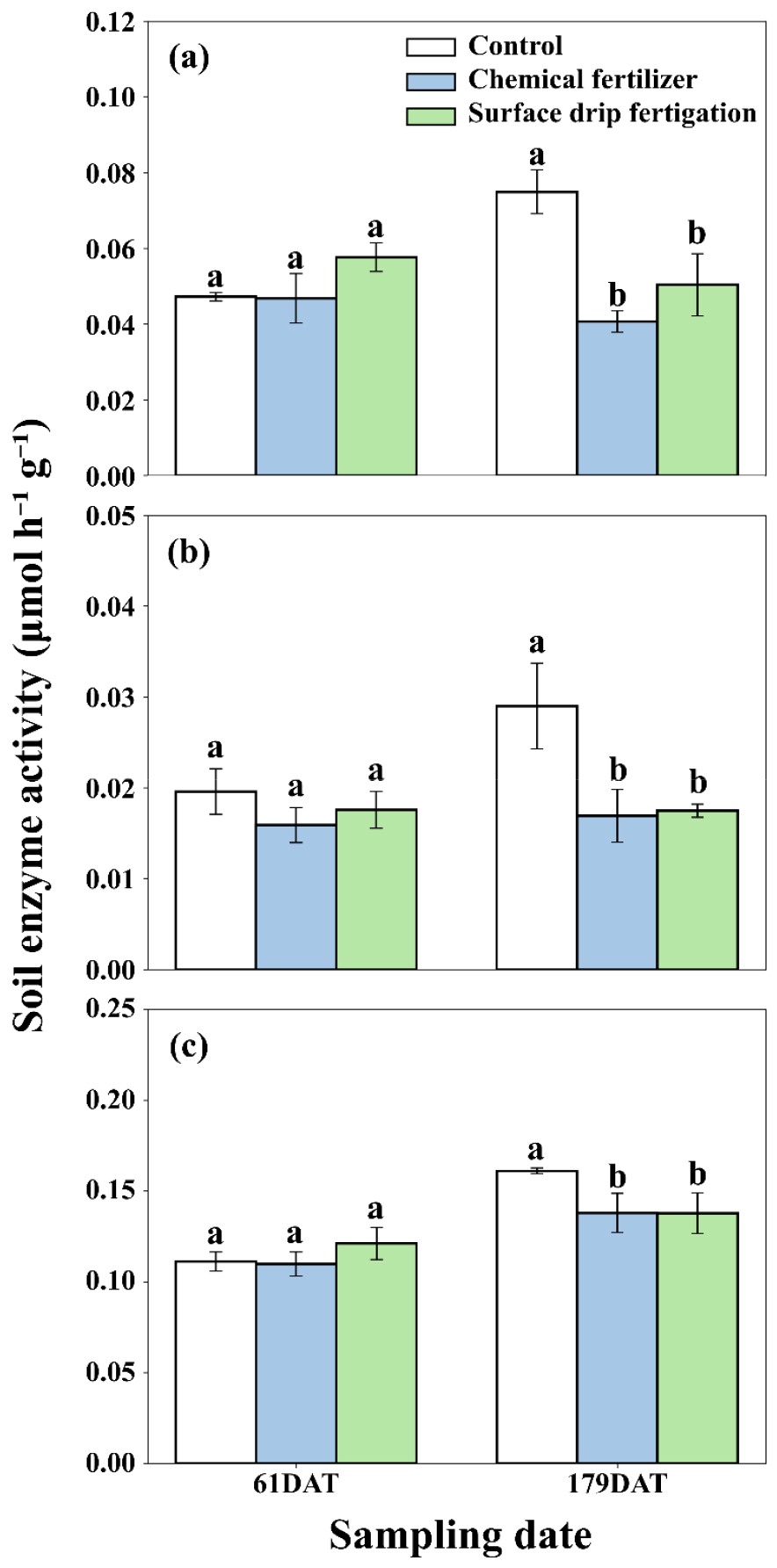
Fig. 2
Changes in the enzyme activities of soils at 61 and 179 days after transplanting (DAT): (a) β-1,4-glucosidase, (b) β-1,4-N-acetylglucosaminidase, and (c) acid phosphatase. Abbreviations: error bars indicate standard error and bars with the same lowercase letters are not significantly different at p < 0.05.
Conclusions
본 연구 결과, 노지 생강 포장에서 관행 무기질비료와 관비는 생육 초기 (61DAT)와 수확기 (179DAT) 모두 MBC와 탄소, 질소 및 인 순환 관련 효소 활성은 유의미한 차이를 보이지 않았다. 이는 관수와 관비를 통해 적정 수분함량이 유지되고 유기물 투입이 이루어지지 않았으며, 양분유효도가 비슷하였기 때문으로 판단된다. 하지만 수확기 (179DAT)에는 비료 시비가 없었던 무처리구의 효소 활성이 비료를 시비하였던 무기질비료 처리구와 관비 처리구보다 유의미하게 높은 것으로 나타났다. 관비는 관행 무기질비료와 비교하여 생물학적 지표 변화에 차이가 없지만 노동력 절감 측면에서 유리한 시비 전략으로 판단된다. 본 연구는 시비 시점과 토양 샘플링 시점의 차이, 유기물 투입 여부 등으로 인한 결과 해석 한계가 있다. 따라서 시비 조건에 따른 토양 미생물 및 효소활성도를 평가하기 위해서는 적절한 토양 샘플링 시기를 통해 시비 효과가 반영될 수 있도록 평가하고, 다양한 비종 (유기질비료 vs 무기질비료) 처리를 적용하여 생육 시기별 조사 및 평가가 필요할 것으로 판단된다.