Introduction
비소는 환경에서 인간 활동이나 지구과학적인 급원으로부터 유래되는 가장 해로운 물질 중 하나이다 (Kim and Sahoo, 2013; Smith et al., 1999). 미국 환경보호청 (US EPA)에서는 비소를 피부, 폐, 간, 방광, 신장의 암을 유발하는 A급 인체발암물질로 분류하고 있으며, 심장혈관, 신경, 혈액, 호흡기관 질환을 일으킬 정도로 인체 건강에 심각한 영향을 미치는 물질로 보고하고 있다 (US EPA, 1998; Abernathy et al., 1999; Tchounwou et al., 2003; Ng et al., 2003; Johnson et al., 2010; Martinez et al., 2011).
비소는 지구 생화학적 자연 발생으로 암석 및 용수에 존재하고, 광산, 제련, 살충제, 제초제, 비료, 오수, 목제 방부제등과 같은 인위적인 투입에 의해 발생한다 (Duker et al., 2005; Mandal and Suzuki, 2002). 특히 국내 농경지 비소 오염의 주요 원인은 자연발생 비소오염 농업용수와 폐광산의 침출수 둥 광산 폐기물이며 (Kim et al., 2010), 강우나 바람에 의해 이동하여 토양 및 농경지로 확산된다. 비소가 농경지로 유입되면 식물로 흡수 및 축적이 되어 식물의 줄기와 뿌리의 생장억제, 잎의 황백화 및 위조 등 다양한 생리대사 장해를 일으킨다 (Adriano, 1986; Kabata-Pendias and Pendias, 1984).
최근 국제식품규격 (Codex Alimentarius) 오염물질분과위원회 (Codex Committee of Contaminants in Foods)에서 백미 및 현미 중 무기비소 권장기준이 2014년과 2016년 각각 0.2 mg kg-1과 0.35 mg kg-1으로 설정되면서 쌀에 대한 비소의 안전성에 관심이 증가하고 있다 (CAC Report, 2014; CAC Report, 2016). 국내 폐광된 금속 광산은 약 2,000개가 있으며 (MIRECO, 2013), 폐광산 인근 농경지 중 우려기준을 초과한 논은 106곳, 밭은 101곳으로 조사되었다 (MOE 2012). 또한 식품의약품안전처에서 전국 44개의 폐광산 인근 농경지에서 재배된 쌀 757점의 비소를 분석하였는데 평균 0.27 mg kg-1 (0 ~ 4.35 mg kg-1)의 범위를 나타내는 것을 보았을 때 이는 Kunhikrishnan et al. (2015)이 전국 쌀 주산단지 82지역에서 조사한 현미 평균 비소 함량 0.15 mg kg-1 (0.04 ~ 0.38 mg kg-1)보다 높은 수치를 보여 비소의 오염을 확인하였다.
비소로 오염된 폐광산 및 공단 인근 농경지에서 안전한 농산물을 재배하기 위해서는 토양 중 비소함량을 기준으로 농경지 관리방안을 계획하여야 하고, 이를 실행하기 위해 ‘농작물 비소 흡수 예측 모델식’을 개발하는 것이 필요하다. 농작물 비소 흡수 예측 모델식 관련한 선행 연구에서는 토양 중금속 총 농도와 토양 pH, 유기물 함량과 같은 토양 특성인자와의 상관성을 고려하여 중금속 오염 농경지의 식물 유효태 예측 모델식 개발하였고, 중금속 이동성 해석 및 생태계 위해성 평가에 이 모델식을 이용하려 하였다 (De Vries et al., 2011; Groenenberg et al., 2010). Kim et al. (2014)은 우리나라 폐광산 인근 농경지를 중심으로 중금속 오염 농경지의 식물 유효태 예측 모델식 개발을 하였다. 카드뮴, 구리, 납, 아연을 기준 원소로 정하였고 추출용액을 달리하여 중금속 오염 농경지 토양의 유효도를 측정하였고 중금속 유효도에 영향을 미치는 토양 특성을 조사하여 그것을 바탕으로 중금속 유효도 유추 모델식을 개발하였다. 그 결과로 카드뮴의 식물유효태 함량은 카드뮴 전함량과 토양 pH 두 인자에 의해서 결정하고, 납과 아연에서도 토양 pH는 식물 유효태 함량에 영향을 미치는 등 토양특성 중 토양 pH와 유기물이 식물 유효태 농도를 유추하는 중요한 변수로 확인되었다. 연구에서 도출된 모델식은 국내 중금속 오염 농경지 토양에 적용 가능할 것으로 판단하였고 관리 대상 지역의 토양 특성을 반영한 ‘토양 내 중금속 유효도 유추 모델식’ 개발의 필요성을 확인하였다. 또한, 국제적으로 Huang et al. (2006)은 17종의 식물 내 비소 함량과 토양의 비소 총 함량 간의 상관성을 조사하였고 그 결과 벼를 포함한 9종의 식물 내 비소 함량은 토양 총 비소 함량과 상관성이 낮은 것으로 나타났다. 그리하여 토양 총 비소 함량만으로 식물 전이량을 예측하기 어려운 실정이다. 또한 많은 연구에서 식물의 중금속 및 비소 흡수가 토양 중 중금속 및 비소의 총함량 보다는 유효태 함량과 정의 상관관계가 있음을 보고하였다 (McLaughlin et al., 2000; Kim et al., 2012). 그러나 농경지 토양의 비소 관리에서 유효도라는 개념이 일반화 되어 있지 않고, 토양 특성을 고려한 농작물 비소 흡수 예측 모델식이 제시된 연구사례가 부족하다. 그리하여 국내에서도 다른 국가들과 같이 토양 내 비소 유효도를 이해하고 그것에 영향을 미치는 토양특성을 관리하여 유효도를 저감시키는 관리방안이 필요하다 (Kim et al., 2007; Wang et al., 2004). 따라서 본 연구에서는 폐광산 및 공단 인근 비소오염 농경지의 안전한 농산물 생산과 효율적인 토양관리방안을 모색하고자 현미 중 비소함량과 토양 비소 총 함량, 비소 유효태 농도, 토양 특성 인자간의 상관관계분석 및 다중회귀분석을 실시하였고, 이를 바탕으로 현미 중 비소 함량 예측 모델식을 제시하고 검증하고자 하였다.
Materials and Methods
대상지역 및 토양시료 채취조제 본 연구에서는 우리나라 비소오염 취약농경지로써 기존의 연구결과에서 조사된 농경지 토양, 농업용수 및 현미 중 비소함량이 상대적으로 높은 3지역을 대상으로 총 46지점 논토양에서 토양을 채취하였고, 농산물 (현미)는 토양 채취와 동일한 지점에서 수확기에 채취하였다. 토양은 음건 후 고무망치를 이용해 뭉쳐진 부분을 분리시켜 2 mm로 체질한 후 토양의 일반 화학성 분석시료로 사용하였고 토양 pH, 유기물, 유효태 인산, 점토 등 성분분석은 농촌진흥청 분석법 (NAAS, 2010)을 근거하여 실시하였다. 알루미늄산화물 함량은 암모늄옥살산 침출법으로 침출 여과 후 ICP-OES (GBC XMP, Australia)으로 측정 하였다 (Schwertmann, 1973; Lim et al., 2014). 또한 2 mm로 체질한 시료 소량을 채취하여 막자사발로 곱게 마쇄한 다음 100 메쉬 표준체로 다시 체질한 후 중금속 분석시료로 사용하였다.
토양 중 비소함량 분석 토양 중 비소 전함량은 토양오염공정시험법 (MOE, 2010)인 환류냉각장치 (Kjeldatherm) (C. Gerhardt GmbH & Co., Northants, UK)를 이용하여 반응 용기에 토양 3 g을 칭량하여 왕수 (염산 21 mL, 질산 7 mL / 3:1 비율 + 증류수 1 mL)를 주입하여 반응시간은 30°C에서 2시간 침지 후, 서서히 온도를 높여 90°C에서 2시간 가열하였다. 이후 냉각과정을 거쳐 분해 후 여과하였고 0.5 M 질산으로 100 mL로 정용하여 ICP-OES (GBC Integra-XMP, Braeside, Australia)를 이용하여 분석하였다. 토양 중 비소의 식물 유효도를 평가하기 위해 쌀의 비소흡수와 상관성이 있는 것으로 보고된 단일추출법 4종 (1.0 M NH4NO3, 0.01 M Ca(NO3)2, Mehlich 3, 1.0 N HCl)을 선정하여 실행하였다. Seo et al. (2013)은 0.01 M CaCl2 추출법을 보완한 방법으로 0.01 M Ca(NO3)2 추출법을 제안 하였고, 1 N HCl 추출법은 환경부의 토양오염공정시험법 중 중금속 분석법이 총 함량 분석법으로 단일화되기 전에 사용하던 추출 방법으로 비소의 경우 가용성 함량을 분석하였다 (MOE, 2002). 또한, 독일에서 농경지 관리를 하는데 사용되는 방법인 1.0 M NH4NO3 (DIN, 1995) 추출법을 선택하였다. Mehlich (1984)는 유효태 비소 함량을 측정하기 위해 Mehlich 3 추출법을 이용하였다. 추출 후 ICP-OES로 측정하였다.
쌀 (현미) 시료 채취 및 조제 수확기 쌀 시료는 토양 시료채취와 동일한 지점에서 시료를 채취하였다. 수확한 쌀 시료를 풍건한 후, 드라이오븐에서 60°C에서 하루 건조 후 현미기(SYTH88, Ssangyong Instrument, Korea)를 이용하여 도정 한 뒤 1분 동안 자동 균질기를 사용하여 고운 가루로 빻아서 실온에 보관하였다. 건조한 쌀 시료 0.25 g을 고압 폴리테트라플로로에틸렌 (PTFE) vessel로 옮긴 후, 8 mL 70% HNO3 (Sigma, USA), 1 mL H2O2 (Sigma, USA)를 각각 주입하였다. 모든 vessel은 screw cap으로 밀봉하여 설정된 프로그램에 의해 microwave digestion system (ETHOS, Milestone, Italy)를 이용하여 180°C에서 20분간 산 분해를 수행하였다. 산 분해 후, vessel용기를 상온에서 충분히 냉각시킨 후 얻은 분해액을 0.45 µm의 여과지로 여과한 다음 초순수 증류수로 25 mL까지 정용하여 분석 시료로 사용하였다.
토양 및 현미 중 중금속 분석 중금속 함량 분석을 위해 각각의 중금속 표준원액 (Merck, Germany) 1,000 mg L-1 stock solution을 구입 후, 2% HNO3 용액으로 희석하여 0.1 ~ 50 µg L-1 농도범위로 조제하였고, 토양은 ICP-OES로, 농산물은 ICP-MS (Agilent technologies, 7500a)로 분석하였다. 분석법 검증을 위해 시료를 분석하는 동안 standard reference material (SRM)인 쌀가루 (NIST 1568a)를 이용하여 정확도를 검증하였고, spiked 시료에 대한 회수율을 측정하여 80 ~ 120% 사이의 결과를 확인하였다.
토양 및 현미 중 비소함량 상관성 및 예측모형식의 적합성 분석 토양과 농산물 내 비소 함량간의 상관성 검토는 상관계수 (r) 산출을 위한 상관관계분석과 조정된 결정계수 (adj R2) 산출을 위한 단순선형회귀분석으로 구분하여 실시하였다 (Koh et al., 2013). 토양 화학적 특성과 비소 전 함량, 식물 유효태 및 현미 비소 함량간의 단순상관분석과 다중회귀분석을 통해 현미의 비소 함량에 영향을 주는 인자들을 조사하였고, 통계 프로그램은 SPSS (IBM, ver, 20)를 이용하였다. 또한, 현미비소 함량 예측 모델식의 적합성 및 타당성을 판단하기 위한 지표로 normalized mean error (NME)와 normalized root mean square error (NRMSE)를 사용하였다 (De Vries et al., 2011). P는 모델식에서 도출된 예측값, O는 본 실험에서 얻은 실제값을 의미한다. NME 값이 양이면 모델식에서 도출된 예측값이 실제값보다 높아 모델식이 overestimation, 음의 값이면 underestimation한 것으로 판단 할 수 있다. NME값이 0에 가까울수록 실제값과 모델식에서 도출된 예측값이 비슷한 것이고, 적합한 모델식이 될수 있음을 의미한다. NRMSE는 실제값과 예측값 사이에 편차를 나타내는 지표로서 값이 커질수록 실제값과 예측값의 차이가 커 변동성이 크다는 것을 의미하고 그러므로 모델식의 타당성이 저하된다 (Groenenberg et al. 2010; Lim et al., 2015).
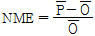 (1)
(1)
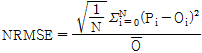 (2)
(2)
Results and Discussion
공시토양의 화학성 분석 본 연구 공시토양의 화학적 특성인자인 토양 pH, 유기물 함량 (OM), 유효인산, 점토함량 및 알루미늄 산화물의 함량을 Table 1에 나타내었다. 토양 pH는 약산성 5.4에서 염기성 8.1토양까지 비교적 고르게 분포하였고, 평균 수치는 6.2로 우리나라 농경지 논토양의 평균인 5.9 및 범위 4.1 ~ 8.4와 비슷한 수치를 보였다 (Kang et al., 2012). 유기물 함량은 9.22 ~ 88.91 g kg-1으로 분포를 보였고 평균 함량은 44.46 g kg-1 우리나라 농경지 토양의 평균 수치 26.0 g kg-1보다는 높은 경향을 보였다 (Kang et al., 2012). 이는 본 실험에서 습식 산화법이 아닌 강열감량법으로 측정하였기 때문이라고 판단된다. 유효태 인산의 평균함량 및 범위는 각각 25.26 mg kg-1및 3.87 ~ 118.1 mg kg-1으로 Kang et al. (2012)의 결과에 비하여 낮은 수치를 보였다. 또한, 점토 및 알루미늄 산화물의 함량분포는 Table 1에 나타난 바와 같이 넓은 분포를 보였다. 이들 결과는 중금속 오염 농경지의 식물 유효태 예측 모델식 개발을 위한 우리나라 폐광산 인근 논토양 사례연구 결과와 유사하였다 (Lim et al., 2014). 또한, 현미 중 비소 함량과 토양 비소 전 함량 및 비소 유효도에 영향을 미치는 토양 화학성간의 상관관계 분석을 통해 통계적 유의성을 검토 후 다중회귀분석을 실시하는 과정을 거쳐 개발되기 때문에 폭넓은 비소 농도 및 토양특성 수치를 가진 토양시료를 확보할 필요가 있는 것으로 판단된다.
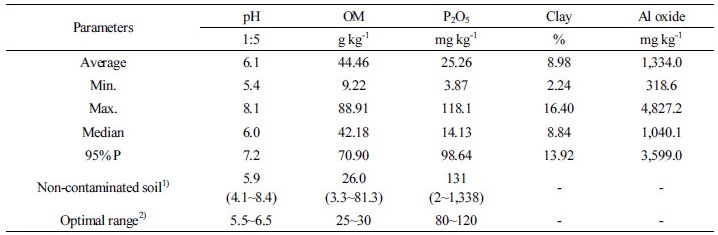
1): Physico-chemical properties in non-contaminated paddy soils in Korea surveyed in 2011 (Kang et al., 2012)
2): Optimal range of physico-chemical properties in paddy soils.
공시토양의 비소 전함량 및 유효태 함량 공시 토양 46점의 토양 중 비소 전함량 및 단일추출용매에 의한 유효태 비소의 농도는 Table 2와 같다. 조사 논토양의 비소의 평균함량 및 범위는 45.30 mg kg-1 (4.06 ~ 274.76) mg kg-1이었다. 이는 토양환경보전법에서 정하는 토양오염우려기준에 비하여 비소의 평균함량이 1.8배이며 최대함량이 11배로서 높은 수준을 확인하였고, 특히 중간값이 25.00 mg kg-1로 토양환경보전법에서 제시하는 토양오염우려기준 수준으로 1/2정도가 기준을 초과하였으며, 일부 시료는 토양오염대책기준을 초과하였다. 이는 2010년 보고된 비소오염 5개 폐광산 인근 논토양에서 조사된 비소 전함량 평균농도인 13.24 mg kg-1보다 높은 수준을 확인하였다 (Kim, et al., 2010). 또한, Kunhikrishnan 등 (2015)이 조사한 우리나라 논토양의 평균 비소 농도인 4.41 mg kg-1과 비교하여 보았을 때는 10배 이상 높은 수치를 확인하였고, Yoon 등 (2009)이 조사한 우리나라 토양의 비소 자연배경농도인 6.83 mg kg-1과 비교하여 보았을 때도 높은 수치를 확인하여, 이는 본 연구의 조사 토양이 인근 광산의 광미, 폐수 및 지구화학적 요인 등에 영향을 받은 것으로 판단된다.
단일 추출용매에 따른 토양 중 유효태 비소의 평균함량과 범위는 각각 1.0 N HCl 추출법 12.06 mg kg-1(0.05 mg kg-1 ~ 87.31 mg kg-1), 1.0 M NH4NO3 추출법 0.04 mg kg-1(0.00 mg kg-1 ~ 0.28 mg kg-1), 0.01M Ca(NO3)2 추출법 0.10 mg kg-1 (0.08 mg kg-1 ~ 0.14 mg kg-1), M3 (Mehlich 3) 추출법 2.29 mg kg-1(0.26 mg kg-1 ~ 11.57 mg kg-1)로 평균 농도는 1.0 N HCl > M3 > 1.0 M NH4NO3 > 0.01M Ca(NO3)2 순으로 1N HCl의 농도가 가장 높은 것으로 나타났다. 전 함량 대비 각 추출법에 대한 유효태 농도 함량의 평균 비율은 1.0 N HCl (26.65%) > Mehlich 3 (4.95%) > 1.0 M NH4NO3 (0.22%) > 0.01M Ca(NO3)2 (0.09%)순으로 확인되었다. 이러한 결과는 1.0 N HCl 추출 유효태 비소가 전함량에 대한 비율로서 평균 23.55% (5.39% ~ 41.92%)로 조사된 기존의 결과와 일치하였다 (Kim et al., 2010). 이 비율은 논토양의 비소 형태별 함량에서 쌀 중 비소함량과 정의 상관을 보인 비 특이적 흡착 (non-specially adsorbed), 특이적 흡착 (specially adsorbed) 및 무정형 및 비결정형 철/알루미늄 수산화물 형태 (associated with amorphous Fe and Al oxyhydroxides)의 비율과 일치하고 이는 작물로 흡수 이행되는 토양 중 비소형태로 추정된다 (Kim et al., 2010).
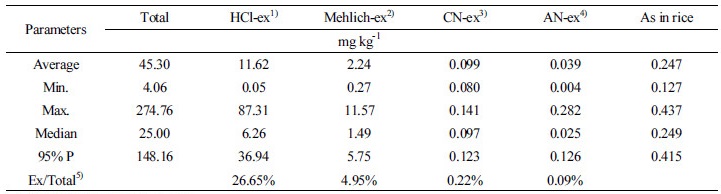
1): 1 N-HCl extractable As in soil
2): Mehlich 3 extractable As in soil
3): 0.01 M-Ca(NO3)2 extractable As in soil
4): 1 M-NH4NO3 extractable As in soil
5): Fraction of extractable As to total As.
공시현미 중 비소 함량 분석 비소오염 취약 논토양에서 생산된 현미 중 비소의 평균함량 및 범위는 각각 0.247 mg kg-1 (0.127 ~ 0.437) mg kg-1이었다 (Table 2). 이는 2009년 보고된 탑라이스 생산지역 논토양에서 생산된 현미 중 비소 평균 함량인 0.080 mg kg-1보다 높게 나타났다 (Park et al., 2009). 또한, 2015년 보고된 중금속 비오염 벼 주산단지 일반 논토양에서 재배된 현미 중 비소 모니터링 결과 (0.146 mg kg-1)과 비교하여 높게 나타났다 (Kunhikrishnan et al., 2015). 이러한 결과를 종합해 볼 때 비소오염 취약 논토양에서 생산된 쌀의 비소오염을 확인할 수 있다.
현미 중 비소 함량에 영향을 미치는 토양의 물리화학성 검토 본 연구에서 현미 비소 함량과 토양 특성의 상관성을 볼 때, 토양 pH를 제외하고 Al 산화물, 유효태 인산, 유기물 함량은 통계적으로 비슷한 수준의 유의한 양의 상관관계를 보였다 (Table 3). 특히 토양 pH는 토양 특성 및 환경인자 중에서도 중금속의 식물 유효도에 제일 크게 영향을 미치는 인자로 보고되고 있다 (Kim et al., 2007). 그러나 본 연구에서 토양 pH는 현미의 비소 함량과 낮은 유의성을 보였는데 그 이유는 카드뮴, 납, 아연과 같은 중금속과 달리 비소는 환경에 따라 흡수 기작이 다르기 때문이다. 비소는 환원상태일 때 비소 3가로 환원되어 토양 pH가 3 ~ 9의 범위일 때 토양 pH가 감소할수록 비소 용해도가 높아지고, 그와 대조적으로 산화상태일 때 비소 5가로 산화되어 용해율이 반대로 토양 pH가 감소할수록 비소 용해도도 감소하는 결과에 기인한 것으로 사료된다 (Manning and Goldberg, 1997; Smith et al., 1999; Tyler and Olsson, 2001). 우리나라 평균 논토양 pH가 5.5 ~ 6.5 사이인 것을 고려하여 토양 pH 7.0이상의 지점은 제외하고 현미 비소함량과 토양 pH의 상관관계를 분석한 결과 음의 상관관계 (R = 0.406**)로서 통계적으로 유의하였다.
현미 중 비소 함량과 토양 내 Al+Fe+Mn 산화물은 양의 상관관계를 보였다. 이것은 토양 내 Al 산화물 등과 비소와 높은 친화력을 가지고 있어서 혐기성 상태일 때 비소의 이동성을 높여 비소의 식물 흡수율을 높였다 (Fitz and Wenzel, 2002; Takahashi et al., 2004). 토양 내 유효태 인산 함량과 현미 비소 함량 간에 양의 상관관계를 갖는다. 토양 내 유효태 인산 함량이 증가함에 따라 식물이 이용할 수 있는 형태의 비소 함량이 증가하기 때문이다 (Hong et al., 2015). 토양 내 유효태 인산과 비소는 토양 교질의 흡착자리를 두고 서로 경쟁하게 되며 유효태 인산이 많이 존재하는 토양 환경에서는 비소의 용해도가 증가하게 된다 (Peryea, 1991). 토양 내 유기물 함량은 비소의 이동성에 영향을 미친다. 유기물과의 흡착으로 인해 토양 내 유기물 함량이 많으면 비소의 용해도가 줄어든다 (Lund and Fobian, 1991). 그와 반대로 유기물의 분해는 비소의 용해도를 증가시킨다. 토양 내 유기물은 유기물과 연결된 철 수산화물의 환원성 용해로 인해 토양 산화환원전위의 감소와 미생물의 활동을 증가 시켜 토양상 비소의 탈착을 높이고, 또한 유기물은 음전하를 띠는데 그것은 토양에 수착하기 위해 비소와 경쟁하기 때문이다 (Turpeinen et al., 1999; Harvey et al., 2002; Selim Reza et al., 2010). 본 연구에서는 토양 내 유기물 함량이 높아질수록 현미 비소 함량이 높아지는 양의 상관관계를 보였다.
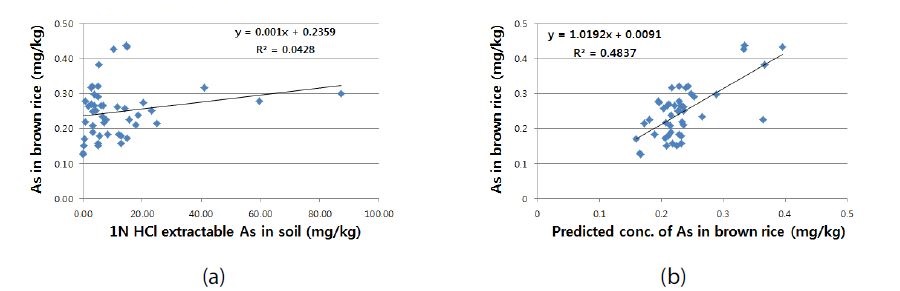
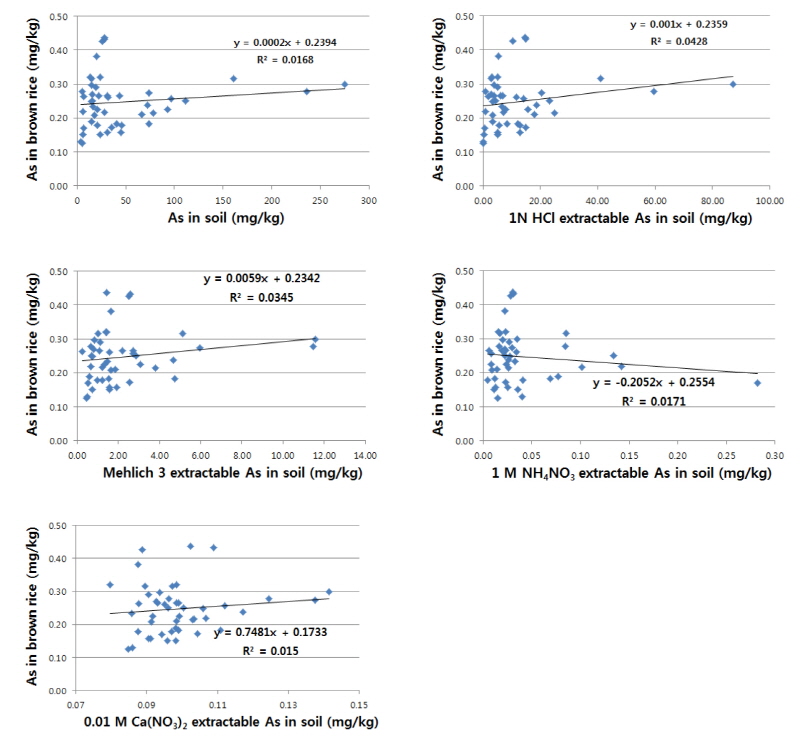
현미 중 비소 함량과 토양 중 비소 함량 간에는 통계적으로 유의성을 보이지 않았다 (Table 4 and Fig. 1). O’Neill (1990)의 보고에서도 토양 내 비소가 고농도로 존재하여도 식물체의 함량은 대체적으로 위험수준까지 도달하지 않는다고 하였다. 특히 토양 중 비소 전함량과의 상관성은 1.0 N HCl 및 Mehlich 3 추출 유효태 함량에 비해 낮았다. 이는 토양 내 이화학적 특성과 여러 가지 환경 인자에 의해 식물유효태가 달라지기 때문이고 이는 작물로의 흡수에 영향을 미치는 것으로 추정된다.
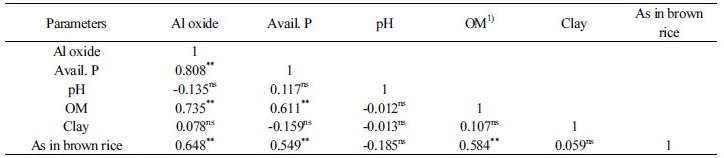
** : Significant at P = 1%
ns : Not significant
1) : Soil organic matter content in soil
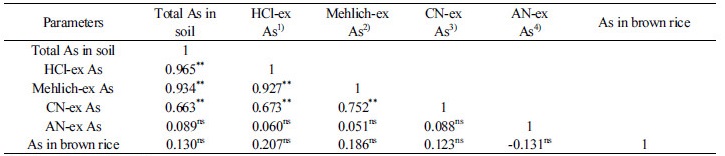
** : Significant at P = 1%
ns : Not significant
1): 1 N-HCl extractable As in soil
2): Mehlich 3 extractable As in soil
3): 0.01 M-Ca(NO3)2 extractable As in soil
4): 1 M-NH4NO3 extractable As in soil
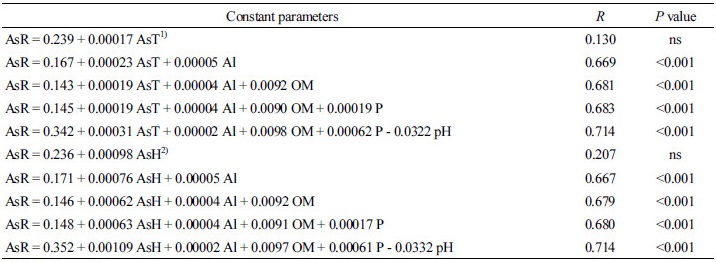
현미 중 비소 함량 예측모델식 개발 및 적합성 검증 토양 중 비소 전함량 및 1.0 N HCl 추출 유효태 비소 함량과 토양의 화학적 특성을 동시에 고려한 다중회귀분석을 실시하였고 그 결과 Table 5와 같이 회귀식으로 도출하였다. 다중회귀분석을 통해 도출된 회귀식을 보면 토양의 화학적 특성 중 Al 산화물 함량 및 토양 pH가 모델식에 추가 되었을 때 가장 큰 조정된 결정계수 증가폭을 보여 주요 변수임을 확인할 수 있었다 (Table 5). 이외 유기물 함량 및 유효태 인산 함량은 추가로 적용하여도 결정계수가 크게 증가하지 않은 것으로 나타났다.
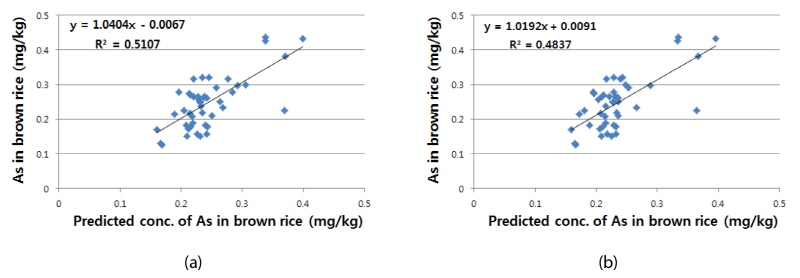
다중회귀분석을 통해 나온 모델식에서 도출된 예측값 (Predicted value) 과 본 연구에서 실제 분석을 통해 얻은 측정값 (Measured value)을 통해 NME, NRMSE를 산출하였다. 그리하여 이를 통해 본 연구에서 도출한 모델식의 Overestimation, Underestimation 여부, 모델식 적합성을 판단하였다. 토양 중 비소 전함량과 1 N HCl 추출 함량에 따른 현미 비소 함량 예측 모델식에서 NME 값은 각각 -0.0128과 -0.055로 약간 Underestimation한 것을 확인할 수 있었다. NRMSE 값은 각각 0.2108과 0.2229로 예측값과 측정값간의 변동성은 크게 차이나지 않는 것을 의미하므로 모델식의 타당성이 높다고 판단되어진다. Fig. 2는 토양 중 비소 전함량과 1 N HCl 추출 함량에 따른 현미 중 비소 함량 예측 모델식에 의해 도출된 예측값과 현미 비소 함량 측정값 간의 상관관계를 나타낸다. 예측값과 측정값 간의 상관관계에서 0.71**으로 강한 양의 상관관계를 확인하였다. 그리하여 본 연구에서 지정한 비소 오염 농경지내 현미 비소 함량을 예측하기 위해서 본 모델식을 적용할 수 있다고 판단된다.
Conclusion
본 연구에서는 비소오염 농경지에서 안전한 농산물 생산과 효율적인 토양관리방안을 모색하고자 토양 중 함량 및 화학성을 고려한 현미 중 비소 함량 예측 모델식을 개발 하였다. 국내 비소취약 오염농경지 토양 및 현미 46점을 채취하여 현미 및 토양 중 비소 함량을 분석하였다. 비소 총 농도를 조사한 결과 토양 총 비소함량은 평균 45.30 mg kg-1, 현미 중 비소 함량은 평균 0.24 mg kg-1으로 나타났고, 식물 유효태 비소 농도는 1.0 N HCl 추출법 11.62 mg kg-1, 1.0 M NH4NO3 추출법 0.039 mg kg-1, 0.01M Ca(NO3)2 추출법 0.099 mg kg-1, Mehlich 3 추출법 2.24 mg kg-1로 나타났다. 현미 비소 함량과 토양 특성과의 상관관계에서는 Al산화물, 유효태인산, 유기물과 양의 상관관계를 보였다. 토양 pH와 현미 비소 함량간의 상관관계에서는 통계적으로 낮은 유의성을 보였지만, 염기성 토양을 제외시킨 후 상관관계를 보았을 때 음의 상관관계를 나타냈다. 현미 비소 함량과 식물유효태 비소 농도와의 상관관계에는 1.0 N HCl이 가장 높은 양의 상관관계를 나타냈다. 본 결과를 토대로 향후 본 연구에서 선정한 비소 오염 농경지에서 유효도 평가시 1.0 N HCl 침출법을 활용할 수 있을 것으로 판단되며, 토양 특성을 함께 고려하여 토양 중 비소 유효태 함량을 평가하여야 할 것으로 판단된다. 이를 토대로 비소 오염 농경지에서 현미 비소 함량 예측 모델식을 개발하였다. 비소 전 함량, 토양특성을 이용하여 다중회귀분석을 실시한 결과 비소 전 함량과, 토양 pH, Al산화물, 유효태 인산, 유기물함량이 현미 비소 함량에 영향을 미치는 주요 매개변수로 확인되었고, 현미 비소 함량은 비소 전 함량 및 토양 특성에 의해서 결정된다고 판단할 수 있었다. 이는 상대적으로 높은 상관관계를 갖는 중요한 인자들만을 적용한 회귀식을 이용하여 현미 비소 함량을 예측 모델식을 구축하는 것이 적합하다고 판단된다. 토양 중 1 N HCl 유효태 비소함량을 고려한 현미 중 비소함량 예측 모델식은 다음과 같다. As in brown rice = 0.352 + 0.00109 * HCl extractable As in soil + 0.00002 * Al oxide + 0.0097 * OM + 0.00061 * avail-P – 0.0332 * soil pH (R = 0.714***). 모델식에 대한 적합성 및 타당성을 평가하기 위해 NME, NRMSE 값을 산출하였다. 현미 비소 함량 예측 모델식에서 도출한 예측값과 실제 측정치간의 차이가 크지 않았고, 예측값과 측정값간의 상관관계에서 높은 상관관계를 보였기 때문에 본 연구에서 대상으로 지정한 비소 오염 농경지에서 현미 비소 함량을 예측 모델식을 적용 할 수 있다고 판단된다.