Introduction
인류발생 증가로 인한 지구온난화와 지구온난화 가스 발생량 증가와의 관계는 반박할 여지가 없는 매우 밀접한 관계이다. 산업혁명 이후 대기 중 이산화탄소 (CO2), 메탄 (CH4), 그리고 아산화질소 (N2O)의 양은 각각 36%, 148%, 20% 증가하였으며 특히, N2O의 경우 지구 온난화 지수 (Global warming potential, GWP)가 296으로 온실효과에 매우 강력한 영향을 미치는 온실가스로 주목 받고 있다 (IPCC, 2007).
N2O의 배출원은 주로 농업활동에 의한 것으로 이는 퇴비 및 화학비료 시용, 작물 잔재물 (residue)의 시용 등을 포함한다 (Regina et al., 2013). 화학비료 및 가축분 퇴비시용은 다양한 경로로 N2O 발생에 영향을 미치게 되는데, 1) 질화과정 및 탈질화과정에서 화학비료 및 가축분 퇴비 내 다양한 N 형태 (NH4, NO3, 유기 질소)는 N2O 가스 생성에 영향을 미치며, 2) 화학비료 및 가축분 퇴비 내 쉽게 분해될 수 있는 유효 탄소는 탈질화 과정을 가속화 시키며, 산소의 소비를 빠르게 증가시키게 만든다. 또한 3) 화학비료 및 가축분 퇴비는 토양 내 pH 변화를 일으킬 뿐 아니라 토양 내 염도 및 수분상태를 변화로 인하여 토양 내 생물 물리 화학적 과정을 변화시킨다 (Velthof et al., 2003).
Flynn and Smith (2010)과 Qin et al. (2012)의 보고에 의하면 1990년부터 2005사이 세계 식량공급량은 증가 하였지만 이에 따라 화학비료 및 퇴비의 사용량도 증가함으로써 대기 중 N2O의 양이 17% 증가하였다고 한다. 또한 퇴비의 시용은 토양의 비옥도 증가, 토양 내 미생물량의 증가 및 양분동원력을 높여줌으로 효소활성을 높여주는 중요한 역할을 하지만 가축분 퇴비 제조 시 많은 양의 지구 온난화 가스 (CO2, N2O)를 배출 할 뿐 아니라 질화 및 탈질화의 과정을 가속화함으로 N2O 배출량을 증가시킨다. 더욱이, 화학비료를 시용하였을 때 보다 장기간 더 많은 N2O를 배출한다는 연구가 보고되었다 (Rochette et al., 2008).
IPCC의 methodology에 의하면 농경지 토양에 시비되는 총 질소함량이 N2O 발생에 영향을 미치는 주요 요인이라 판단된다고 한다 (Mosier et al., 1998).
따라서 본 연구는 밭 작물 재배기간 동안 퇴비의 시용에 의해 발생되는 N2O 발생 특성을 조사하여 퇴비의 투입이 N2O의 발생량에 미치는 기여도를 파악하고자 실시되었다.
Materials and Methods
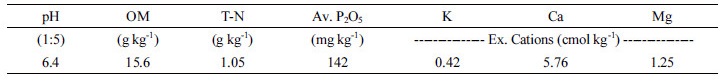
공시토양 및 퇴비의 특성 본 연구를 수행하기 위해 경남 밀양시 부북면 오례리에 소재하는 부산대학교 부속농장 밭토양 (35°30'07.6"N 128°43'16.0"E)을 공시토양으로 선정하였다. 대상지역의 토양은 용지통에 속하는 토양이었으며 pH는 6.4이었으며 총 질소 함량은 1.05 g kg-1이였다. 자세한 공시토양 및 퇴비의 화학적 특성은 Table 1, 2에 나타냈다.
시험포장 및 재배관리 각 처리구의 크기는 2.5 × 4 m (10 m2)로 난괴법 (Randomized complete block design), 4 반복하였으며, 경운 로터리실시와 함께 두둑을 설치하였다.
시험에 사용된 재배 작물은 베니하루까 고구마 (Ipomoea batatas)로 재식거리는 이랑 폭 75 cm × 포기사이 20 cm였으며, 2016년 6월 4일에 모종을 삽식 하였고, 2016년 9월 29일에 수확하였다. 토양수분 관리는 자연 강우량으로 하였다.
퇴비 및 화학비료 시용 퇴비는 우분을 사용하였으며, 퇴비 및 화학비료 시비량은 고구마 표준시비법 (RDA, 2010)에 준하여 우분은 10 Mg ha-1를 화학비료는 요소 (N), 용성인비 (P2O5), 황산칼리 (K2O)를 55-63-156 kg ha-1으로 시비하였다. 우분은 고구마 정식 2주전에 시용하였으며, 화학비료는 고구마 정식 후 7일 후에 시비하였다.
챔버 설치 및 N2O 가스 채취방법 static 챔버 방법을 사용 (Conen and Smith, 1998)하였으며, 챔버 면적은 0.05 m2로 각 처리구 중앙 두둑위에 0.05 m깊이로 조심스럽게 설치하였다. 시험 전 밭 토양의 N2O 베이스라인을 잡기 위해 퇴비 처리 전 각 반복구간을 대표 할 수 있는 곳에 챔버 설치 후 가스를 채취하였다. 챔버는 각 처리구 두둑 정 중앙에 1개의 챔버를 설치하였으며 1주 간격으로 N2O 배출량을 측정하였다. 재배기간 동안에는 챔버 안에 식물체가 자라지 않게 하였다.
챔버 설치 후 2주 안정기를 가진 후 매주 1회 간격으로 N2O 배출량을 측정하였으며, 이벤트 (퇴비 처리, 화학비료 처리, 집중강우) 후에는 주 2회씩 시료를 채취하였다. 가스 시료 채취 (Consentino et al., 2013)는 오전 9:00부터 오후 12:00 사이에 하였으며, 가스 채취 시간은 0, 40분으로 하였으며 (Chadwick et al., 2014) 가스 채취 시작 전, 후에 대기 중 가스도 채취하였다. 가스 시료 채취 시 각 처리구의 챔버 내 온도 및 portable 토양 수분센서를 이용하여 토양 수분을 측정하였다. 대기 중 N2O의 농도는 가스크로마토그래피 (Simatzu Optimum 800, Japan)을 이용하여 측정하였다.
N2O 배출량 계산 및 water-filled pore space (WFPS)
F = ρ× (V/A) × (Δc /Δt) × (273/T) (Eq. 1)
F는 N2O 배출량, ρ는 가스밀도 (mg cm-1), V는 챔버 내 공기체적 (m3), A는 챔버 바닥면적 (m2), Δc/Δt 챔버 내 가스농도의 평균 증가속도 (mg m-1 hr-1), T 는 챔버 내 평균기온 (K).
WFPS % = (부피수분 함량% / 공극률%] × 100
공극률 % = [1- (bulk density / 2.65)] × 100
토양의 화학적 특성 분석 공시토양의 이화학적 분석방법은 다음과 같은 방법으로 수행하였다. pH (1:5 토양:물), 유기물 함량 (Walkley and Black method; Allison, 1965), 총질소 함량 (Kjeldahl method; Bremner, 1965), 치환성 양이온 K+, Ca2+, Mg2+ (1 N NH4-acetate pH 7.0, AAS, atomic absorption spectroscopy, Perkin elmer model 3300, Norwalk, CT, USA). 유효인산의 함량은 Lancaster법 (RDA, 2000)을 이용하여 분석하였다.
토양 내 무기태 질소 분석 방법은 다음과 같이 수행하였다: 토양 건조시료 5 g에 25 mL의 2 M KCl을 넣고 30분 동안 진탕한 후 Whatman No. 2로 여과하여 침출액을 각각의 실험에 이용하였다.
암모늄태 질소 (NH4-N)는 Indophenol-Blue 비색법 (Searle, 1984)으로 측정하였다. 침출액 2 mL에 EDTA 용액을 0.5 mL, Salicylate 용액을 2 mL, Hypochlorite 용액 1 mL, 증류수 7 mL을 넣고 혼합한 후 37°C에 30분간 중탕시킨 후 UV/VIS Spectrophotometer (Optizen 3220UV, Mecasy Co. Ldt, Korea)를 이용하여 667 nm의 파장에서 측정하였다. 질산태 질소 (NO3-N)는 brucine 법 (Wolf, 1944)으로 측정하였다. 침출액 5 mL에 30% NaCl 1 mL와 5 mL H2SO4 (4:1 H2SO4:H2O)을 넣고 혼합한 후 10분간 수냉한다. 다음으로 brucinesulfanilic acid 0.25 mL를 넣고 혼합한 후 90°C에 20분간 중탕시킨 후 수냉한다. 충분히 식힌 다음 UV/VIS Spectrophotometer를 이용하여 410 nm의 파장에서 측정하였다.
통계분석 통계분석은 SAS 통계프로그램 (버전 9.2)을 이용하여 실시하였다 (SAS institute, 2006). 처리간의 차이를 비교하기 위하여 조사된 자료는 ANOVA 검증을 통하여 분석하였다. F-test 결과 값이 P < 0.05의 범위에서 유의한 경우에만 최소유의차 검정 (LSD)을 실시하였다.
Results and Discussion
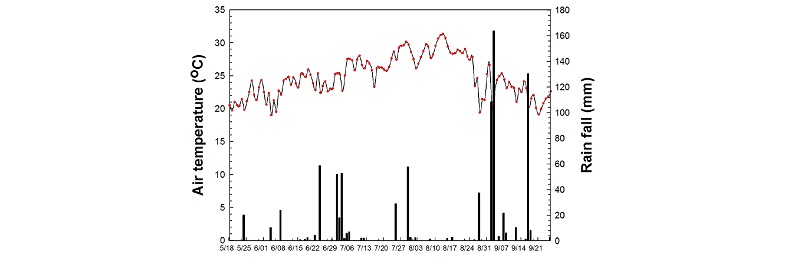
기상환경 및 토양수분함량 작물 재배 중 대기온도 및 강우량은 Fig. 1과 같다. 재배 중 월별 평균 대기온도는 19.6~27.5°C였으며, 재배 기간 중 누적 강우량은 855.8 mm이였으나, 9월 누적강우량이 454 mm로 9월에 강우량이 집중되었다. 또한 처음 퇴비 처리 4주 후 누적강우량은 56.4 mm였다.
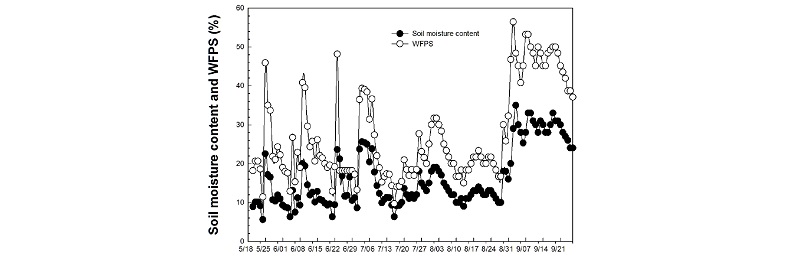
작물 재배 중 토양 내 수부함량 (Fig. 2)은 5.6~33%로 평균 16%였으며, WFPS의 범위가 9.6~53.2%로 평균 23%였다.
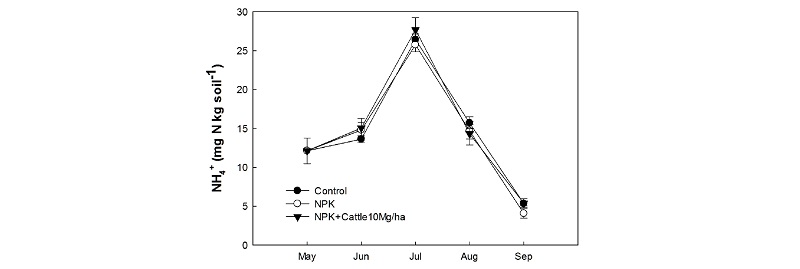
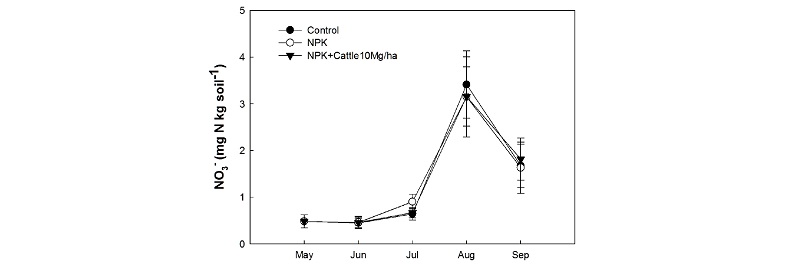
토양 내 질산태 질소 및 암모니아태 변화 시험 전 공시토양의 토양 내 NH4+-N 및 NO3--N는 10 및 0.4 mg kg-1였다. NH4+-N의 경우 퇴비 및 화학비료 처리 후 25.7~27.7 mg kg-1까지 유의하게 증가 (p < 0.01) 하다가 7월 이후 감소하였으며 (Fig. 3), NO3--N 의 경우 퇴비 및 화학비료 처리 후 3.2~3.4 mg kg-1까지 유의하게 증가 (p < 0.01)하다가 8월 이후 감소하였다 (Fig. 4). NH4+-N 및 NO3--N 모두 처리간 유의차는 나타나지 않았다.
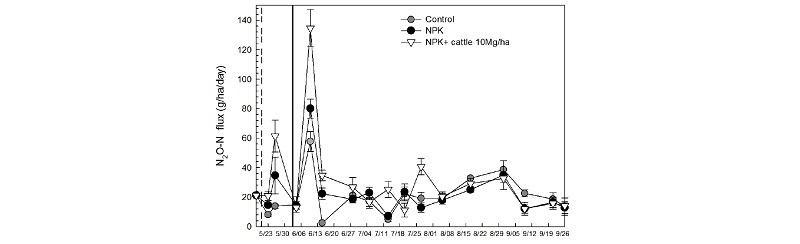
N2O 일일 배출량 화학비료 및 퇴비 처리는 토양 내 미네랄 질소의 함량을 증가시켜 높은 량의 N2O를 배출하게 한다. 작물 재배기간 중 N2O 일일 배출량은 2주에서 5주 사이에 가장 놓았다가 점차적으로 감소하는 경향이었다. 각 처리구의 일일 N2O 배출량의 범위는 무처리구 2.4~57.7 g ha-1, NPK 7.1~80.1 g ha-1, NPK + 우분10 Mg ha-1 11.1~134.6 g ha-1였으며, 일일 평균 N2O 배출량은 각각 20.4, 23.0, 34.1 g ha-1 day-1로 NPK + 우분10 Mg ha-1처리구 > NPK 처리구 > 무처리구 순으로 높았다 (Fig. 5).따라서 본 연구결과 화학비료 및 퇴비의 처리는 N2O의 발생량에 가장 큰 영향을 미침을 확인하였다. 이전 연구결과에 따르면 화학비료 처리 후 7일에서 42일 후에 대부분의 N2O가 배출된다고 한다 (Chadwick et al., 2000; Chantigny et al., 2010; Rochette et al., 2008). 본 연구결과 역시 퇴비처리 및 화학비료 처리 후 각각 6일, 10일 후에 N2O 발생량이 높음을 확인하였다.
일반적으로 토양수분은 N2O 배출량에 있어 중요 요소로 고려되며 특히 > 60 WFPS 일 때 가장 큰 영향을 미친다고 보고되어 왔다 (Baral et al., 2016; Bateman and Baggs, 2005; Davidson, 1993; Dobbie et al., 1999; Line and Doran, 1984; Metay et al., 2007; Ruser et al., 2006). 본 연구결과 역시 비료 및 퇴비 처리 후 5월 24일, 6월 4일, 6월 8일에 20.1 mm, 10.1 mm, 23.9 mm의 강우량 (Fig. 1)은 토양 수분 (20~22%) 및 WFPS (40~45%)의 증가에 영향을 미쳤으며 (Fig. 2), 이에 따라 비료 및 퇴비처리와 이후의 토양수분 및 WFPS 증가가 더해져 많은 양의 N2O 배출에 큰 영향을 미쳤을 것이라 판단된다. 하지만 최근 연구결과 (Bara et al., 2017)에 의하면 높은 강우량은 토양 내 산소 공급 차단으로 인해 N2O 발생에 영향을 미칠 수 있지만, 퇴비 처리가 토양 수분함량 보다 N2O 발생량에 더 직접적으로 영향을 미친다고 한다. 따라서 본 연구결과에서 보여지는 것처럼 퇴비 및 화학비료 처리 10일 후의 강우량은 N2O 배출 발생량에 큰 영향을 미치지 못한 것으로 보여진다 (Bara et al., 2017).
또한 앞서 언급한 것과 같이, 토양 내 NO3--N의 농도는 N2O 배출량에 큰 영향을 미친다고 알려져 있다 (Alvarez et al., 2012; Baral et al., 2017; Cosentino et al., 2013). 본 연구 결과 8월에 N2O 배출량이 증가되다가 9월 이후 다시 감소됨을 됨을 확인하였는데, 이는 8월에 NO3--N의 농도가 최고로 높아졌다가 다시 9월에 감소하는 경향과 일치하였다 (Fig. 4).
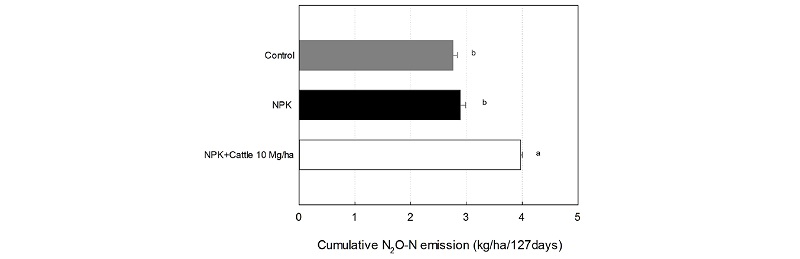
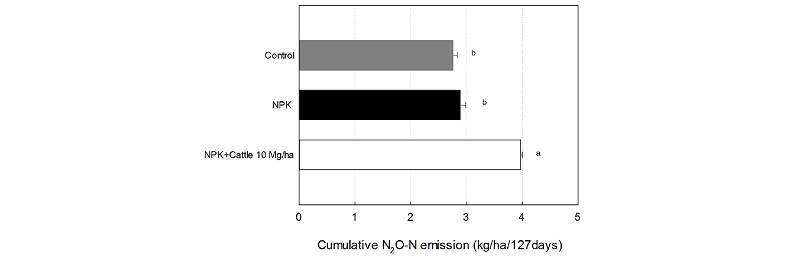
N2O 배출 누적량 재배기간 중 NPK + 우분10 Mg ha-1, 화학비료, 무처리구의 N2O 배출 누적량은 각각 3.9, 2.8, 2.7 kg ha-1 127 day-1로 NPK + 우분10 Mg ha-1 처리구가 다른 처리구와 비교하였을 때 유의차를 나타내었다 (Fig. 6). 하지만 화학비료 처리구와 무처리구에서의 N2O 누적량은 유의한 차이를 보이지 않았다 (Fig. 6).