Introduction
Materials and Methods
배양실험 및 시료채취
분석 및 계산
통계 분석
Results and Discussion
질산화 및 토양 무기태질소 농도 변화
토양에서 N2O 배출
Conclusions
Introduction
농경지 토양에서 질소 비료 투입은 작물 생육과 수확량을 증진시키는 핵심적인 농업 관리 수단이다. 그러나 질소 비료의 과도한 사용은 토양 질소 순환 과정을 교란시켜 강력한 온실가스이자 오존층 파괴 물질인 아산화질소 (N2O) 배출을 증가시킬 수 있다 (Smith et al., 1997; Wang et al., 2011). 전 세계 N2O 배출에서 농업 활동이 차지하는 비중은 70% 이상이며, 질소질 비료의 사용 증가가 주요 원인으로 지목되고 있다 (IPCC, 2022). 산업혁명 이전 약 270 ppbv 수준이었던 N2O 농도는 지속적으로 상승하여 2025년에는 338.7 ppbv에 도달하였으며 (NOAA Global Monitoring Laboratory, 2025), 농도 자체는 이산화탄소 (CO2)에 비해 낮지만 100년 기준 지구온난화지수 (GWP100, global warming potential)는 CO2의 273배에 해당하여 지구온난화에 대한 영향이 큰 것으로 평가된다 (IPCC, 2022).
토양에서 N2O는 미생물이 관여하는 여러 질소 변환 과정에서 생성되어 대기 중으로 배출된다. 질산화 (nitrification), 탈질 (denitrification), 혐기성 암모늄 (NH4+) 산화 (anammox, anaerobic ammonium oxidation), 질산화균 탈질 (nitrifier denitrification) 등의 여러 경로를 통해 N2O가 생성될 수 있으며, 이 중 질산화와 탈질 과정이 N2O 배출의 주된 생성 경로로 알려져 있다 (Bremner, 1997; Wrage et al., 2001; Toma et al., 2011; Wei et al., 2017; Nie et al., 2019). 질산화는 주로 밭과 같은 호기성 토양에서 유기태 질소의 무기화 (mineralization)로 생성된 NH4+이 산화되는 과정으로, NH4+가 주요 기질로 이용된다 (Schmidt, 1982; Hart et al., 1994; Sahrawat, 2008). 반면, 탈질은 논과 같은 혐기성 토양에서 질산 (NO3-)이 환원되는 과정으로 NO3-가 주요 기질로 이용된다 (Hasebe et al., 1987; Pandey et al., 2018; Schlüter et al., 2025). 이러한 두 가지 질소 전환 반응 과정에서 N2O는 중간 생성물로 생성되어 토양으로부터 대기 중으로 배출된다 (Robertson and Tiedje, 1987; Maag and Vinther, 1996; Bateman and Baggs, 2005).
질소 변환 과정에서의 N2O 배출은 온도와 수분 조건 등 다양한 토양 환경 요인의 영향을 받는 것으로 알려져 있다 (Regaert et al., 2015; Wang et al., 2021). 온도 조건을 달리하여 배양실험을 수행한 선행연구에서는 온도 상승에 따른 N2O 배출 증가는 NH4+ 산화 속도 증가에 기인하기보다는 유기질소 무기화가 촉진되면서 추가적으로 공급되는 질소 기질의 양에 크게 의존하는 것으로 보고하였다 (Lim et al., 2024). 토양 수분 조건은 질소 전환 경로를 변화시키며, 수분 함량 증가에 따라 산소 확산이 제한되고 탈질 과정이 촉진되어 N2O 배출이 증가하는 것으로 보고되었다 (Liu et al., 2022; Button et al., 2022).
토양 내 NH4+와 NO3-는 N2O 생성량을 결정하는 핵심 요인이므로, 비료 시비와 같은 질소 공급에 따라 N2O 배출량이 크게 달라질 수 있다 (Butterbach-Bahl et al., 2013; Smith, 2017). 농경지에서 질소 비료 사용은 가용성 질소의 농도를 증가시켜 N2O 배출을 선형 또는 지수적으로 증가시키는 것으로 보고되고 있다 (Signor and Cerri, 2013; Shcherbak et al., 2014; Cai et al., 2016). 기존 연구들은 주로 질소 처리량 또는 토양 내 가용성 질소 농도 증가에 따른 N2O 배출을 보고하였으나, 실험 기간 동안의 N2O 누적배출량까지 분석한 연구는 제한적이며, 토양 내 질소 전환 반응과 N2O 배출 간의 관계에 대한 정량적 해석이 부족하다. 질소 비료 사용은 토양 pH 및 질소 전환 반응에 관여하는 토양 화학성을 변화시켜 N2O 생성 양상에 영향을 미칠 수 있다 (Mørkved et al., 2007; Farquharson, 2016; Li et al., 2020). 특히, 과도한 질소 비료 처리에 따른 토양 산성화는 질산화 반응을 억제할 수 있으며, 이는 N2O 배출이 질소 처리량에 비례하지 않을 수 있음을 시사한다.
이에 본 연구에서는 호기성 토양에서 N2O 누적 배출량이 질소 처리량 자체보다는 질산화 반응의 누적 진행 정도에 의해 지배될 것이며, 고농도 질소 처리에 따른 토양 산성화가 질산화 반응을 억제함으로써 N2O 생성을 조절할 것이라는 가설을 설정하였다. 이를 검증하기 위해, 호기 조건에서 암모늄염을 서로 다른 수준 (0 - 300 mg N kg-1)으로 처리한 토양을 밀폐조건에서 배양실험을 수행하여 N2O 누적 배출량, 토양 pH 변화, 질산화 반응을 분석하였다. 토양에서의 N2O 배출량은 일반적으로 정적 챔버법 (static chamber method)을 이용하여 산정되어 왔으나 (Jeong et al., 2016; Lee et al., 2021; An et al., 2024), 질소가 시비된 토양에서는 질소 전환 반응이 단기간에 빠르게 진행될 수 있기에, 본 연구에서는 배양기간 동안 밀폐 조건을 유지하여 N2O 누적 배출량을 산정하였다 (Lim et al., 2024).
Materials and Methods
배양실험 및 시료채취
시험 토양은 전북특별자치도 익산시 원광대학교 시험포장 (35°58′6.6″N, 126°57′41.4″E)에 위치한 밭 (송정통, Songjeong series)에서 채취하였고, 풍건 후 2 mm 체로 거른 뒤 실험에 사용하였다. 토양의 물리화학적 특성은 Table 1에 제시하였다.
Table 1.
Physicochemical properties of soil used for the experiment.
처리구는 일반적인 농경지의 질소 시비 수준을 고려하여 0 (무처리구), 50, 100, 200, 300 mg N kg-1으로 설정하였으며, 각 처리구는 각각 N0, N50, N100, N200, N300으로 표기하였다. 질소 처리량이 높을수록 질산화 과정이 장기간 지속될 것을 고려하여 처리구별로 토양 채취 횟수를 다르게 설정하였다 (N0, N50, N100, N200, N300 각각 1, 3, 4, 5, 5회). 배양 동안에 주기적인 가스채취와 배양 마지막 토양채취를 위해 4개 반복을 두고, 나머지 반복은 배양 동안에 주기별로 토양 채취를 위해 3개 반복을 두었다.
100 mL 폴리에틸렌 병 59개 (N0, N50, N100, N200, N300 각각 4, 10, 13, 16, 16개)에 토양을 25 g씩 담고, 토양 수분함량을 포장용수량 (field capacity, FC)보다 낮은 14.5% (w/w)로 맞춘 후 25°C의 암조건 항온 배양기에서 10일 동안 예비 배양하였다. 예비 배양 후 각 처리구에 해당하는 질소 농도가 되도록 황산암모늄 [(NH4)2SO4] 용액을 제조하여 토양에 1 mL씩 처리하였다. 이후 토양을 섞고 토양 전용적밀도가 1.2 g cm-3가 되도록 하였으며, 증류수를 이용하여 토양 수분함량을 포장용수량인 18.5% (w/w)로 맞추었다. 이 토양을 1 L 유리 배양용기에 넣어 뚜껑을 닫고 25°C에서 배양하였다.
각 처리구의 배양용기에 담긴 반복 시료 중에서 4개는 배양 동안에 주기적인 가스채취와 배양 마지막 토양채취에 이용하였고, 나머지 반복은 배양 동안에 주기별로 3개씩 토양 채취에 이용하였다. 가스채취는 개폐가 가능한 튜브가 연결된 배양용기 뚜껑을 이용하여 주 2 - 3회 진행하였고, 가스 채취 후에는 증류수를 이용하여 토양 수분함량을 포장용수량으로 맞추고 배양용기를 환기하여 호기적 조건을 유지하였다. 그리고 토양이 들어있지 않은 배양용기에 대해서도 같은 방법으로 배양하고 공기를 채취하였다.
분석 및 계산
시험 토양은 풍건 후 2 mm 체로 걸러 토양의 물리·화학적 특성을 분석하였다. pH는 토양과 증류수를 1:5 (w/v) 비율로 혼합하여 진탕한 후 pH meter (SevenCompact S220, Mettler Toledo, Switzerland)를 이용하여 측정하였다. 총 탄소와 총 질소 함량은 원소분석기 (Flash 2000 series, Thermo, USA)를 사용하여 분석하였다. 무기태질소 (NH4+-N 및 NO3--N)는 토양 시료를 2 M KCl로 침출하여 여과한 후 증류법으로 분석하였다 (Keeney and Nelson, 1982). 토양의 포장용수량은 압력판 추출장치 (Pressure plate extractor, Soilmoisture Equipment Corp., USA)를 이용하여 33 kPa 장력 조건에서 측정하였고, 토성은 유기물을 과산화수소로 분해한 후 sodium hexametaphosphate를 첨가하여 분산시킨 뒤 피펫법으로 분석하였다 (Gee and Bauder, 1986).
배양기간 동안의 토양 무기태질소 농도 변화를 구하기 위해, 각 처리구별로 토양 시료를 주기적으로 채취하였다. N0은 배양 후 51일, N50은 3, 10, 51일, N100은 3, 10, 12, 51일, N200은 3, 10, 14, 17, 51일, N300은 3, 10, 17, 28, 51일에 채취하였으며, 토양 pH도 함께 분석하였다.
CO2 및 N2O의 농도는 기체크로마토그래피 (7890A, Agilent, USA)로 분석하였고, 검출기로 각각 FID-methanizer와 μECD를 이용하였다. CO2와 N2O의 플럭스 (flux) 및 누적 배출량은 다음 식을 이용하여 계산하였다.
여기서, ρ는 CO2와 N2O의 기체밀도를 의미하며, 각각 1.977와 1.967 kg m-3 이다. V는 배양용기 부피 (m3), m은 배양용기 내 토양 무게 (kg), ∆c는 배양용기 내 1일당 CO2 증가 농도 (μmol mol-1) 또는 N2O 증가 농도 (nmol mol-1)를 의미하고, ∆t는 가스 채취 간의 시간 간격 (day), T는 배양온도 (K)이다. R은 CO2 플럭스 (mg CO2 kg-1day-1) 또는 N2O 플럭스 (μg N2O kg-1day-1)이며, D는 해당 플럭스가 적용된 기간(day)이다.
토양 내 유기질소의 순 무기화 (net mineralization) 양은 무기태질소 농도 변화로 계산하였다. 질소 무처리구인 N0은 배양 종료 시 채취한 토양의 전체 무기태질소 (NH4+-N + NO3--N) 농도에서 초기 토양의 농도를 차감하여 계산하였다. N0을 제외한 나머지 처리구에서 배양기간 동안 전체 무기태질소 농도의 변화에 대한 선형 회귀식의 기울기를 구하고, 해당 기울기와 마지막 배양 일수를 곱하여 순 무기화 양을 계산하였다. 기울기를 이용해 산출한 순 무기화 양의 표준편차는 회귀식 기울기의 표준편차에 마지막 배양 일수를 곱하여 추정하였다.
통계 분석
토양 pH와 무기태질소 농도 및 가스 배출량에 대한 통계분석은 R 프로그램 (version 4.3.3, Vienna, Austria)을 이용하였다. 처리 효과는 분산분석 (ANOVA)을 통해 검정하였고, 유의한 차이가 나타난 경우 α = 0.05 유의수준에서 던컨의 다중범위검정 (Duncan’s multiple range test, DMRT)을 이용하여 처리간 차이를 비교하였다. 토양 pH에 대한 질소 처리량의 영향과 가스 배출량에 대한 질소 처리량, 질산화, 토양 pH의 영향은 선형 회귀분석을 통해 평가하였으며, 회귀모형의 유의성은 P < 0.05, P < 0.01 또는 P < 0.001 수준에서 판단하였다.
Results and Discussion
질산화 및 토양 무기태질소 농도 변화
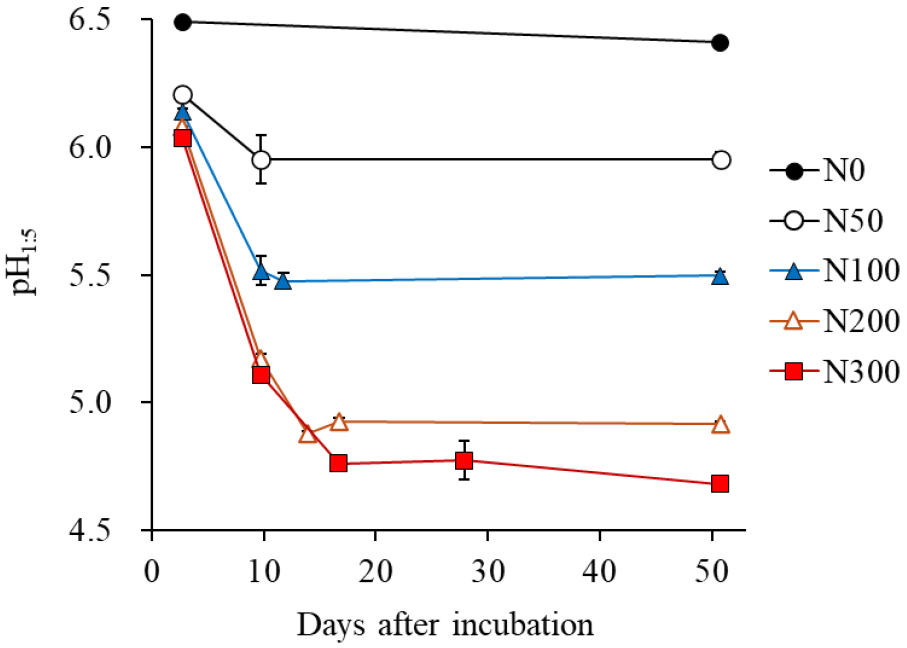
토양 pH는 질소 처리량이 높아짐에 따라 뚜렷하게 감소하였다 (Fig. 1). 무처리구 (N0)는 배양기간 동안 pH 변화가 거의 없었고, 암모늄 질소를 처리한 N50, N100, N200, N300 처리구는 pH가 감소하였다. 배양 초기 pH는 6.0 - 6.2였고, 배양 마지막 날 N50 - N300 각 처리구의 pH는 6.0, 5.5, 4.9, 4.7로 처리량이 증가할수록 더욱 낮아졌다. 토양에서 NH4+이 NO3-로 산화되는 과정에서 수소이온 (H+)이 생성되고 (Robertson, 1989; Ward, 2013), 질소 처리량이 높을수록 더 많은 H+가 방출된다. 이를 반영하여 pH 변화에 대한 질소 처리량의 설명력은 r2 = 0.94 (P < 0.01)로 유의한 선형관계가 나타났고, 질소 처리량이 100 mg N kg-1 증가할 때 토양 pH는 0.58 감소하는 것으로 나타났다. N300 처리구는 배양 마지막 날에 NH4+이 49.2 mg N kg-1 농도로 상대적으로 높았으며 (Fig. 2a), 남은 NH4+이 추가로 산화될 경우 토양 pH는 더 낮아질 것으로 예상된다.
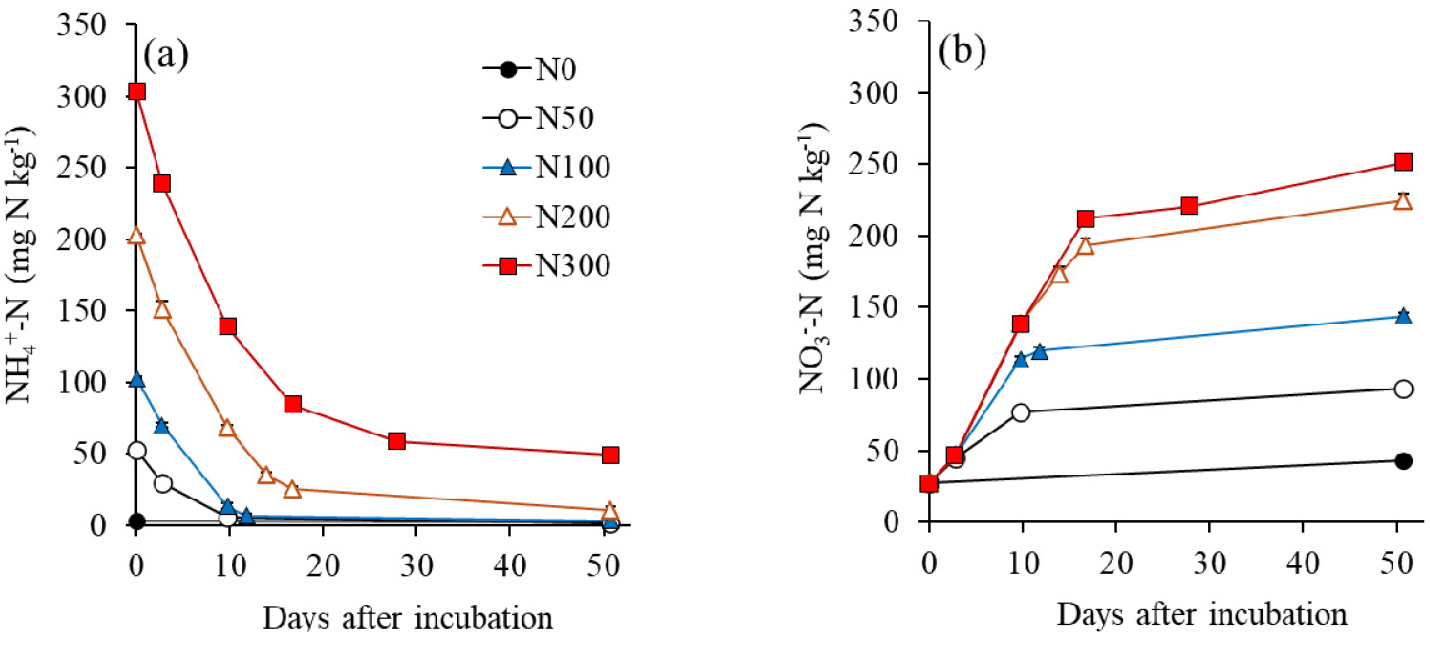
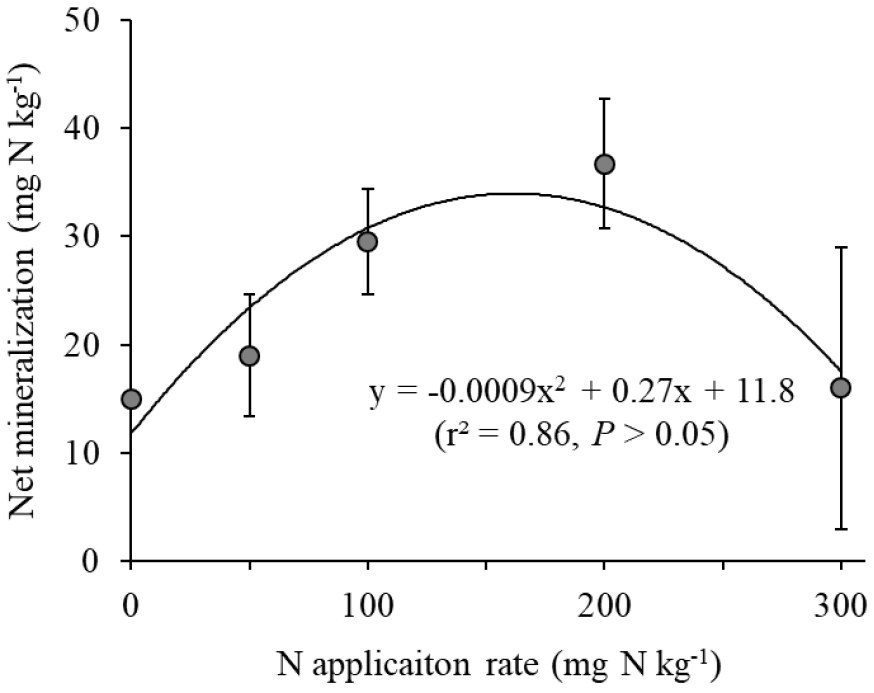
배양기간 동안 토양 NH4+-N 농도가 감소하면서 NO3--N 농도가 증가하였고, 이때 NH4+-N 농도의 감소보다 NO3--N 농도의 증가가 더 컸다. 먼저 질소 무처리구의 경우, 토양 NH4+-N 농도는 변화가 없었으나 NO3--N 농도가 증가하였다 (Fig. 2). 이는 토양 유기질소의 무기화로 인해 NH4+가 공급되고, 이어 산화되어 NO3-로 변환된 결과이다 (Signor and Cerri, 2013; Lim et al., 2024). 여기서, 무처리구의 무기태질소 농도 증가로 구한 순 무기화 양은 15.0 mg N kg-1이다. 질소 처리구의 경우 토양 NH4+-N 농도는 천천히 감소하면서 NO3--N가 증가하였다. 배양기간 동안 N50, N100, N200, N300 처리구의 순 무기화 양은 각각 19.0, 29.5, 36.7, 16.0 mg N kg-1이었다 (Fig. 3). 전체 처리구를 종합해 보았을 때, N0에서 N200으로 질소 처리량이 증가할수록 순 무기화 양이 증가하는 경향을 보였으나, N300 처리구의 순 무기화 양은 질소 무처리구와 비슷한 수준으로 떨어졌다.
질소 무기화 및 질산화 관여 미생물의 활성은 pH 5.5 미만인 산성 토양에서 저해된다고 알려져 있다 (Curtin et al., 1998; de Boer and Kowalchuk, 2001; Breugem et al., 2024). 본 연구에서 N200과 N300 처리구는 배양 마지막 일에 pH가 각각 4.9와 4.7으로 5.5보다 크게 낮아져 미생물 활성이 저하되었을 것으로 예상되며, N300에서는 무기화 양이 감소한 결과가 이를 반영하고 있다. 또한 고농도 처리구인 N200, N300에서 질산화 반응 속도가 느려지는 결과도 나타났다 (Fig. 2a). N200 처리구는 배양 마지막 날 남은 NH4+ 농도가 10.8 mg N kg-1으로 저농도 처리구 (N0, N50, N100)에 비해 높았다 (P < 0.05). N300에서 질산화 과정 저해 현상이 더욱 뚜렷하게 나타났는데, 배양 후 28일과 51일의 NH4+-N 농도가 각각 59.0과 49.2 mg N kg-1으로 변화가 작았으며, 처리한 NH4+의 상당량이 배양 마지막 날까지 소모되지 않고 남아 있었다.
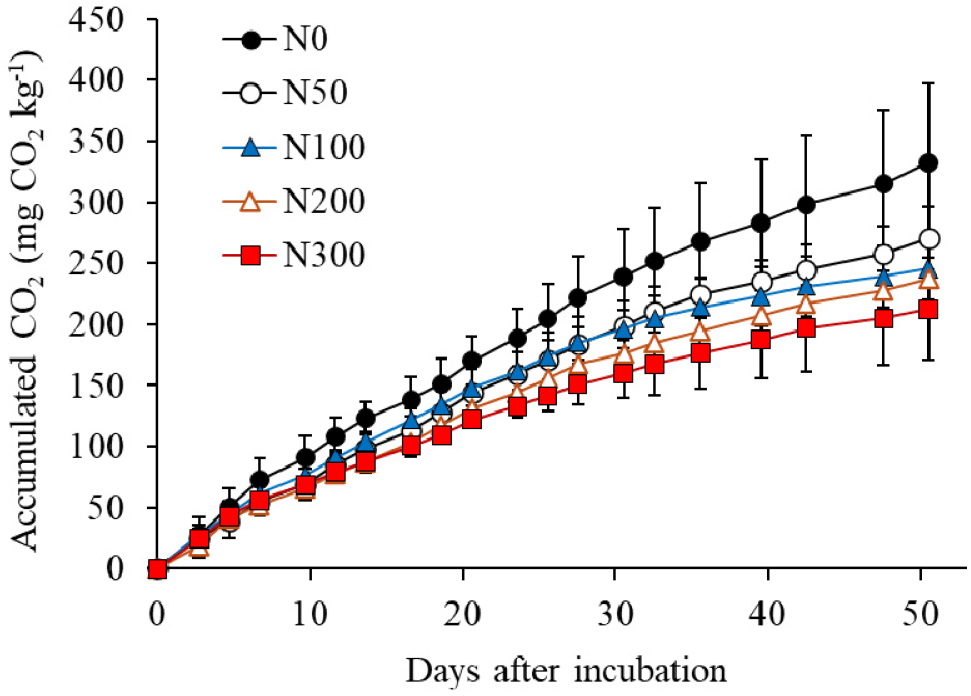
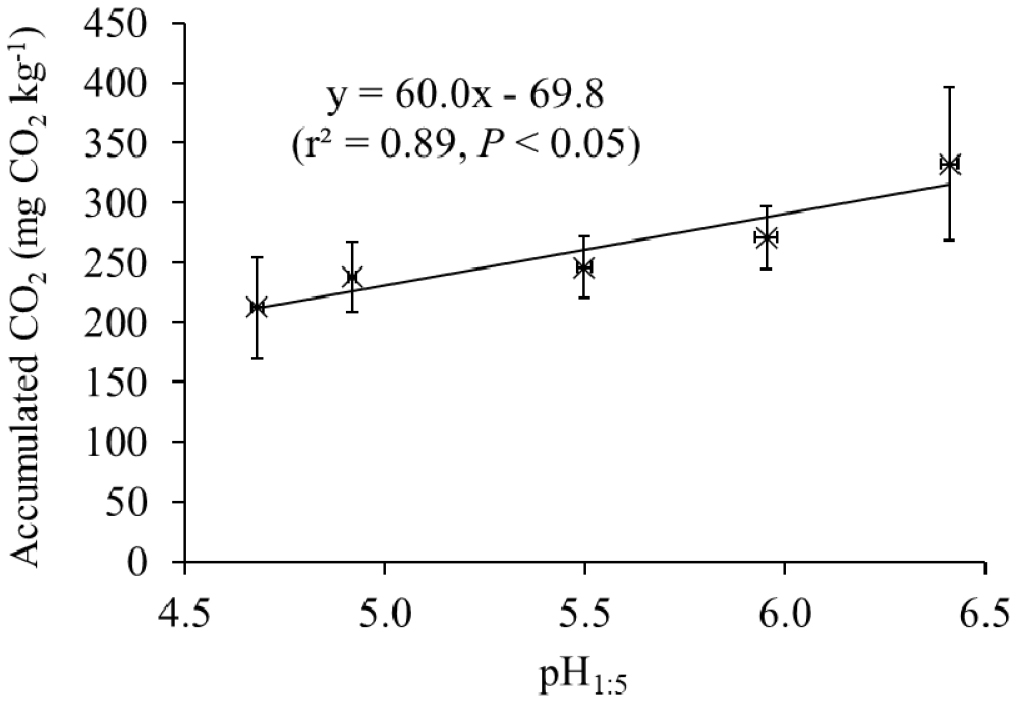
질소 처리량 증가에 따른 미생물 활성 감소는 CO2 배출량을 통해서도 확인할 수 있었다 (Fig. 4). CO2 누적 배출량은 질소 무처리구에서 332.4 mg CO2 kg-1이었고, N50, N100, N200, N300의 각 처리구에서 각각 270.9, 245.9, 237.8, 212.5 mg N kg-1로 질소 처리량이 증가할수록 감소하였다. 토양 pH가 감소함에 따라 CO2 배출량이 감소하였고 (r2 = 0.88, P < 0.05, n = 5; Fig. 5), 이는 pH 감소에 따라 미생물 활성이 억제된 결과임을 보여준다.
토양에서 N2O 배출
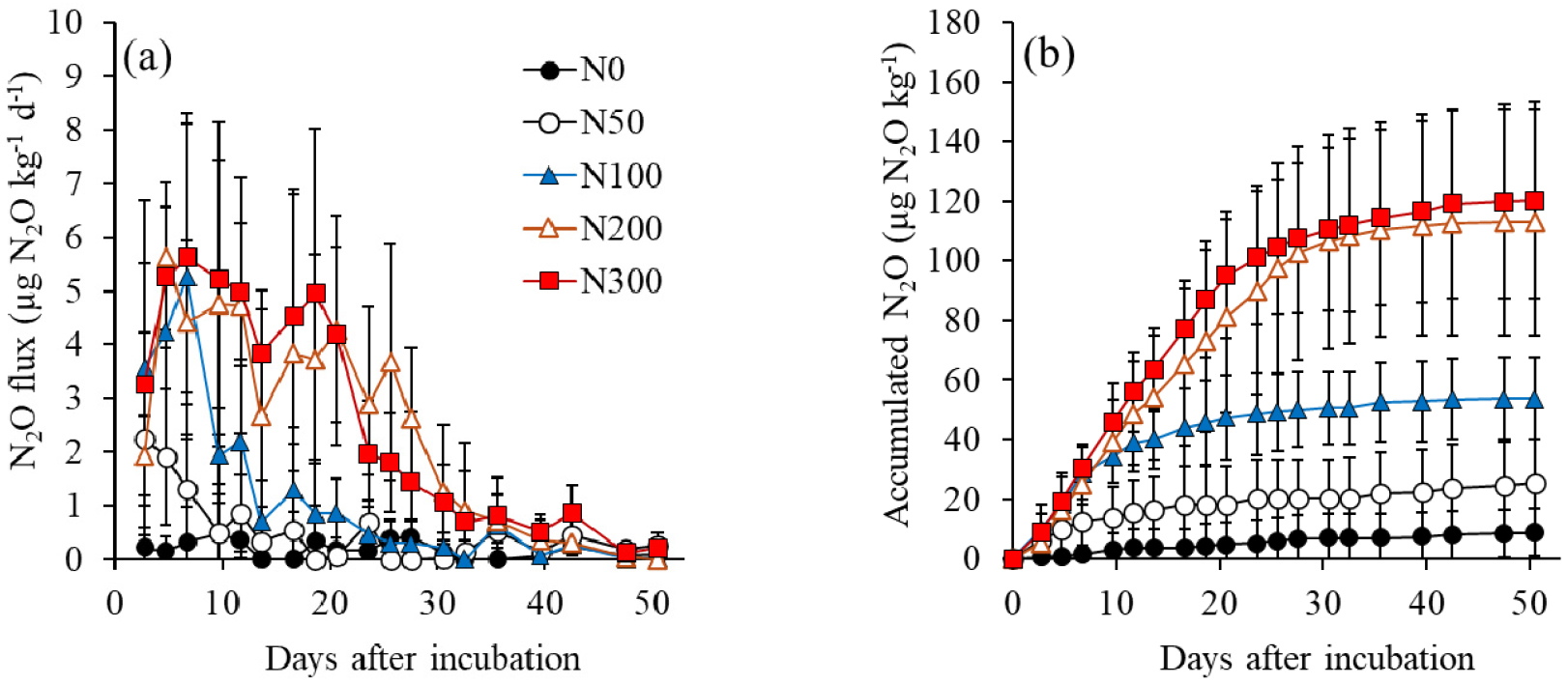
N2O 배출은 질소 처리량이 높을수록 더 활발하였다. 질소 무처리구에서는 전체 배양기간 동안 0.5 μg N2O kg-1 d-1 미만으로 배출이 거의 관찰되지 않았고, 암모늄 질소를 처리한 N50, N100, N200, N300 처리구에서는 질소 처리량이 높을수록 N2O 배출이 더 크고 더 오랫동안 지속되었다 (Fig. 6a). 처리량이 낮은 N50과 N100 처리구는 배양 초기 높았다가 이후 점차 감소하여 배양 후 7일과 17일 이후에는 1 μg N2O kg-1 d-1 미만으로 유지되었다. N100, N200, N300 처리구에서는 배양 후 21일까지 높게 유지되다가 31일 이후 거의 배출되지 않았다. 이러한 N2O 배출의 시기별 차이는 NH4+가 NO3-로 산화가 활발이 일어나는 시기와도 일치한다. N2O의 주요 생성 경로는 호기 조건에서의 질산화와 혐기 조건에서의 탈질 과정으로 알려져 있으며 (Bateman and Baggs, 2005; Wang et al., 2021), 본 연구에서는 배양기간 동안 토양 수분함량을 포장용수량으로 조절하고 주기적으로 환기하여 호기 조건을 유지하였다. 또한, N2O 배출은 토양 NH4+-N 농도가 높은 시기에 활발하였으며 (Figs. 2a and 6), NO3--N 손실은 관찰되지 않았다 (Fig. 2b). 이는 NO3-를 기질로 하는 탈질 과정 보다는 질산화 과정이 더 우세하였음을 보여준다.
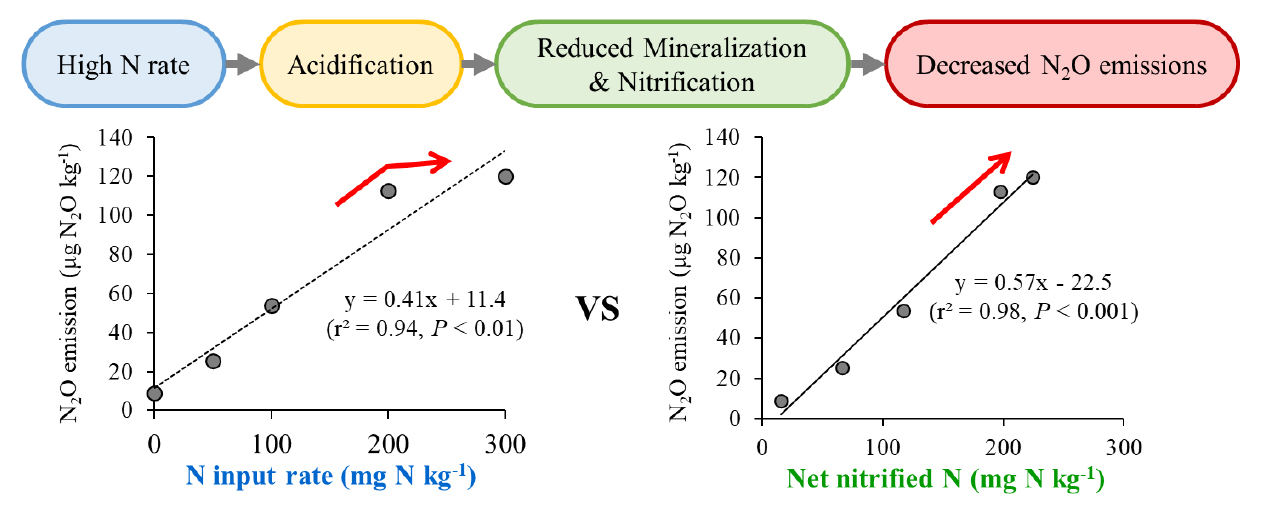
질소 처리량이 높을수록 N2O 누적 배출량은 증가하였다 (Fig. 6b). N0, N50, N100, N200, N300 처리구의 누적 배출량은 각각 8.8, 25.6, 53.6, 112.9, 120.3 μg N2O kg-1로 처리량에 따라 증가하였으며, N300 처리구의 경우 N200 처리구에 비해 7% 더 높았지만 통계적 유의성은 없었다 (P > 0.05). 이와 같은 관계를 반영하여 선형 회귀분석을 수행한 결과, 질소 처리량은 N2O 누적 배출량을 유의하게 설명하였으며 (r2 = 0.94, P < 0.01, n = 5; Fig. 7), 암모늄 질소 처리량이 1 mg N kg-1 증가할 때 N2O 누적 배출량은 0.41 μg N2O kg-1 증가하는 것으로 나타났다. 한편, 토양내 NH4+가 잔존한 N300 처리구를 제외한 경우 회귀모형의 설명력은 더욱 증가하였으며 (r2 = 0.99, P < 0.01, n = 4), 이때 암모늄 질소 처리량이 1 mg N kg-1 증가할 때 N2O 누적 배출량의 증가량도 0.53 μg N2O kg-1로 높아졌다. 이와 같이 고농도로 처리한 N300을 제외할 경우 유의성이 높아지고 질소 처리량 당 배출량이 높아지는 것은, N2O 배출이 질산화 과정에서 일어나는 것을 의미하고 N300의 고농도 처리 조건에서 질산화 반응이 억제되었을 가능성을 보여주는 결과이다.
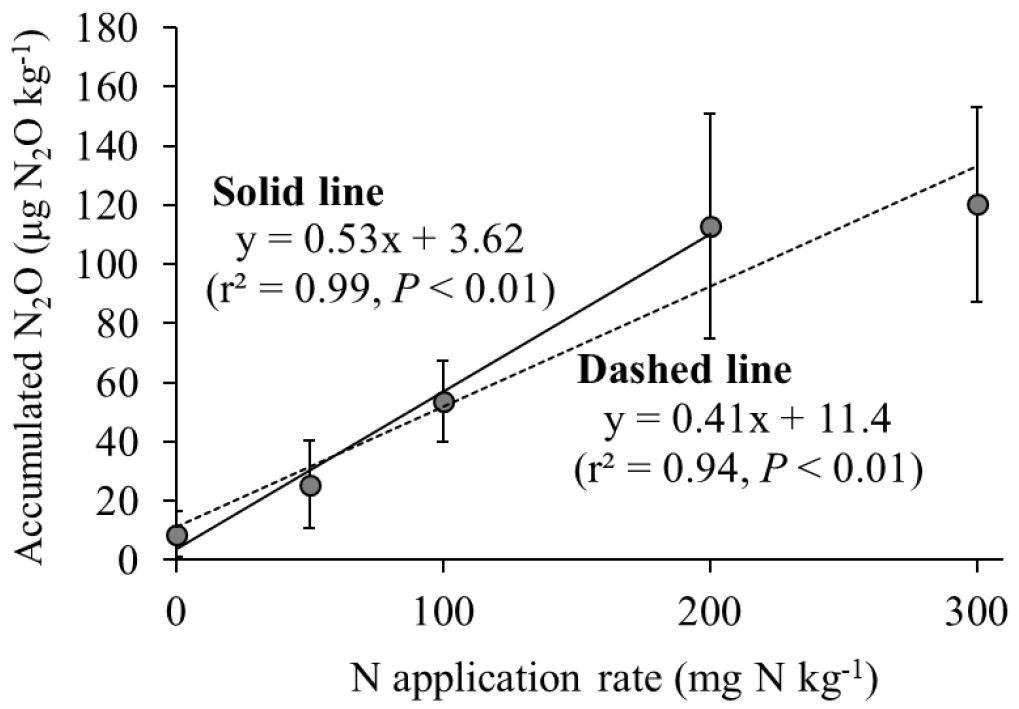
Fig. 7
Relationship between N application rates and accumulated N2O emissions. Vertical bars represent standard deviations (n = 4). The solid line represents the regression line for N application rates from 0 to 200 mg N kg-1, whereas the dashed line represents the regression line including 300 mg N kg-1.
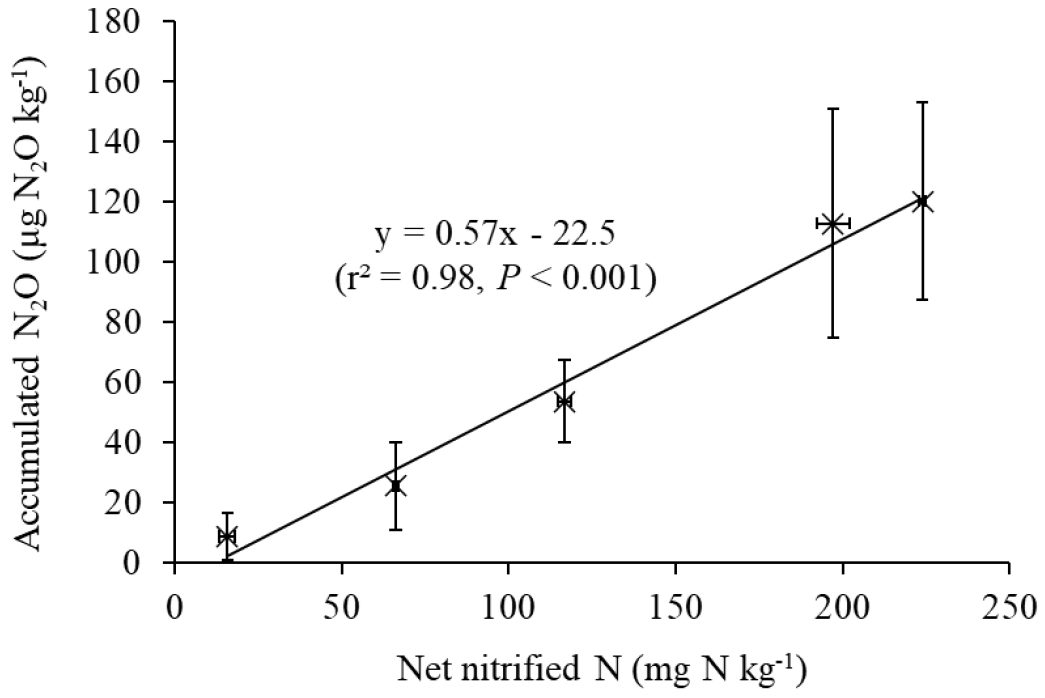
본 실험 조건인 호기성 토양에서 N2O 누적 배출량은 질산화 반응의 진행 정도와 직접적으로 연관될 수 있다. 이때 질산화 반응의 진행 정도는 NH4+-N 농도 감소량 또는 NO3--N 농도 증가량을 이용할 수 있다. 그러나 NH4+-N 농도는 질산화 과정에서 감소하는 동시에 유기질소 무기화에 의해 증가할 수 있어, 질산화 반응의 순 진행 정도를 정확히 반영하지 못할 가능성이 있다. 특히, 고농도 처리구에서는 질산화 반응이 억제되어 NH4+가 충분히 산화되지 않고 높은 수준으로 잔존함에 따라, NH4+-N의 순 감소량이 실제 질산화 반응 양을 과소평가할 수 있다. 이에 따라 본 연구에서는 질산화 반응 정도를 평가하는 지표로 NO3--N 증가량을 활용하였다. 그 결과, N2O 누적 배출량과 순 질산화 양 사이에는 높은 설명력을 갖는 유의한 선형관계가 나타났으며 (r2 = 0.98, P < 0.001, n = 5; Fig. 8), 순 질산화 된 질소 양이 1 mg N kg-1 증가할 때 N2O 누적 배출량은 0.57 μg N2O kg-1 증가하는 것으로 나타났다. 이는 N2O 생성이 전반적으로 질산화 과정에서의 기질 전환 정도에 크게 의존함을 보여준다.
Conclusions
본 연구는 토양에서 질소 처리량이 N2O 배출에 미치는 영향을 구명하고자 호기 조건의 토양에 암모늄염을 0, 50, 100, 200, 300 mg N kg-1 수준으로 처리하여 배양 실험을 수행하였다. 질소 처리량이 증가할수록 토양 pH는 뚜렷하게 감소하였고, 고농도로 처리한 200과 300 mg N kg-1 처리구는 각각 4.9와 4.7로 낮아져 질소 무기화 및 질산화가 억제되는 경향을 보였다. N2O 배출은 질소 처리량이 증가할수록 높아졌으며, 200 mg N kg-1 처리구까지는 질소 처리 수준에 비례하여 증가한 반면, 300 mg N kg-1 처리구에서는 배출량이 200 mg N kg-1 처리구와 유의적인 차이가 없었다 (P > 0.05). 이는 과도한 암모늄태 질소 처리에 따른 토양 pH 감소가 질산화 반응 속도를 조절함으로써 반응에 참여한 기질의 양을 감소시킨 결과로 해석된다. 배양기간 동안의 질산화 반응 정도를 나타내는 NO3--N 농도 순 증가량과 N2O 누적 배출량 간에는 높은 설명력을 갖는 선형 관계가 나타났으며 (r2 = 0.99, P < 0.001), 이는 N2O 배출이 질소 처리량 보다는 질산화 반응의 누적 진행 정도에 의해 지배됨을 명확히 보여준다. 즉, 질소 유입량, 토양 산도 등의 환경요인은 질산화 반응을 조절함으로써 간접적으로 N2O 배출에 영향을 주며, 궁극적으로 N2O 배출량은 암모늄태 질소 투입량 보다는 질산화 과정 동안 암모늄이 질산으로 전환되는 양에 정량적으로 의존하는 것으로 나타났다. 향후 연구로서, 농경지에서 식물과 질산화 미생물은 암모늄태 질소를 경쟁적으로 이용하므로 작물재배 조건에서 암모늄태 질소 식물 이용과 N2O 배출에 대한 질소 투입량의 영향에 대해 정량적으로 평가할 필요가 있다.