Introduction
Materials and Methods
항생제 배지 제조
종자 소독 및 작물생육
뿌리 길이 측정 및 엽록소 함량 조사
실험 통계분석
Results and Discussion
항생물질이 작물 뿌리 발달에 미치는 영향
항생물질이 작물 엽록소 함량에 미치는 영향
Introduction
항생제는 약 60년 전부터 인간과 가축의 질병 치료 목적으로 이용되고 있다 (Knapp et al., 2009). 그리고 인간의 병 치료 보다 더 많은 양의 항생제가 가축의 질병 치료와 성장촉진 용으로 사용되고 있다 (Gelband et al., 2015). 지난 10 연간 국내에서 평균 900 ton/year의 축산용 항생제가 판매되었으며 이 중 Tetracycline 계열의 항생제 비율이 가장 높았다 (The Republic of Korea Ministry of Agriculture, Food and Rural Affairs, 2017). 가축 체내에서의 항생제는 낮은 생물학적 분해율 때문에 투입량의 30 - 90%가 분뇨의 형태로 배출된다 (Eichhorn and Aga, 2004; Bártíková et al., 2016). 우리나라의 경우, 배출되는 가축분뇨의 약 90%는 퇴·액비 형태로 우리나라 농경지 개량에 활용된다. 따라서 우리나라의 경우 상당량의 항생제가 농경지로 유입될 것으로 예측된다 (Kim et al., 2020).
항생물질의 농경지 잔류는 다양한 형태로 인간의 건강과 자연 생태계에 영향을 미치고 있다. 예를 들어, 항생물질은 화학적/생물학적 분해에 대한 안정성 때문에 토양 내의 잔류 시간이 길며 이로 인해서 작물 생육기간 동안 잔류량을 증가시킨다 (Sarmah et al., 2006; Du and Liu, 2012; Kim et al., 2019). 항생제의 환경 노출에 대한 가장 큰 이슈는 항생제 저항성 박테리아 출현율 증가와 항생제 저항성 유전자의 발현 증가이며, 이에 대한 다양한 연구가 진행되고 있다 (Knapp et al., 2009; Kang et al., 2017; Kuppusamy et al., 2018). 그러나 항생제의 농작물 독성에 대한 연구결과는 아직까지 상대적으로 부족한 편이다 (Pan and Chu, 2016; Rydzynski et al., 2019). 항생제의 종류와 농도에 따라 작물 생장에 대한 연구의 필요성이 강조되고 있다. Liu et al. (2009)에 의하면 Chlortetracycline, Tetracycline 외 4종의 항생제에 대한 벼, 귀리, 오이의 종자 발아시험에서 벼의 뿌리 신장이 가장 크게 억제 되었다. 그리고 Tetracycline, Sulfamethazine, Norfloxacin, Erythromycin, Chloramphenicol 중에서 Tetracycline이 종자 발아와 뿌리 신장에 가장 큰 독성을 보였으며, 작물 (상추, 토마토, 당근, 오이) 중에서는 상추가 가장 항생물질에 대하여 민감한 것으로 보고 하였다 (Pan and Chu, 2016). 반면 Hillis et al. (2011)은 동일한 항생물질에서 상추보다 당근이 더 항생물질에 대해 민감한 것으로 보고하였다. 본 연구에는 항생물질 중 사용량이 가장 많고, 농경지 잔류가 비교적 높은 (0.003 - 100 mg/kg) (Hamscher et al., 2002; Martínez-Carballo et al., 2007; Massé et al., 2014) Tetracycline, Chlorotetracycline, Oxytetracycline을 선택하였다. 그리고 우리나라 대표적인 잎채소와 뿌리채소인 상추, 배추 무를 대상으로 항생물질이 작물생육에 대한 영향을 평가하여 미래 농경지 안전관리 기초자료로 활용하고자 한다.
Materials and Methods
항생제 배지 제조
본 연구에서는 Tetracyclines 계열의 Tetracycline (TC), Chlortetracycline (CTC), Oxytetracycline (OTC) (>98%, Sigma-Aldrich) 3가지 항생물질을 1,000 mg/L stock으로 제조하여 사용하였다. 항생제 배지를 만들기 위하여 증류수에 1.2% agar를 넣고 고온고압멸균 처리하였다. 멸균처리가 된 배지에 각각 TC, CTC, OTC 1,000 mg/L stock을 이용하여 0, 5, 10, 20 mg/L의 항생물질이 포함된 배지를 제조하였다. 이는 가축분뇨에서 검출되는 Tetracycline 계열의 항생물질 농도를 기준으로 (Martínez-Carballo et al., 2007) 설정하였다. 항생제 배지는 스퀘어디쉬 (12 × 12)에 굳혀 종자생육배지로 사용하였다.
종자 소독 및 작물생육
대상 작물인 상추 (Lactuca sativa), 배추 (Brassica campestris) 그리고 무 (Raphanus raphanistrum) 종자는 생육 시 곰팡이 억제를 위해 4% NaClO 용액을 사용하여 소독 하였다 (Lee et al., 2019). 소독된 종자는 항생제 배지 스퀘어디쉬 (12 × 12) 상부에 심고, 작물 생장을 위해 5일간 수직으로 식물배양기 (growth chamber)에서 배양하였다. 이때 식물 배양기 생육조건은 20°C, 상대습도 75%, 단일조건인 8시간 (낮), 16시간 (밤) 조건이었다. 모든 처리구는 3반복으로 진행되었다.
뿌리 길이 측정 및 엽록소 함량 조사
항생물질이 작물의 지상 및 지하부 생육에 미치는 영향은 엽록소 함량과 뿌리길이로 평가하였다. 작물의 지상부인 식물의 떡잎을 수확해 95% 에탄올에 떡잎이 백색이 될 때까지 엽록소를 추출하였다. 추출된 에탄올을 664 nm와 649 nm에서 흡광도를 측정하여 생체중으로 총 엽록소 함량을 Chlorophylla = 13.36A664 - 5.19A649, Chlorophyllb = 27.43A649 - 8.12A664 식을 이용하여 계산하였다 (Sumanta et al., 2014). 지하부 뿌리 길이는 5일간의 생육 후 Image J 프로그램을 이용하여 측정하였다.
실험 통계분석
항생제에 농도에 대한 작물의 뿌리 신장과 엽록소 함량 차이는 SAS (version 9.1.3)를 이용하여 분산분석과 최소유의차 (LSD, p < 0.05) 검증을 실시하였다.
Results and Discussion
항생물질이 작물 뿌리 발달에 미치는 영향
Tetracycline 계열 3종 항생물질 (TC, CTC, OTC)을 0, 5, 10, 20 mg/L agar 배지에 상추, 배추, 무 대상으로 발아율과 초기 뿌리 신장을 조사한 결과 작물의 발아율은 차이가 없었다. 그러나 항생물질의 농도에 따라서 작물의 뿌리 생장은 유의성 있는 차이를 보였다. 상추의 경우 Tetracycline 5 (TC 5), 10 (TC10), 20 (TC20) mg/L에서는 무처리구 대비 각각 40, 67, 77% 뿌리신장억제가 있었으며, Chlortetracycline 5 (CTC 5), 10 (CTC10), 20 (CTC20) mg/L에서는 무처리구 대비 뿌리신장억제는 각각 64, 76, 78%였으며, Oxytetracycline 처리에서도 동일한 경향을 보였다 (Fig. 1. b, e, h).
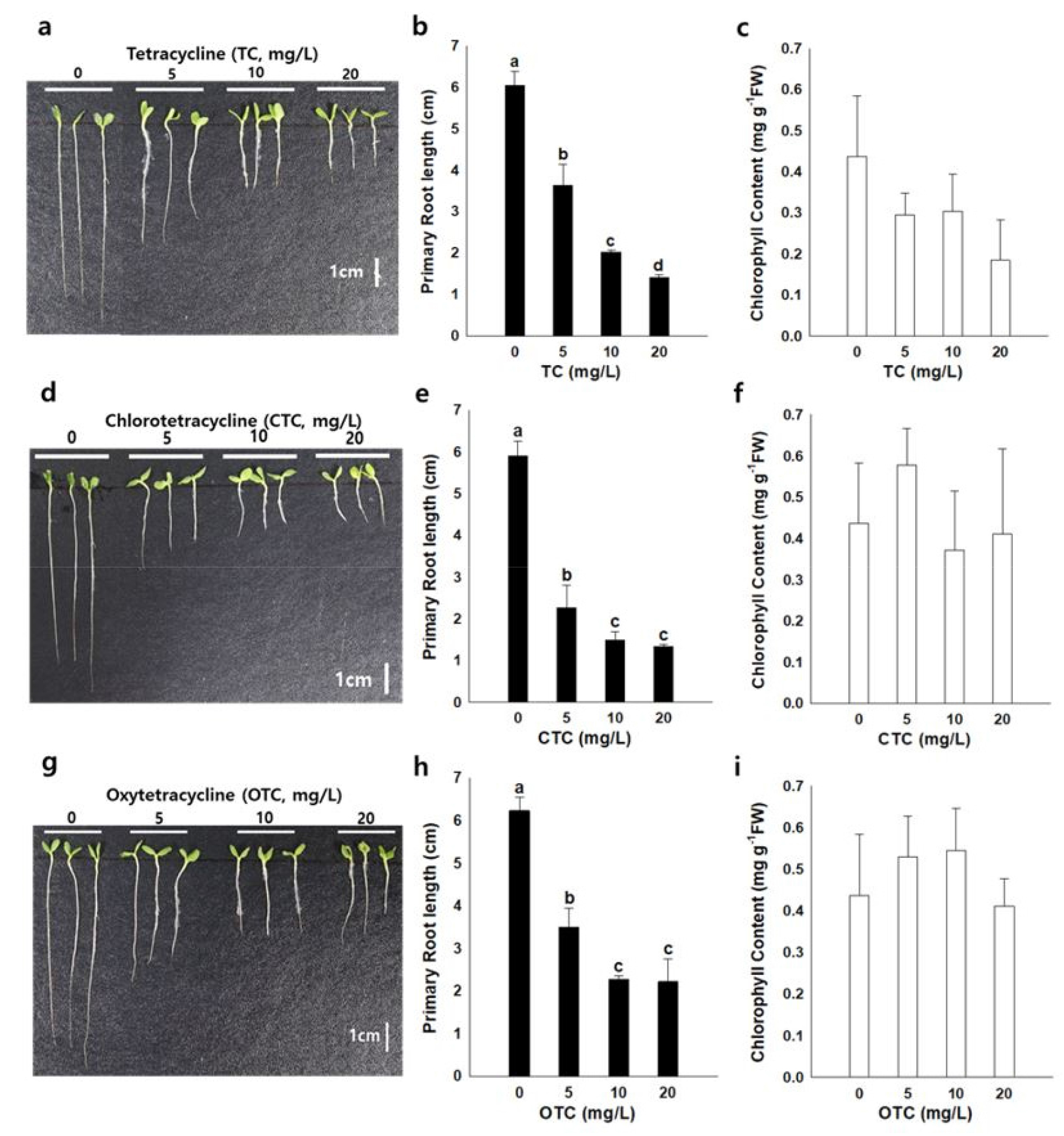
Fig. 1
Effects of Tetracycline (TC), Chlorotetracycline (CTC), and Oxytetracycline (OTC) treatments on seedling growth in Lactuca sativa. Seeds were cultured in deionized and distilled water containing TC, CTC, and OTC at 0, 5, 10, and 20 mg/L for 5 days. Morphological phenotype a)TC, d)CTC, and g)OTC. Primary root length b)TC, e)CTC, and h)OTC. Chlorophyll content c)TC, f)CTC, and i)OTC. Asterisks indicate the significant differences between the control (0 mg/L) and the treatments (5, 10, and 20 mg/L) (*; p < 0.05, **; p < 0.01, ***; p < 0.001).
항생물질이 무의 초기 뿌리신장억제에 미치는 영향은 상추와 동일한 경향을 보였다 (Fig. 3. b, e, h). 배추의 경우 TC와 CTC가 뿌리발달에 미치는 영향은 상추 및 무와 동일한 경향을 보였지만 OTC의 경우 항생물질이 뿌리신장 억제에는 영향을 미쳤지만 농도에 따른 생육억제는 나타나지 않았다 (Fig. 2. b, e, h). 배추에서는 OTC에게 받는 감도가 TC와 CTC에 비하여 적다는 것을 추측할 수 있다. 작물의 생육억제에 대한 항생물질 영향은 항생물질과 작물의 종류에 따라서 상이한 결과를 나타내고 있다 (Hillis et al., 2011). Tetracycline 계열의 항생물질은 종자의 발아에는 영향을 미치진 않지만 뿌리 신장에는 영향을 미치는 것으로 보고되고 있다 (Bellino et al., 2018). Tetracycline 계열 항생물질이 작물의 뿌리신장 억제는 산화적 스트레스 유발 (Han et al., 2019), 뿌리신장에 관여하는 H2O2 신호전달 방해 (Cheong et al., 2020), 그리고 뿌리의 세포분열 억제에 의한 것이라고 생각된다 (Yu et al., 2017). 항생물질에 의한 작물의 생육억제는 항생물질 및 작물의 종류뿐만 아니라 항생물질의 잔류 농도에도 큰 영향을 받는다. Zhang et al. (2016)은 중국의 125개 표토에서 항생물질의 농도는 분석한 결과 OTC 가 최고 8.4 mg/kg이 검출되었고, 돈분에는 20 - 46 mg/kg의 TC 계열의 항생물질이 검출되었다 (Martínez-Carballo et al., 2007). 본 연구에서 실시한 TC 계열의 항생물질 농도 5 - 20 mg/kg에서 나타난 작물 초기 뿌리신장억제는 실제 가축분퇴비 장기 연용 농경지에서 일어날 가능성이 있으므로 추가적인 연구 수행이 필요할 것으로 판단된다. 따라서 농경지 항생물질 잔류에 의한 작물의 생육억제에 대한 다양한 연구가 필요할 것으로 생각된다.
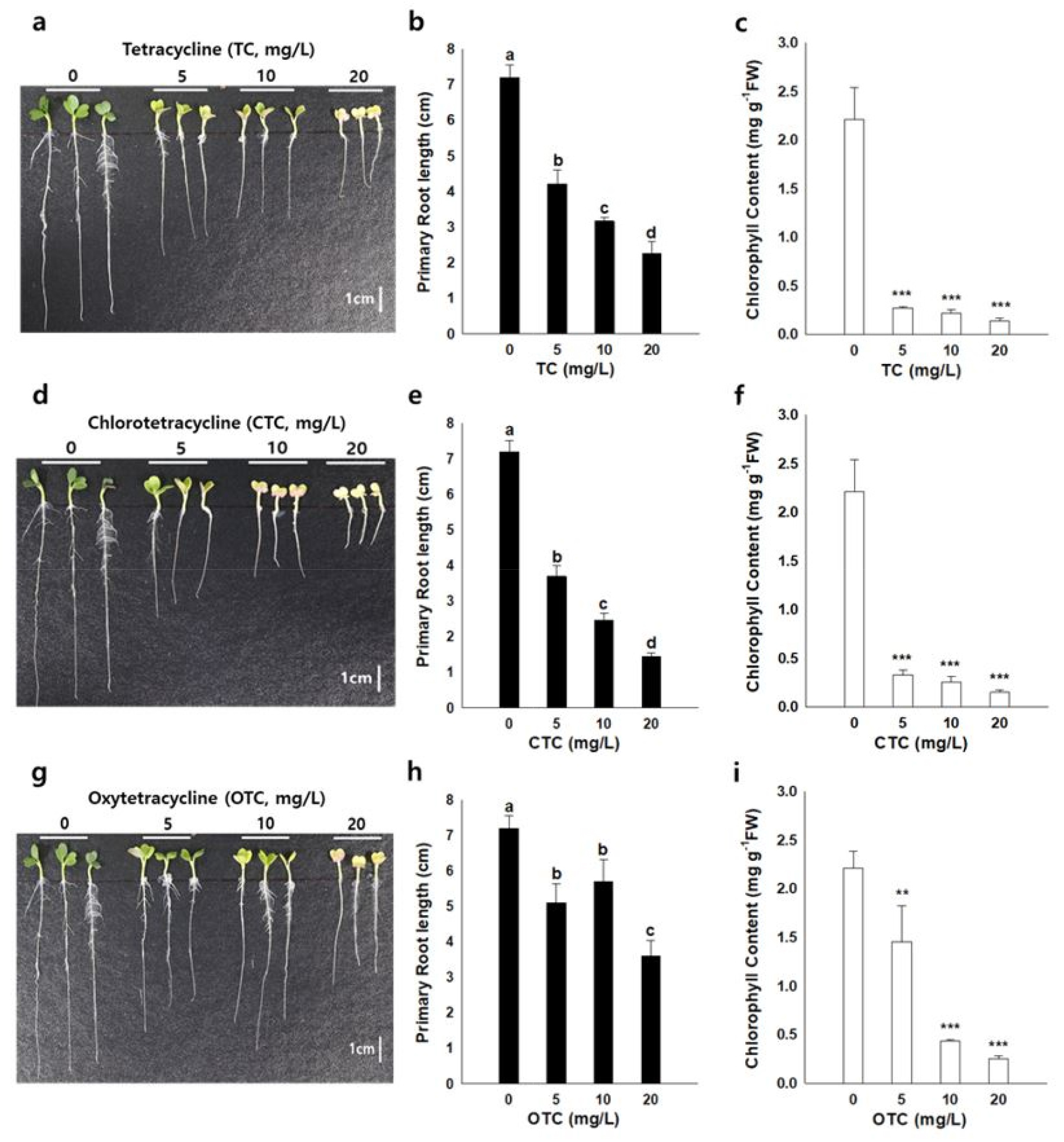
Fig. 2
Effects of Tetracycline (TC), Chlorotetracycline (CTC), and Oxytetracycline (OTC) treatments on seedling growth in Brassica campestris. Morphological phenotype a)TC, d)CTC, and g)OTC. Primary root length b)TC, e)CTC, and h)OTC. Chlorophyll content c)TC, f)CTC, and i)OTC. Asterisks indicate the significant differences between the control (0 mg/L) and the treatments (5, 10, and 20 mg/L) (*; p < 0.05, **; p < 0.01, ***; p < 0.001).
항생물질이 작물 엽록소 함량에 미치는 영향
Tetracycline 계열 3종 항생물질 (TC, CTC, OTC)은 상추, 배추 및 무의 발아 후 엽록소 합성을 크게 억제하는 것으로 나타났다. 배추에서는 항생제 종류와 농도에 따라 엽록소 함량은 TC 5, 10, 20에서는 각각 0.27 ± 0.02, 0.22 ± 0.04, 0.14 ± 0.03 mg/g, CTC 5, 10, 20에서는 각각 0.33 ± 0.05, 0.26 ± 0.05, 0.15 ± 0.02 mg/g, OTC 5, 10, 20에서는 각각 1.46 ± 0.37, 0.43 ± 0.02, 0.25 ± 0.03 mg/g로 무처리에 비해 유의성 있게 감소하였다 (Fig. 2. c, f, i). 무의 경우도 OTC 5 mg/L 처리를 제외하고 배추와 동일한 경향을 보였다(Fig. 3. c, f, i). 상추의 경우, 무처리에 비해 TC 계열의 3가지 항생물질을 처리했을 때 유의성 있는 영향이 나타나지 않았다 (Fig. 1. c, f, i). Li et al. (2011)에 의하면 항생물질은 농도 증가에 따라서 작물의 엽록소 함량은 현저히 감소 하였고, 이는 항생물질의 노출시간에 따라서 다른 결과를 보였다 (Rydzyński et al., 2017). 본 연구의 대상 작물인 상추는 국화과 작물로서 십자화과 작물인 배추와 무와 TC 계열의 항생물질이 엽록소 함량 변화에 미치는 영향이 상이하였다. 그러나 Yang et al. (2020)의 연구에서는 TC와 OTC 250 mg/kg 처리 후 20일간 상추 재배에서 엽록소 함량 감소가 있었다. 따라서 항생물질에 의한 작물의 엽록소 감소는 항생물질의 농도와 노출 시간에 영향을 받으며 항생물질이 작물의 생육 억제에 미치는 영향은 동일한 항생물질이라도 작물에 따라서 다른 작용 메커니즘이 있는 것으로 나타났다.
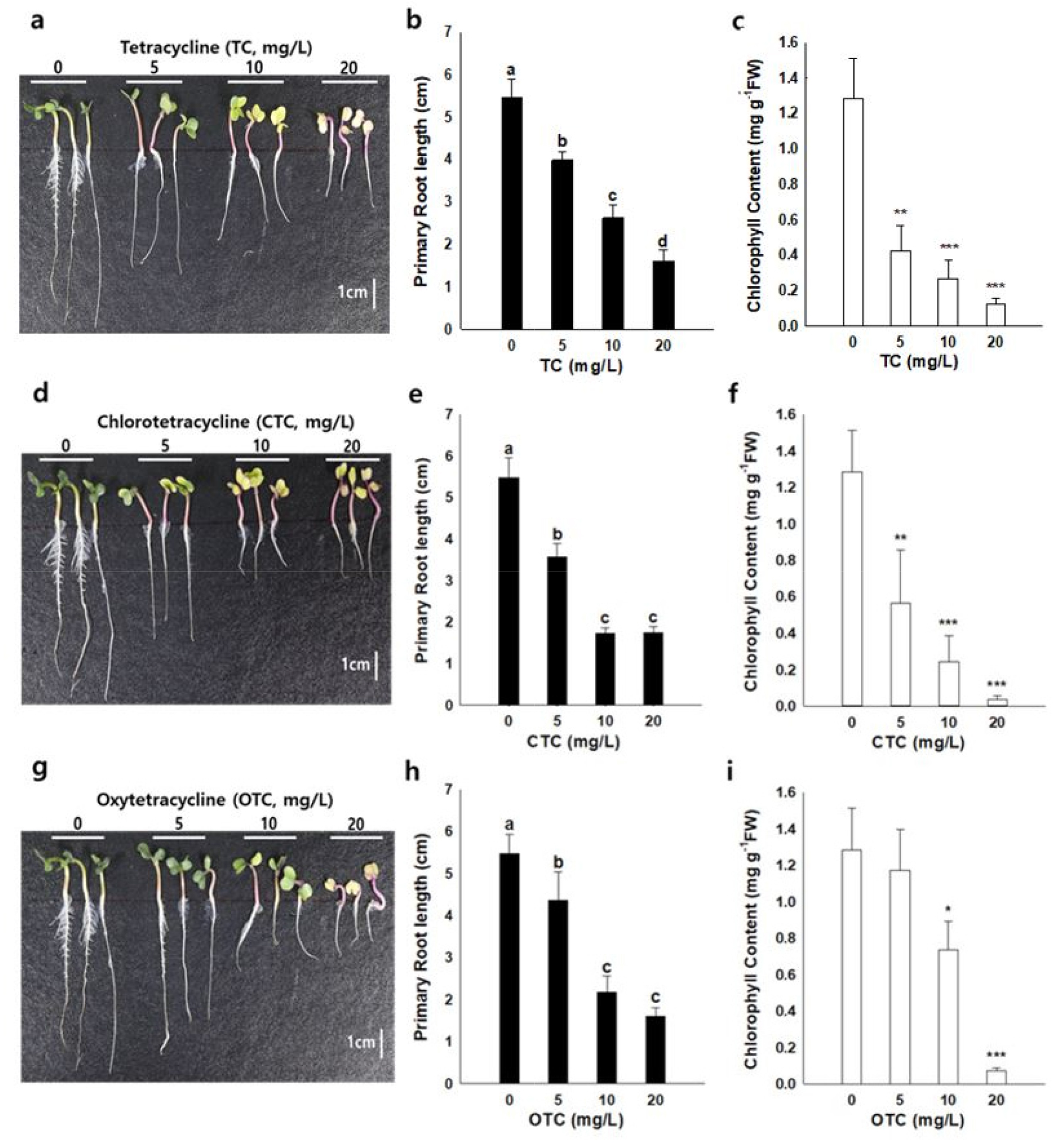
Fig. 3
Effects of Tetracycline (TC), Chlorotetracycline (CTC), and Oxytetracycline (OTC) treatments on seedling growth in Raphanus raphanistrum. Morphological phenotype a)TC, d)CTC, and g)OTC. Primary root length b)TC, e)CTC, and h)OTC. Chlorophyll content c)TC, f)CTC, and i)OTC. Asterisks indicate the significant differences between the control (0 mg/L) and the treatments (5, 10, and 20 mg/L) (*; p < 0.05, **; p < 0.01, ***; p < 0.001).
Tetracycline 계열 3종 항생물질 (TC, CTC, OTC)과 상추, 배추 및 무 작물 종류에 따라서 뿌리 생육 및 엽록소 합성을 억제시키는 효과가 있었으며, 작물에 따라 차이가 다르게 나타났다. 이는 작물이 농경지에 잔류 되어있는 항생물질을 흡수하고 생장했을 때 작물별로 다양한 영향을 끼칠 것으로 판단된다. 따라서 다양한 작물에 항생물질 작용 메커니즘 구명 및 항생물질 잔류 안전 기준을 설정 할 수 있는 연구가 필요함을 시사한다.