Introduction
세계적인 산업화 및 도시화는 농경지, 농업용수 그리고 생활용수 등의 오염수준을 급속히 증가시키고 있다 (Galiulin et al., 2001; Kirkham, 2006). 카드뮴 오염은 환경적으로 부정적인 영향을 끼칠 뿐만 아니라 먹이사슬의 최정상에 위치한 인간의 건강을 위협하는 치명적인 위해요소로 간주되고 있다 (Jan et al., 2015; Nagajyoti et al., 2010). 카드뮴은 전반적인 식물생장에 부정적으로 작용하며 세포분열을 방해하여 뿌리의 신장을 억제할 뿐만 아니라 보조인자로 필수금속이온 (Cu, Zn, Mn, Fe 등)을 포함한 단백질들의 금속이온을 치환함으로써 펜톤반응 (fenton reaction)을 일으키고, superoxide 음이온 라디칼 (O2•−), 과산화수소 (H2O2) 및 수산기 라디칼 (hydroxyl radical, OH•) 등의 활성산소종 (reactive oxygen species, ROS)을 발생시켜 세포 내에서 지질과산화작용을 야기함으로써 세포막을 파괴하고 최종적으로 세포를 사멸시킨다 (Barceló et al., 1988; Jung et al., 2015, 2016; Lagriffoul et al., 1998; Vassilev and Yordanov, 1997; Vassilev et al., 1997). 특히 카드뮴에 의해 발생된 산화적 스트레스는 활성산소종의 세포 내 축적으로 인하여 탄수화물, 단백질, 지질 및 핵산의 생합성에 부정적인 영향을 미치고 산화․환원 항상성을 교란하여 정상적인 생체 기능을 저해한다 (Gayomba et al., 2013; Singh and Agrawal, 2010; Singh et al., 2006, Xu et al., 2014).
식물에서 카드뮴의 흡수 정도는 토양 중에 존재하는 함량에 비례적으로 흡수되어지고, 일단 흡수된 카드뮴은 세포 내외 또는 특정조직에 축적된다 (Jung et al., 2016; Yan et al., 2010a, 2010b). 그러나 식물은 과도하게 흡수된 카드뮴의 독성을 최소화하기 위해 다양한 생리․생화학적 방어시스템을 가동하여 식물독성을 극복하고자 한다 (Raven and Loeppert, 1997; Salt et al., 1995). 카드뮴에 의해 유도된 활성산소종의 소거는 항산화효소 (superoxide dismutase (SOD), catalase (CAT), peroxidase (POD), ascorbate peroxidase (APX), glutathione reductase (GR))에 의한 효소적인 소거와 항산화제 (ascorbate (AsA), glutathione (GSH))에 의한 비효소적 소거를 기반으로 한, 무독화 시스템이 생체 내의 주요한 활성산소종 소거전략으로 정설화되어 있다 (Gill and Tuteja, 2010; Talukdar, 2012; Zhang et al., 2013). 카드뮴에 의해 유도되는 활성산소종의 소거에 항산화효소 및 비효소적인 GSH의 역할과 기능은 여러 연구를 통하여 잘 구명되었지만 (Harada et al., 2002; Meuwly and Rauser, 1992), 산화적인 스트레스에 의해 야기된 활성산소종 소거, 산화․환원 (redox) 조절, 세포주기, 세포성장 및 손상된 DNA 복구 등에 관여하는 AsA의 기능과 역할은 아직도 연구가 미흡한 상태이다 (Kerk and Feldman, 1995; Luwe, 1996).
카드뮴의 식물전이는 작물의 재배환경과 더불어 여러 이온들의 상호작용에 따라 흡수 및 축적되는 정도가 상이하게 나타난다 (Fergusson, 1990; Jung et al., 2016; Lee et al., 2012; Park et al., 2009). 비료의 3요소 중의 하나인 인과 중금속인 비소의 길항작용에 관한 연관성 연구는 여러 연구보고들을 통하여 확실한 정설로 자리매김을 하고 있는 실정임에도 불구하고 (Brachhage et al., 2014; Gomes et al., 2014), 카드뮴과 인의 상호연관성 연구는 일부 식물에서의 연구를 제외하고 아직도 미진한 상태이므로 깊이있는 연구가 필요할 것으로 판단된다 (Arshad et al., 2016). 인은 식물의 주된 에너지원인 아데노신 삼인산 (adenosine triphosphate, ATP) 생성과 여러 효소반응을 촉진하여 Cd의 독성에 의해 발생되는 활성산소종 소거에 관여할 뿐만 아니라 식물의 생장촉진에도 효과를 나타낸다 (Jalil et al., 1994; Mishra et al., 2014). 그럼에도 불구하고 Cd과 P의 상호연관성 해석에 하나의 핵심 단서가 될 수 있는 항산화제의 변화에 대한 연구 또한 미비한 상태이다.
따라서 본 연구는 카드뮴오염지에서 벼의 식물독성경감을 위한 처리인자를 탐색하고자 인시용에 따른 카드뮴의 식물전이를 평가하였고, 카드뮴에 의한 식물독성과 연관된 활성산소종 및 항산화제의 항상성을 조사하였다. 이를 통하여 카드뮴 이행절감 기술개발과 안전한 농산물생산에 기초적 및 응용적 자료를 제공하고자 수행하였다.
Materials and Methods
공시식물 동진벼 종자를 70% 에탄올로 2분간 멸균하고, 증류수로 여러 번 세척한 다음, 2 mL L-1 농업용 살균제 (8% ipconazole) 용액에서 48시간 동안 표면살균한 후 증류수로 종자를 완전히 헹구었다. 살균된 종자를 30°C에서 48시간 침종 및 발아시킨 후 균일하게 생장한 1.5~2.0 엽기의 유묘를 선별하여 수경액 (1 mM NH4NO3, 0.6 mM NaH2PO4․H2O, 0.3 mM K2SO4, 0.2 mM CaCl2, 0.4 mM MgCl2․6H2O, 45 µM Fe-EDTA, 50 µM H3BO3, 9 µM MnCl2․4H2O, 0.3 µM CuSO4․5H2O, 0.7 µM ZnSO4․7H2O, 0.1 µM Na2MoO4․2H2O, pH 5.6)으로 채워진 수경재배용 베드 (원예용 2호 고베드, 가화텍)에 이식하고, 자연광에서 주야간의 평균온도 30/25°C, 상대습도 60/80%로 유지되는 유리온실 (국립농업과학원) 조건 하에서 4 엽기까지 생육시킨 식물체를 본 연구의 실험재료로 이용하였다 (Jung et al., 2015; Kamachi et al., 1991). Jung et al. (2015)에 의해 결정된 벼 생리활성연구를 위한 카드뮴 (Cd, CdCl2) 적정처리농도인 30 µM과 수경재배시 인 (P, NaH2PO4․H2O)의 추천농도인 0.6~3.0 mM 범위보다 높은 6 mM P을 본 연구를 위한 적정처리농도로 결정하였다. 또한 Cd 및 P처리에 따른 pH 변화는 무처리의 5.5~5.7 범위와 비교하여 유의적인 차이가 없었다. 생육이 균일한 4엽기의 유묘에 30 µM Cd 또는 6 mM P을 처리한 후 14일에 초장, 엽령, 그리고 지상부 건물중을 조사하였고, 생리 및 항산화제 분석을 위하여 식물체를 채취하였다. 그 채취된 식물체를 뿌리와 잎으로 분리하고, 각기 부위별로 100 mg씩을 E-tube에 넣어 액체질소로 급속 동결시킨 다음, -80°C의 초저온냉동고에 보관하였다.
식물체 내 카드뮴과 인 함량 분석 식물체 분석은 국립농업과학원 식물체 분석법에 준하여 실시하였다 (NAAS, 2011). 수경재배된 동진벼 4엽기에 30 µM Cd 또는 6 mM P을 처리하고, 14일 후에 식물체를 부위별 (뿌리, 잎)로 나누어 분리하여 약 5분 동안 증류수로 세척한 다음, 80°C에서 완전히 건조한 후 분쇄하여 분석에 이용하였다. 식물체의 Cd과 P함량 분석을 위하여 시료의 분해는 Graphite Block Acid Digestion System (ODLAB Co., Ltd. Seoul, Korea)을 이용하였고, 분말시료 200 mg에 질산 14 mL을 넣고 산분해한 분해액을 여과지 (No. 40, Whatman, Buckinghamshire, UK)에서 미세한 불순물을 제거한 다음에 유도결합플라즈마 질량분석기 (ICP-MS, Agilent 7900, Agilent Technologies Inc., Santa Clara, CA, USA)를 사용하여 Cd과 P 함량을 측정하였다.
활성산소종과 지질과산화 분석 Superoxide 음이온 라디칼 (superoxide anion radical, O2•−) 함량은 Elstner and Heupel (1976)에 의해 기술된 방법을 사용하여 측정하였다. 식물체를 막자사발에 넣고 액체질소로 급속 동결시킨 후, 미세한 분말이 되도록 마쇄한 다음, 시료에 1 mL의 50 mM K-phosphate buffer (pH 7.8)를 넣어 잘 혼합시켰다. 그 뒤 혼합액을 4°C에서 12,000 rpm의 속도로 10분간 원심분리하였다. 200 µL의 상징액에 50 µL의 10 mM hydroxylamine hydrochloride을 넣은 후, 25°C에서 60분간 반응시켰다. 그 반응시료에 100 µL의 1% sulfanilamide과 100 µL의 7 mM napthylamine을 첨가하여 최종 반응액을 조제하였다. O2•−함량은 530 nm에서 분광광도법으로 측정하였고, 표준 NaNO2 회귀곡선을 도출하여 계산에 이용하였다.
과산화수소 (hydrogen peroxide, H2O2) 함량은 Jana and Choudhuri (1982)의 방법을 이용하여 분광광도계로 측정하였다. 위의 O2•−함량분석에서 최초로 원심분리된 200 µL의 추출액에 20% H2SO4에 0.1% TiCl4가 용해되어 있는 반응액 200 µL 넣은 후, 10,000 rpm의 속도로 30분간 원심분리하여 얻은 상징액을 분광광도계를 이용하여 410 nm에서 측정하였다. H2O2 함량은 0.28 µM-1 cm-1의 몰흡광계수 (molar extinction coefficient)를 사용하여 산출하였다.
지질과산화작용의 지표화학물질인 malondialdehyde (MDA) 생성량을 thiobarbituric acid (TBA) 방법을 이용하여 측정하였다. 식물체를 막자사발에 넣고 20% trichloroacetic acid (TCA)에 0.5% TBA가 용해되어 있는 용액을 5 mL 넣어 마쇄한 다음, 20,000 g의 속도로 15분간 원심분리하여 상징액을 취하였다. 이 상징액을 100°C에서 25분간 끓인 다음 ice bath에 넣어 냉각시킨 후, 다시 20,000 g의 속도로 15분간 원심분리하여 최종적으로 얻은 상징액을 분광광도계를 이용하여 532 nm에서 흡광도를 측정하고, 600 nm에서의 흡광도 값으로 보정하였다. MDA 생성량은 156 mM-1 cm-1의 몰흡광계수를 이용하여 산출하였다 (Buege and Aust, 1978).
항산화제 분석 시스테인 (cysteine, Cys) 함량은 Gaitonde (1967)의 방법을 이용하여 측정하였다. 560 nm에서 시료의 흡광도를 측정하고, 표준회귀곡선을 이용하여 시스테인 함량을 산출하였다.
글루타티온 (glutathione, GSH) 함량을 측정하기 위하여, 식물체를 막자사발에 넣고 액체질소로 급속 동결시킨 후, 미세한 분말이 되도록 마쇄하였다. 그 시료에 1.2 mL의 5% (w/v) 5-sulfosalicylic acid를 넣어 GSH의 산화를 감소시켰고, 그 뒤 혼합액을 4°C의 12,000 g의 속도로 10분간 원심분리하였다. 200 µL의 상징액에 800 µL의 반응액 (143 mM Na-phosphate buffer (pH 7.5), 6.3 mM EDTA, 0.22 mM nicotinamide adenine dinucleotide phosphate (NADPH))을 넣은 후 100 µL의 6 mM 5,5-dithiobis-2-nitrobenzoic acid (DTNB)를 첨가하여 최종 반응액을 조제하였다. 반응 개시를 위하여 0.5 unit의 GSH 환원효소 (GSH reductase)의 첨가하고, 412 nm에서 1분 동안 흡광도의 변화를 측정하였다. 여러 농도의 GSH로 표준회귀곡선을 작성하여 각기 시료의 GSH 함량을 산출하였다 (Meister and Anderson, 1983).
아스코베이트 (ascorbate, AsA)는 Law et al. (1983)에 의해 개발된 측정법을 약간 변형하여 측정하였다. 각 시료의 흡광도는 525 nm에서 기록되었고, 여러 농도의 AsA를 이용하여 표준회귀곡선을 작성하고, 회귀식에 각기 측정된 시료의 흡광도를 대입하여 AsA 함량을 계산하였다.
통계처리 본 연구는 완전임의 배치 3반복으로 온실에서 수행하였고, 모든 데이터의 통계처리는 Statistical Analysis Software (SAS ver. 9.2) 프로그램을 이용하여 처리 간 분산분석 (ANOVA)을 실시하였다. 처리의 효과는 Fisher 최소유의차 검정 (p = 0.05)을 통하여 유의성 유무를 판단하였고 데이터는 평균값 ± 표준오차로 표현하였다.
Results and Discussion
카드뮴 독성에 따른 식물생장반응에 미치는 인의 영향 수경재배된 4엽기의 벼 유묘에 Cd 및 P 처리에 따른 초장, 엽령 및 지상부 건물중을 조사한 결과는 Table 1과 같다. 모든 처리에서 엽령의 유의적인 차이는 확인할 수 없었던 반면 무처리와 비교한 Cd처리는 초장과 지상부 건물중 모두를 감소시켰다. 그렇지만 Cd + P처리에서는 Cd의 독성으로 인한 생장저해가 현저히 경감되었다 (Table 1). 이는 Cd 스트레스에 노출된 여러 식물종들의 경우에서도 P시용에 따라 건물중의 증가를 나타내는 보고와 유사한 결과를 보여주고 있다 (Jiang et al., 2007; Sajwan et al., 2002).

†Leaf age indicates the number of leaves.
‡Means within a column followed by the same letter are not significantly different at the 5% level based on Fisher’s least significant difference (LSD) tests.
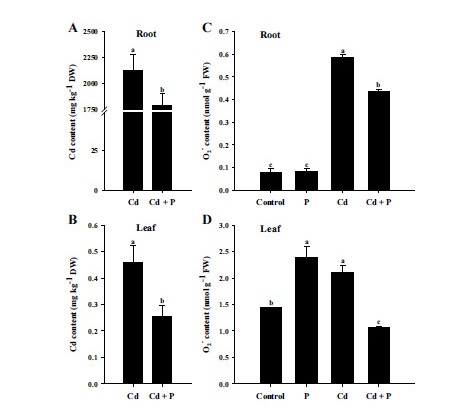
식물체 부위별 카드뮴전이 P시용에 따른 식물체 부위별 Cd의 식물전이 양상을 평가하기 위하여, Cd 또는 Cd + P처리 간에 Cd 및 P함량을 뿌리와 잎으로 나누어 처리 후 14일에 비교․분석하였다. 뿌리에서 잎보다 유의적으로 월등히 높은 Cd함량을 나타냈다. 그렇지만 Cd + P처리에서는 뿌리뿐만 아니라 잎에서도 Cd의 식물전이가 유의적으로 감소되었다 (Fig. 1). 그러나 무처리와 P처리의 Cd은 모든 식물체 부위에서 검출되지 않았다. Cd의 식물체 내로의 흡수․이행은 식물의 종류에 따라 다양한 양상을 나타낸다. 또한 식물의 뿌리, 줄기, 잎, 그리고 종실 등의 조직부위별로도 큰 차이를 보인다. 이는 식물 및 품종에 따라 그들 조직 내로의 Cd 흡수․축적 능력에 따라 상이한 차이가 있음을 시사하는 것이다 (Fergusson, 1990; Park et al., 2009; Jung et al., 2015, 2016).
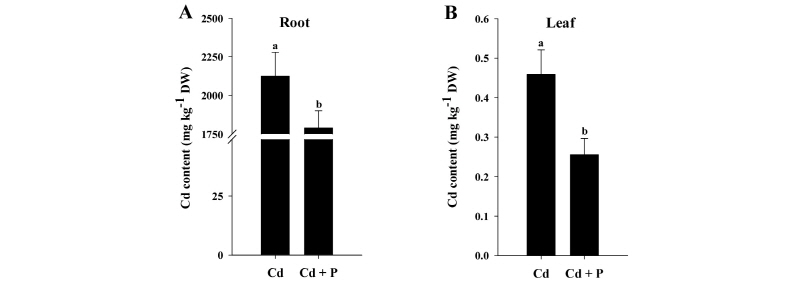
Fig. 1.
Effects of phosphorus (P) on the cadmium (Cd) content of rice plants grown in Cd-treated hydroponics. Rice seedlings at the four-leaf stage were cultivated in a hydroponics containing 30 µM Cd, with or without 6 mM P, for 14 days. Following treatment, the levels of Cd in the roots (A) and leaves (B) were measured via inductively coupled plasma-mass spectroscopy (ICP-MS) analysis. Each data point is the mean ± standard error (SE) of three replications. Means denoted by the same letter are not significantly different at the 5% level, according to Fisher’s least significant difference (LSD) tests.
Cd + P처리에 따른 P의 흡수에 있어, P을 처리하지 않은 뿌리의 무처리와 Cd처리 간에는 통계적인 차이가 없었던 반면 잎에서는 Cd처리가 무처리보다 오히려 높은 함량을 나타냈다. P함량의 경우, P시용 조건 하에서 Cd의 존재유무에 따라 뿌리와 잎 간에는 상이한 반응차이를 보였다. 뿌리의 P함량은 P처리에서 Cd + P처리보다 유의적으로 높게 검출되었지만, 잎은 반대의 경향으로 Cd + P처리에서 P처리보다 월등히 높은 함량을 나타냈다 (Fig. 2). 이상의 결과에 근거하여, 벼 뿌리 및 잎으로의 카드뮴전이에 P의 시용효과가 확인되었다. 뿌리에서 16% 감소를 나타냈고, 특히 지상부인 잎으로의 전이를 44% 감소시킴으로써 전반적인 카드뮴독성을 완화시키는 것으로 판단된다 (Jiang et al., 2007; Mishra et al., 2014; Sajwan et al., 2002).
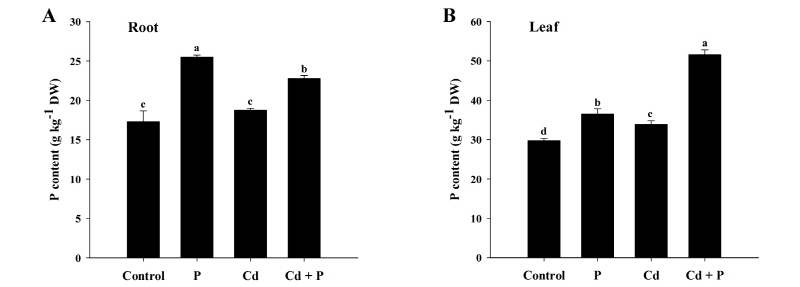
Fig. 2.
Effects of phosphorus (P) on the P content of rice plants grown in cadmium (Cd)-treated hydroponics. Rice seedlings at the four-leaf stage were cultivated in a hydroponics containing 30 µM Cd, with or without 6 mM P, for 14 days. Following treatment, the levels of P in the roots (A) and leaves (B) were measured via inductively coupled plasma-mass spectroscopy (ICP-MS) analysis. Each data point is the mean ± standard error (SE) of three replications. Means denoted by the same letter are not significantly different at the 5% level, according to Fisher’s least significant difference (LSD) tests.
활성산소종과 지질과산화 변화 카드뮴독성으로 인하여 유도되는 산화적 스트레스 정도를 분석하기 위하여, Cd 또는 P을 처리하고 처리 후 14일에 superoxide와 H2O2 함량 및 지질과산화작용의 지표화학물질인 MDA 생성량을 조사하였다.
Superoxide 함량에 있어, 무처리와 P처리 간의 뿌리에서는 통계적 차이가 없었다 (Fig. 3A). 그렇지만 잎에서는 P처리가 다른 처리구에 비해 유의적으로 높게 나타났던 반면 Cd처리와의 비교에서는 통계적인 차이가 없었다 (Fig. 3B). 무처리와 비교한 Cd처리의 superoxide 함량은 뿌리에서는 7.6배 그리고 잎에서는 1.5배가 높게 생성되었음에도 불구하고, Cd + P처리의 뿌리에서는 1.3배 그리고 잎에서는 2배를 감소시켰다 (Fig. 3). 그러나 잎에서의 P처리 및 Cd처리 모두에서 높은 생성량을 나타냈지만, Cd + P처리에서는 오히려 낮게 생성되었다. 이는 식물체 내에서의 P영향으로 인하여 Cd의 뿌리에서 잎으로 전이를 낮춤으로써 superoxide 생성을 감소시키는 것으로 판단된다.
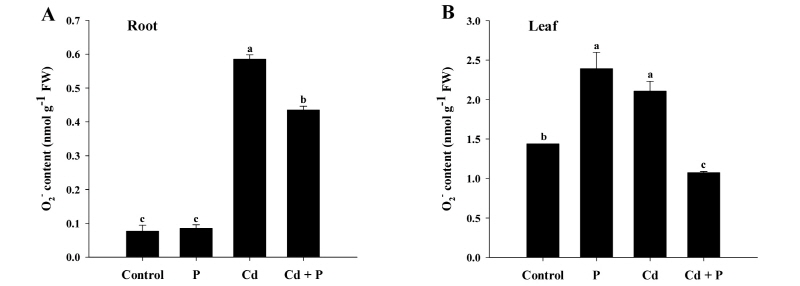
Fig. 3.
Effects of phosphorus (P) on the levels of superoxide (O2•−) in rice plants grown in cadmium (Cd)-treated hydroponics. Rice seedlings at the four-leaf stage were cultivated in a hydroponics containing 30 µM Cd, with or without 6 mM P, for 14 days. Following treatment, the levels of O2•− in the roots (A) and leaves (B) were measured. Each data point is the mean ± standard error (SE) of three replications. Means denoted by the same letter are not significantly different at the 5% level, according to Fisher’s least significant difference (LSD) tests.
뿌리의 H2O2 함량은 superoxide와 비슷한 경향으로 Cd처리에서 증가했던 반면 (Fig. 4A) 잎에서는 오히려 무처리보다 다소 낮게 검출되었으며, 특히 P처리에서 가장 적은 함량을 나타냈다 (Fig. 4B). Cd처리에 P시용에 따른 H2O2 생성량 변화에 있어, 뿌리에서는 약간 감소시키는 효과가 확인되었지만 잎에서는 유의적인 차이가 없었다 (Fig. 4).
지질과산화작용의 최종산물인 MDA 생성량 또한 무처리에 비해 Cd처리의 뿌리에서 2.4배 그리고 잎에서 1.4배가 더 많이 생성되었다. 그렇지만 뿌리와 잎 모두에서 Cd + P처리에 따른 Cd의 독성으로 유도되는 MDA의 생성량을 낮추는 효과를 확인하였다 (Fig. 5).
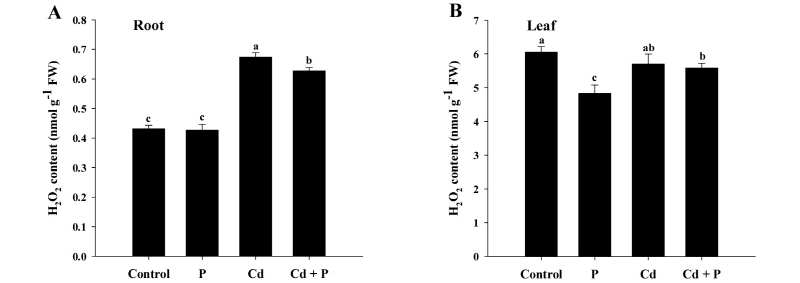
Fig. 4.
Effects of phosphorus (P) on the levels of H2O2 in rice plants grown in cadmium (Cd)-treated hydroponics. Rice seedlings at the four-leaf stage were cultivated in a hydroponics containing 30 µM Cd, with or without 6 mM P, for 14 days. Following treatment, the levels of H2O2 in the roots (A) and leaves (B) were measured. Each data point is the mean ± standard error (SE) of three replications. Means denoted by the same letter are not significantly different at the 5% level, according to Fisher’s least significant difference (LSD) tests.
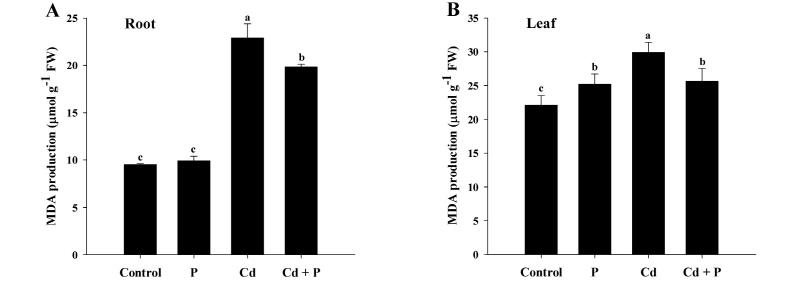
Fig. 5.
Effects of phosphorus (P) on the levels of malondialdehyde (MDA) production in rice plants grown in cadmium (Cd)-treated hydroponics. Rice seedlings at the four-leaf stage were cultivated in a hydroponics containing 30 µM Cd, with or without 6 mM P, for 14 days. Following treatment, the levels of MDA in the roots (A) and leaves (B) were measured. Each data point is the mean ± standard error (SE) of three replications. Means denoted by the same letter are not significantly different at the 5% level, according to Fisher’s least significant difference (LSD) tests.
카드뮴독성 완화를 위한 산화적 스트레스 산물인 활성산소종 (superoxide와 H2O2)과 지질과산화 작용의 최종산물인 MDA 생성량에 있어, P의 시용효과가 확연히 나타남을 확인할 수 있었다 (Figs. 3~5). Cd + P처리에서 Cd 농도의 감소는 뿌리 세포벽의 바깥 부분에서 탄소 또는 칼슘 등 양이온들과의 복합체를 형성하여 식물체 내로의 전이를 낮추는 결과를 초래할 수도 있을 것이다 (Siebers et al., 2013). 그럼에도 불구하고 우리의 연구결과와 비슷한 보고는 화본과 작물인 밀 (wheat)에서의 결과에서 찾아볼 수 있었고, P시용에 따라 H2O2 생성량이 감소됨으로써 전체적인 지질과산화가 완화된다는 결과를 제시하였다 (Arshad et al., 2016). 그러므로 P처리에 따른 Cd의 흡수․이행저감은 카드뮴독성으로 인하여 야기되는 활성산소종인 superoxide와 H2O2 및 지질과산화작용의 지표화학물질인 MDA 생성량의 감소로 이어짐으로 써, 벼 유묘의 카드뮴 독성경감에 효과를 나타내는 것으로 판단된다.
함황아미노산과 항산화제 변화 카드뮴의 무독화에 있어 중요한 역할을 담당하는 함황아미노산인 시스테인 (cysteine)과 항산화제인 glutathione (GSH) 및 ascorbate (AsA)의 변화를 측정하였다. 시스테인함량 변화에 있어, 무처리와 비교한 P처리의 모든 식물부위에서 유의적으로 높은 시스테인 함량을 나타냈다. 그렇지만 Cd처리의 뿌리는 Cd + P처리보다 낮은 함량을 보였던 반면, 잎에서는 반대의 경향으로 오히려 높게 나타났다 (Fig. 6).
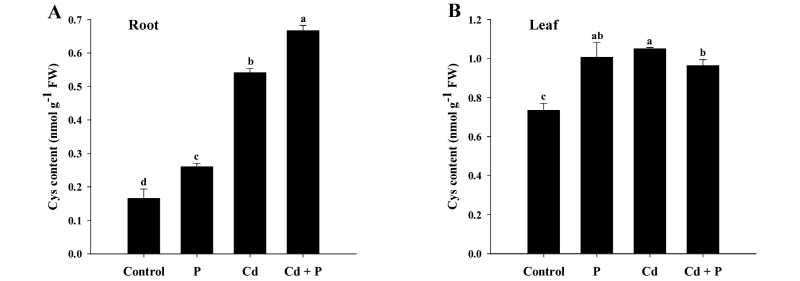
Fig. 6.
Changes in the content of cysteine (Cys) in rice plants grown in cadmium (Cd)-treated hydroponics. Rice seedlings at the four-leaf stage were cultivated in a hydroponics containing 30 µM Cd, with or without 6 mM P, for 14 days. Following treatment, the levels of Cys in the roots (A) and leaves (B) were measured. Each data point is the mean ± standard error (SE) of three replications. Means denoted by the same letter are not significantly different at the 5% level, according to Fisher’s least significant difference (LSD) tests.
GSH의 경우 뿌리에서는 Cd과 P처리 간에 통계적인 차이가 없었던 반면 잎의 경우 Cd + P처리에서 다소 낮게 나타남을 확인할 수 있었다 (Fig. 7A and B). Cd을 처리하지 않은 무처리에 있어, P시용 유무에 따라 뿌리와 잎의 두 조직 모두에서 통계적인 차이를 나타내지 않았지만 Cd + P처리에서는 AsA 함량이 크게 증가됨을 관찰할 수 있었다 (Fig. 7C and D). Arshad et al. (2016)의 밀 연구결과에서도 Cd 스트레스 하에서 P처리 농도에 비례적으로 AsA 함량이 증가되어, 카드뮴독성으로 인하여 발생되는 과잉의 활성산소종 소거에 중요한 역할을 담당함으로써 총체적인 식물독성을 완화한다는 결론과 매우 유사한 결과를 보여주는 것이다. 이는 카드뮴독성의 무독화와 경감에 관여하는 항산화제인 GSH의 변화에는 유의적 차이가 없이 오히려 P처리에 따라 감소하는 결과를 나타냈음에도 불구하고, 세포 내의 활성산소종 소거와 산화․환원 조절에 중요한 역할을 담당하는 항산화제인 AsA 역할의 중요성을 시사하는 결과라 생각된다 (Arshad et al., 2016; Mishra et al., 2014).
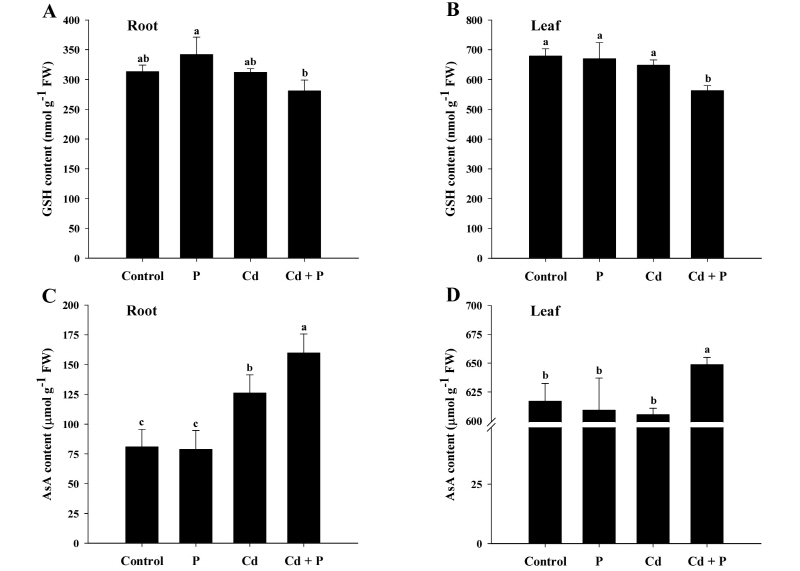
Fig. 7.
Changes in the content of glutathione (GSH) and ascorbate (AsA) in rice plants grown in cadmium (Cd)-treated hydroponics. Rice seedlings at the four-leaf stage were cultivated in a hydroponics containing 30 µM Cd, with or without 6 mM P, for 14 days. Following treatment, the levels of GSH and AsA in the roots (A, C) and leaves (B, D) were measured. Each data point is the mean ± standard error (SE) of three replications. Means denoted by the same letter are not significantly different at the 5% level, according to Fisher’s least significant difference (LSD) tests.
Conclusions
본 연구의 종합적인 결론은 벼의 카드뮴 흡수․이행증가는 활성산소종을 증가시키고 지질과산화를 높이므로 전반적인 생물체량을 감소시켰다. 또한 벼 체내의 카드뮴 무독화를 위해 함황아미노산과 항산화제의 변화를 유발하였다. 그러나 Cd + P처리에 따라 Cd의 식물체 내로의 흡수․이행이 낮아졌고, GSH-AsA cycle 활성을 증대시켜 카드뮴독성으로 인하여 발생되는 활성산소종 소거를 증진함으로써 총체적인 식물독성경감에 기여하였다. 그러므로 카드뮴 오염지에서 P시용은 Cd의 식물전이를 절감시킬 수 있는 하나의 방안이 될 수 있을 것이다. 그렇지만 카드뮴독성에 대한 P의 시용효과를 명확히 하기 위하여 실제로 카드뮴에 오염된 포장에서 P의 적정수준 연구가 필요할 것으로 생각된다.